引用本文: 江楓, 周偉, 張竹紅, 赫天耕. 感染性心內膜炎合并眼內炎繼發黃斑裂孔一例. 中華眼底病雜志, 2020, 36(2): 143-144. doi: 10.3760/cma.j.issn.1005-1015.2020.02.011 復制
患者女,47歲。因左眼視力驟降伴胸悶、憋氣1 d于2016年8月18日就診于天津醫科大學總醫院急診科。既往高血壓病病史10年。2個月前當地醫院行拔牙手術,之后牙齦出血、腫脹,予以口服抗生素治療,具體不詳。1.5個月前出現發熱,伴寒戰、乏力,未正規診療,未監測體溫,自行應用“安乃近、阿莫西林、復方氨酚烷胺”處理。4 d前就診當地醫院,建議住院治療,患者拒絕,帶口服藥物及靜脈藥物回家治療,具體藥物不詳。1 d前左眼突然視力驟降,同時伴胸悶、憋氣,于外院眼科診斷為“(1)左眼眼內炎?(2)左眼結核性葡萄膜炎?”。
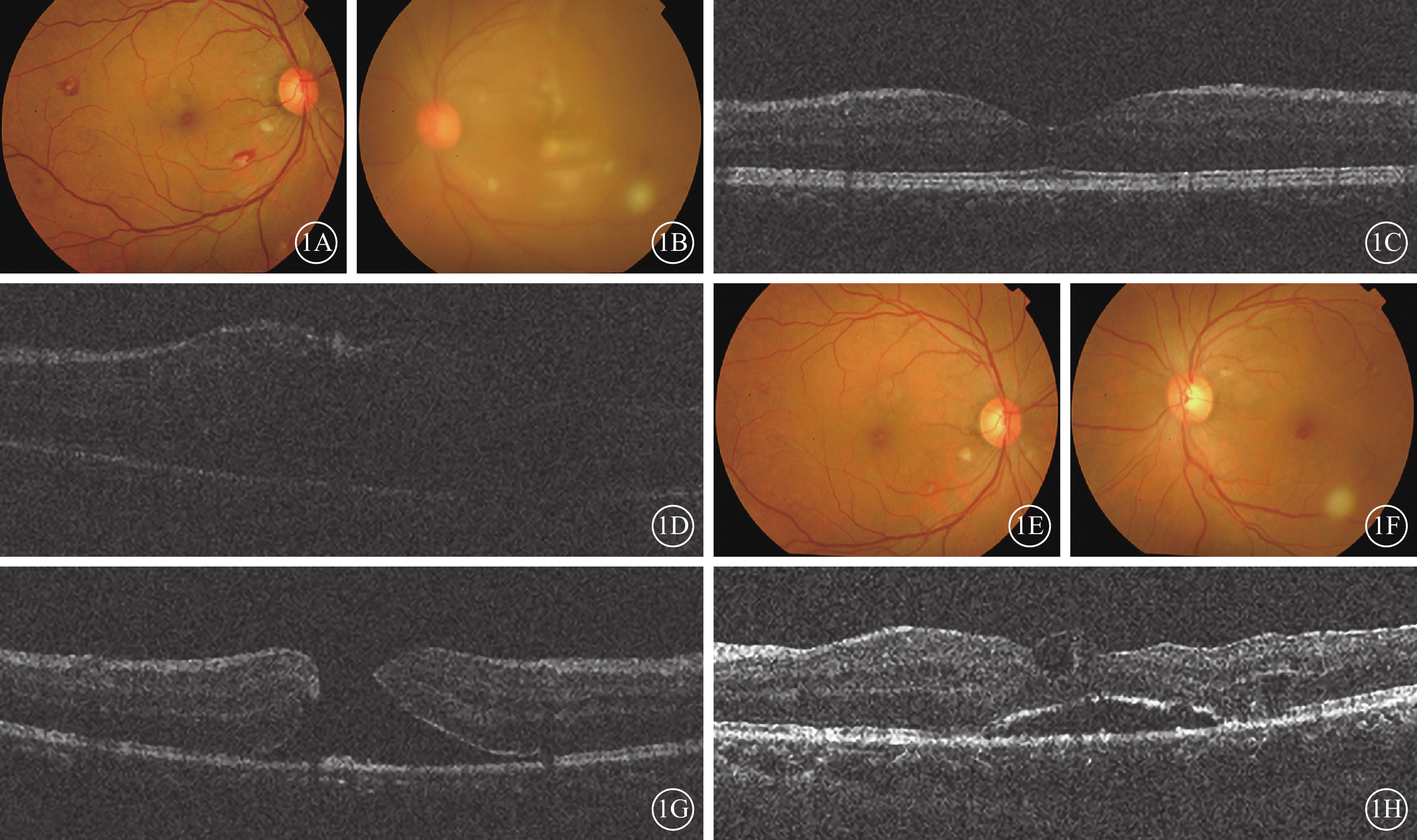
全身檢查:體溫39 ℃,主動脈瓣區4/6級舒張期雜音。心臟彩色超聲檢查,升主動脈及主動脈增寬,主動脈瓣脫垂、穿孔、反流(重度)、合并贅生物,三尖瓣反流(輕度)。眼科檢查:右眼BCVA 1.0,左眼數指/眼前。右眼眼前節正常,Tyn(?),玻璃體輕度混濁,眼底可見Roth斑及棉絨斑;左眼混合性充血(++++),角膜后灰白色KP(++),前房中深,Tyn(++++),下方積膿0.5 mm,瞳孔直徑約3 mm,對光反應遲鈍,瞳孔緣絮狀滲出,玻璃體重度灰白色塵狀混濁明顯,眼底極朦朧,隱約見后極部視網膜灰白色病灶(圖1A,1B)。黃斑區OCT檢查,右眼未見異常;左眼屈光間質不清晰,隱約見黃斑區RPE脫離(圖1C,1D)。急診科以“感染性心內膜炎(IE)、主動脈瓣贅生物、主動脈瓣脫垂伴反流、心功能Ⅲ級(NYHA)、左眼內源性眼內炎、右眼膿毒性視網膜炎、高血壓病3級(極高危)”收治入住心血管外科。入院后患者完善血培養等檢查,全身予以青霉素鈉480萬U,4次/d靜脈滴注經驗性抗感染治療,脫水減輕心臟負擔及對癥營養治療;雙眼局部予以妥布霉素地塞米松滴眼液抗炎抗感染、普拉洛芬滴眼液抗炎、復方托吡卡胺滴眼液散瞳等治療,同時完善心臟手術前檢查。3次血培養結果提示咽峽炎鏈球菌感染(青霉素鈉敏感)。患者于2016年8月23日全身麻醉體外循環下行主動脈瓣置換手術,手術后繼續抗感染治療12 d。治療后復查,右眼、左眼BCVA 1.0、0.04。雙眼眼前節正常。右眼玻璃體輕度混濁,眼底原Roth斑及棉絨斑基本吸收;左眼玻璃體腔輕度灰白色塵狀混濁,原視網膜灰白色病灶明顯吸收,黃斑裂孔形成(圖1E,1F)。OCT檢查,右眼未見異常;左眼黃斑區中心凹處可見視網膜結構全層缺失(圖1G)。補充臨床診斷:左眼黃斑裂孔。主動脈瓣置換手術后8個月行左眼玻璃體切割聯合內界膜剝除手術,手術后左眼視力0.12,黃斑裂孔基本閉合(圖1H)。
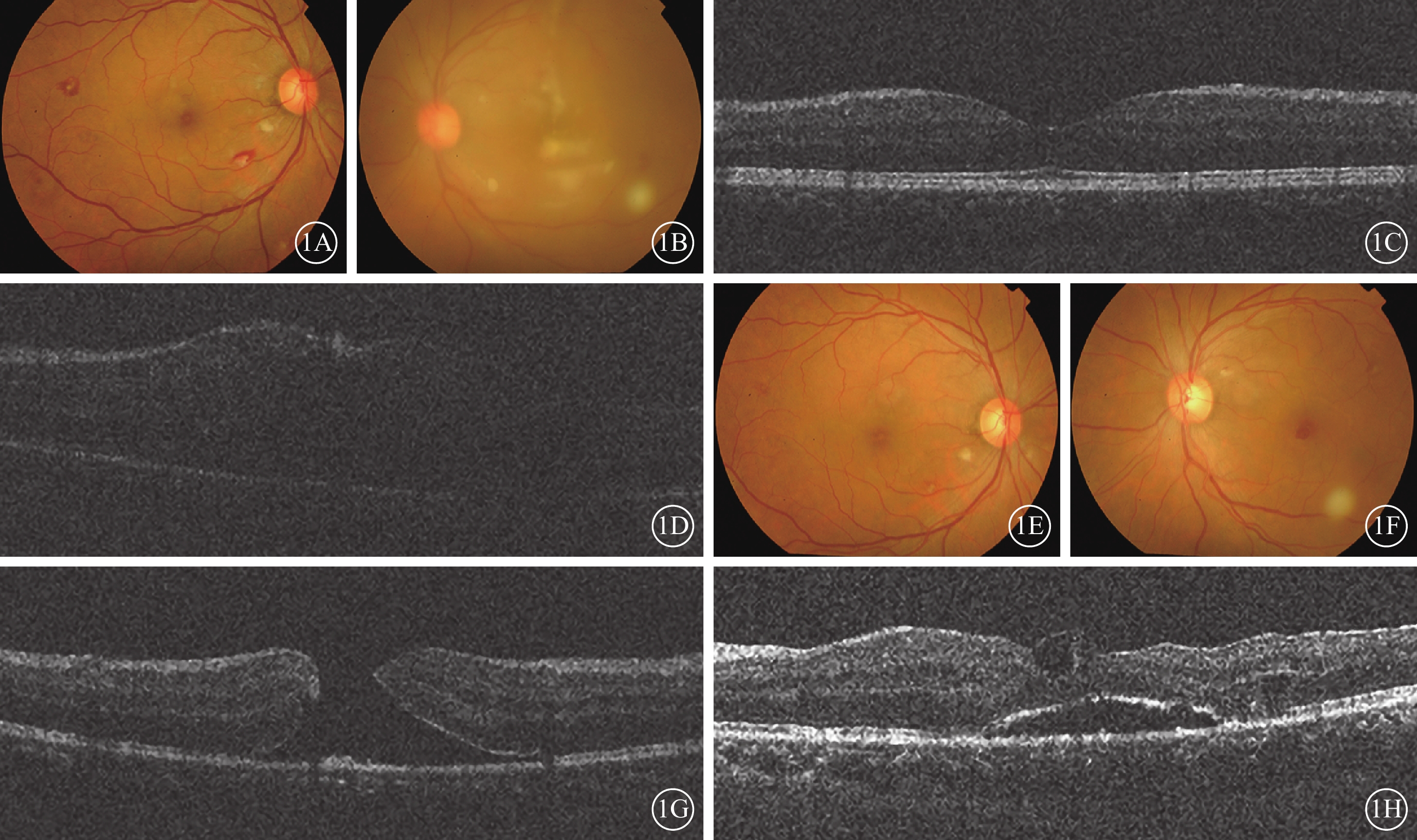 圖1
患者治療前后眼部檢查像。1A、1B分別示治療前右眼、左眼彩色眼底像,右眼Roth斑和棉絨斑;左眼玻璃體混濁,眼底朦朧,后極部可見灰白色病灶。1C、1D分別示治療前右眼、左眼OCT像,右眼視網膜結構未見異常;左眼隱約見黃斑區RPE脫離。1E、1F分別示右眼、左眼主動脈瓣置換手術后彩色眼底像,右眼Roth斑和棉絨斑基本吸收;左眼玻璃體混濁吸收,眼底灰白色病灶大部分吸收,黃斑裂孔形成。1G示主動脈瓣置換手術后患者左眼OCT像,黃斑區中心凹處視網膜結構全層缺失。1H示玻璃體切割聯合內界膜剝除手術后左眼OCT像,可見黃斑區中心凹視網膜結構基本連續
圖1
患者治療前后眼部檢查像。1A、1B分別示治療前右眼、左眼彩色眼底像,右眼Roth斑和棉絨斑;左眼玻璃體混濁,眼底朦朧,后極部可見灰白色病灶。1C、1D分別示治療前右眼、左眼OCT像,右眼視網膜結構未見異常;左眼隱約見黃斑區RPE脫離。1E、1F分別示右眼、左眼主動脈瓣置換手術后彩色眼底像,右眼Roth斑和棉絨斑基本吸收;左眼玻璃體混濁吸收,眼底灰白色病灶大部分吸收,黃斑裂孔形成。1G示主動脈瓣置換手術后患者左眼OCT像,黃斑區中心凹處視網膜結構全層缺失。1H示玻璃體切割聯合內界膜剝除手術后左眼OCT像,可見黃斑區中心凹視網膜結構基本連續
討論 IE是指因細菌、真菌和其他微生物直接感染而產生心瓣膜或心室壁內膜的炎癥,主要由草綠色鏈球菌引起[1]。本例患者為較少見的咽峽炎鏈球菌引起。咽峽炎鏈球菌屬于米勒鏈球菌組,易形成膿腫[2]。在口腔中,米勒鏈球菌存在于牙齦溝和義齒組織面,與牙齦炎、牙周炎等牙周疾病相關,能形成牙源性膿腫,后者可能是本例患者菌血癥的來源。米勒鏈球菌分咽峽炎鏈球菌、星座鏈球菌和中間鏈球菌,其中咽峽炎鏈球菌與IE關系最為密切[2]。本例患者在拔牙后出現局部癥狀,隨即出現發熱、乏力及寒戰等全身癥狀,局部感染引起菌血癥,未正規診治,繼而出現眼部及心臟受累癥狀。
患者就診時心臟彩色超聲檢查顯示主動脈瓣脫垂、穿孔、反流(重度)、合并贅生物,表明心臟瓣膜累及時間較長,心臟瓣膜可能為患者菌血癥重要的病原菌來源。IE眼部并發癥一方面通過病原菌的血行播散直接引起眼部感染,同時,病原菌栓子也能繼發局部免疫性炎癥[1]。IE合并眼部并發癥較少見,僅有個案報道[3-11]。常見的有眼內炎、葡萄膜炎、脈絡膜病變,或僅僅表現為Roth斑;少見的有眶蜂窩織炎[10]。IE合并黃斑裂孔臨床少見,目前發病原因和機制尚不明確。本例患者雙眼體征不一致,右眼僅出現Roth斑及棉絨斑,左眼則呈現感染性眼內炎表現。雙眼眼部表現不一致的原因可能與雙側頸總動脈的解剖不同有關。左側頸總動脈直接由主動脈弓發出,更接近心臟;右側頸總動脈則由頭臂動脈發出,因此內源性眼內炎可能更多發于左眼。不同于外源性眼內炎,內源性眼內炎伴有血眼屏障功能破壞,靜脈輸注敏感抗生素不僅能治療原發灶感染,也能透過血眼屏障有效治療眼內感染[12]。因此,患者雙眼癥狀體征均在全身及局部抗感染治療后明顯改善。右眼病灶基本吸收;左眼玻璃體混濁吸收,黃斑水腫消退,但最終發展為黃斑裂孔。Beatty等[3]曾報道一例β溶血性鏈球菌引起IE,同時眼底出現棉絨斑、Roth斑及線狀出血等典型的IE相關眼部表現,并最終形成黃斑裂孔;且其考慮黃斑裂孔形成可能由后部玻璃體增生牽拉引起。我們分析本例患者左眼最終發展為黃斑裂孔的原因可能是感染性眼內炎導致黃斑滲出、水腫以及玻璃體的牽拉。
IE眼部病變大部分預后良好,但若病變累及黃斑區,則預后較差。也有報道IE合并內源性眼內炎引起雙眼視力無光感的病例[11]。及時使用穿透性好的抗生素治療感染性眼內炎至關重要,推遲治療可能影響視力預后。有研究報道,約37.5%的感染性眼內炎患者最終喪失視力,多次玻璃體腔及球周注射抗生素和地塞米松能減少內源性眼內炎患者眼球摘除的手術幾率[12];而全身抗感染治療同時早期行玻璃體切割手術治療效果更好[13]。本例患者眼部發病時心臟瓣膜受損嚴重,需及時行瓣膜置換手術挽救患者生命;幸運的是患者在積極的全身及局部抗感染治療下左眼眼內炎得到控制,但由于發生黃斑裂孔,最終視力受到一定影響。
患者女,47歲。因左眼視力驟降伴胸悶、憋氣1 d于2016年8月18日就診于天津醫科大學總醫院急診科。既往高血壓病病史10年。2個月前當地醫院行拔牙手術,之后牙齦出血、腫脹,予以口服抗生素治療,具體不詳。1.5個月前出現發熱,伴寒戰、乏力,未正規診療,未監測體溫,自行應用“安乃近、阿莫西林、復方氨酚烷胺”處理。4 d前就診當地醫院,建議住院治療,患者拒絕,帶口服藥物及靜脈藥物回家治療,具體藥物不詳。1 d前左眼突然視力驟降,同時伴胸悶、憋氣,于外院眼科診斷為“(1)左眼眼內炎?(2)左眼結核性葡萄膜炎?”。
全身檢查:體溫39 ℃,主動脈瓣區4/6級舒張期雜音。心臟彩色超聲檢查,升主動脈及主動脈增寬,主動脈瓣脫垂、穿孔、反流(重度)、合并贅生物,三尖瓣反流(輕度)。眼科檢查:右眼BCVA 1.0,左眼數指/眼前。右眼眼前節正常,Tyn(?),玻璃體輕度混濁,眼底可見Roth斑及棉絨斑;左眼混合性充血(++++),角膜后灰白色KP(++),前房中深,Tyn(++++),下方積膿0.5 mm,瞳孔直徑約3 mm,對光反應遲鈍,瞳孔緣絮狀滲出,玻璃體重度灰白色塵狀混濁明顯,眼底極朦朧,隱約見后極部視網膜灰白色病灶(圖1A,1B)。黃斑區OCT檢查,右眼未見異常;左眼屈光間質不清晰,隱約見黃斑區RPE脫離(圖1C,1D)。急診科以“感染性心內膜炎(IE)、主動脈瓣贅生物、主動脈瓣脫垂伴反流、心功能Ⅲ級(NYHA)、左眼內源性眼內炎、右眼膿毒性視網膜炎、高血壓病3級(極高危)”收治入住心血管外科。入院后患者完善血培養等檢查,全身予以青霉素鈉480萬U,4次/d靜脈滴注經驗性抗感染治療,脫水減輕心臟負擔及對癥營養治療;雙眼局部予以妥布霉素地塞米松滴眼液抗炎抗感染、普拉洛芬滴眼液抗炎、復方托吡卡胺滴眼液散瞳等治療,同時完善心臟手術前檢查。3次血培養結果提示咽峽炎鏈球菌感染(青霉素鈉敏感)。患者于2016年8月23日全身麻醉體外循環下行主動脈瓣置換手術,手術后繼續抗感染治療12 d。治療后復查,右眼、左眼BCVA 1.0、0.04。雙眼眼前節正常。右眼玻璃體輕度混濁,眼底原Roth斑及棉絨斑基本吸收;左眼玻璃體腔輕度灰白色塵狀混濁,原視網膜灰白色病灶明顯吸收,黃斑裂孔形成(圖1E,1F)。OCT檢查,右眼未見異常;左眼黃斑區中心凹處可見視網膜結構全層缺失(圖1G)。補充臨床診斷:左眼黃斑裂孔。主動脈瓣置換手術后8個月行左眼玻璃體切割聯合內界膜剝除手術,手術后左眼視力0.12,黃斑裂孔基本閉合(圖1H)。
 圖1
患者治療前后眼部檢查像。1A、1B分別示治療前右眼、左眼彩色眼底像,右眼Roth斑和棉絨斑;左眼玻璃體混濁,眼底朦朧,后極部可見灰白色病灶。1C、1D分別示治療前右眼、左眼OCT像,右眼視網膜結構未見異常;左眼隱約見黃斑區RPE脫離。1E、1F分別示右眼、左眼主動脈瓣置換手術后彩色眼底像,右眼Roth斑和棉絨斑基本吸收;左眼玻璃體混濁吸收,眼底灰白色病灶大部分吸收,黃斑裂孔形成。1G示主動脈瓣置換手術后患者左眼OCT像,黃斑區中心凹處視網膜結構全層缺失。1H示玻璃體切割聯合內界膜剝除手術后左眼OCT像,可見黃斑區中心凹視網膜結構基本連續
圖1
患者治療前后眼部檢查像。1A、1B分別示治療前右眼、左眼彩色眼底像,右眼Roth斑和棉絨斑;左眼玻璃體混濁,眼底朦朧,后極部可見灰白色病灶。1C、1D分別示治療前右眼、左眼OCT像,右眼視網膜結構未見異常;左眼隱約見黃斑區RPE脫離。1E、1F分別示右眼、左眼主動脈瓣置換手術后彩色眼底像,右眼Roth斑和棉絨斑基本吸收;左眼玻璃體混濁吸收,眼底灰白色病灶大部分吸收,黃斑裂孔形成。1G示主動脈瓣置換手術后患者左眼OCT像,黃斑區中心凹處視網膜結構全層缺失。1H示玻璃體切割聯合內界膜剝除手術后左眼OCT像,可見黃斑區中心凹視網膜結構基本連續
討論 IE是指因細菌、真菌和其他微生物直接感染而產生心瓣膜或心室壁內膜的炎癥,主要由草綠色鏈球菌引起[1]。本例患者為較少見的咽峽炎鏈球菌引起。咽峽炎鏈球菌屬于米勒鏈球菌組,易形成膿腫[2]。在口腔中,米勒鏈球菌存在于牙齦溝和義齒組織面,與牙齦炎、牙周炎等牙周疾病相關,能形成牙源性膿腫,后者可能是本例患者菌血癥的來源。米勒鏈球菌分咽峽炎鏈球菌、星座鏈球菌和中間鏈球菌,其中咽峽炎鏈球菌與IE關系最為密切[2]。本例患者在拔牙后出現局部癥狀,隨即出現發熱、乏力及寒戰等全身癥狀,局部感染引起菌血癥,未正規診治,繼而出現眼部及心臟受累癥狀。
患者就診時心臟彩色超聲檢查顯示主動脈瓣脫垂、穿孔、反流(重度)、合并贅生物,表明心臟瓣膜累及時間較長,心臟瓣膜可能為患者菌血癥重要的病原菌來源。IE眼部并發癥一方面通過病原菌的血行播散直接引起眼部感染,同時,病原菌栓子也能繼發局部免疫性炎癥[1]。IE合并眼部并發癥較少見,僅有個案報道[3-11]。常見的有眼內炎、葡萄膜炎、脈絡膜病變,或僅僅表現為Roth斑;少見的有眶蜂窩織炎[10]。IE合并黃斑裂孔臨床少見,目前發病原因和機制尚不明確。本例患者雙眼體征不一致,右眼僅出現Roth斑及棉絨斑,左眼則呈現感染性眼內炎表現。雙眼眼部表現不一致的原因可能與雙側頸總動脈的解剖不同有關。左側頸總動脈直接由主動脈弓發出,更接近心臟;右側頸總動脈則由頭臂動脈發出,因此內源性眼內炎可能更多發于左眼。不同于外源性眼內炎,內源性眼內炎伴有血眼屏障功能破壞,靜脈輸注敏感抗生素不僅能治療原發灶感染,也能透過血眼屏障有效治療眼內感染[12]。因此,患者雙眼癥狀體征均在全身及局部抗感染治療后明顯改善。右眼病灶基本吸收;左眼玻璃體混濁吸收,黃斑水腫消退,但最終發展為黃斑裂孔。Beatty等[3]曾報道一例β溶血性鏈球菌引起IE,同時眼底出現棉絨斑、Roth斑及線狀出血等典型的IE相關眼部表現,并最終形成黃斑裂孔;且其考慮黃斑裂孔形成可能由后部玻璃體增生牽拉引起。我們分析本例患者左眼最終發展為黃斑裂孔的原因可能是感染性眼內炎導致黃斑滲出、水腫以及玻璃體的牽拉。
IE眼部病變大部分預后良好,但若病變累及黃斑區,則預后較差。也有報道IE合并內源性眼內炎引起雙眼視力無光感的病例[11]。及時使用穿透性好的抗生素治療感染性眼內炎至關重要,推遲治療可能影響視力預后。有研究報道,約37.5%的感染性眼內炎患者最終喪失視力,多次玻璃體腔及球周注射抗生素和地塞米松能減少內源性眼內炎患者眼球摘除的手術幾率[12];而全身抗感染治療同時早期行玻璃體切割手術治療效果更好[13]。本例患者眼部發病時心臟瓣膜受損嚴重,需及時行瓣膜置換手術挽救患者生命;幸運的是患者在積極的全身及局部抗感染治療下左眼眼內炎得到控制,但由于發生黃斑裂孔,最終視力受到一定影響。