引用本文: 高云霞, 安靚琪, 曾志冰, 婁華東, 吳國強, 陸方. 脈絡膜上腔注射透明質酸鈉墊壓手術治療單純性孔源性視網膜脫離12例. 中華眼底病雜志, 2019, 35(3): 274-278. doi: 10.3760/cma.j.issn.1005-1015.2019.03.013 復制
鞏膜扣帶手術(SB)和玻璃體切割手術是治療孔源性視網膜脫離(RRD)的兩類常規手術方式。與玻璃體切割手術相比,SB手術具有副作用小、對玻璃體擾動少、手術后高眼壓發生率低等優勢,且兩者治療效果相似;因此,SB被認為是治療早期單純性RRD的首選術式之一[1]。常規SB手術是采用間接檢眼鏡定位視網膜裂孔,并需要在鞏膜壁外固定置入硅膠帶或硅膠海綿墊壓視網膜裂孔,但因其對鞏膜壁的持續施壓,可造成眼球變形、眼軸變長導致屈光度變化、眼球運動障礙、斜視、眼前節缺血等并發癥,甚至出現異物肉芽腫或因植入物不可吸收可能出現異物被排斥、感染、脫落等一系列并發癥[2]。探尋一種操作簡便、并發癥少且能同樣達到促使視網膜復位的視網膜脫離修復手術具有重要的臨床意義。本研究采用脈絡膜上腔注射透明質酸鈉墊壓手術對一組單純性RRD進行了治療,對其視網膜復位情況進行了觀察。現將結果報道如下。
1 對象和方法
2018年10月至2019年2月在四川大學華西醫院眼科臨床確診為單純性RRD患者12例12只眼納入本研究。其中,男性7例,女性5例。年齡15~66歲,平均年齡(32.40±14.81)歲。年齡15~30歲7例,31~50歲3例,50歲以上3例。病程6~30 d,平均病程(19.58±13.48)d。
納入標準:(1)屈光間質無明顯混濁,可窺清眼底;(2)單純性裂孔性視網膜脫離;(3)單個裂孔或多個裂孔累及1個或多個象限;(3)裂孔位于視網膜中周部附近;(4)增生性玻璃體視網膜病變(PVR)≤C2。排除標準:(1)屈光間質混濁,無法窺清眼底或局部混濁影響操作;(2)IOL眼;(3)周邊裂孔巨大,邊緣卷曲明顯,裂孔進入后極部區域;(4)PVR≥C3;(5)復發性視網膜脫離或伴隨其他阻塞性或感染性眼底病變。
所有患眼行BCVA、眼壓、眼部B型超聲、雙目間接檢眼鏡、OCT及掃描激光檢眼鏡(SLO)檢查。12只眼中,BCVA<0.1、0.1~0.4、>0.4各4只眼(33.33%)。眼壓<10 mmHg(1 mmHg=0.133 kPa)4只眼(33.33%),10~15 mmHg 5只眼(41.67%),>15 mmHg 3只眼(25.00%)。視網膜脫離范圍累及1個象限(圖1A)3只眼(25.00%),累及2個象限7只眼(58.33%),累及3、4個象限各1只眼(8.33%)。視網膜脫離已累及黃斑(圖1B)8只眼(66.67%)。視網膜裂孔位于顳上方7只眼(58.33%),位于顳下方3只眼(25.00%),位于鼻上方2只眼(16.67%)。裂孔為小圓孔8只眼(66.67%),馬蹄樣裂孔3只眼(25.00%),不規則裂孔1只眼(8.33%)。PVR A級4只眼(33.33%),B級6只眼(50.00%),C1級2只眼(16.67%)。正視眼 2只眼(16.67%),近視眼10只眼(83.33%)。屈光度-3.00~-6.00 D 1只眼(8.33%);>-6.00 D 9只眼(75.00%)。
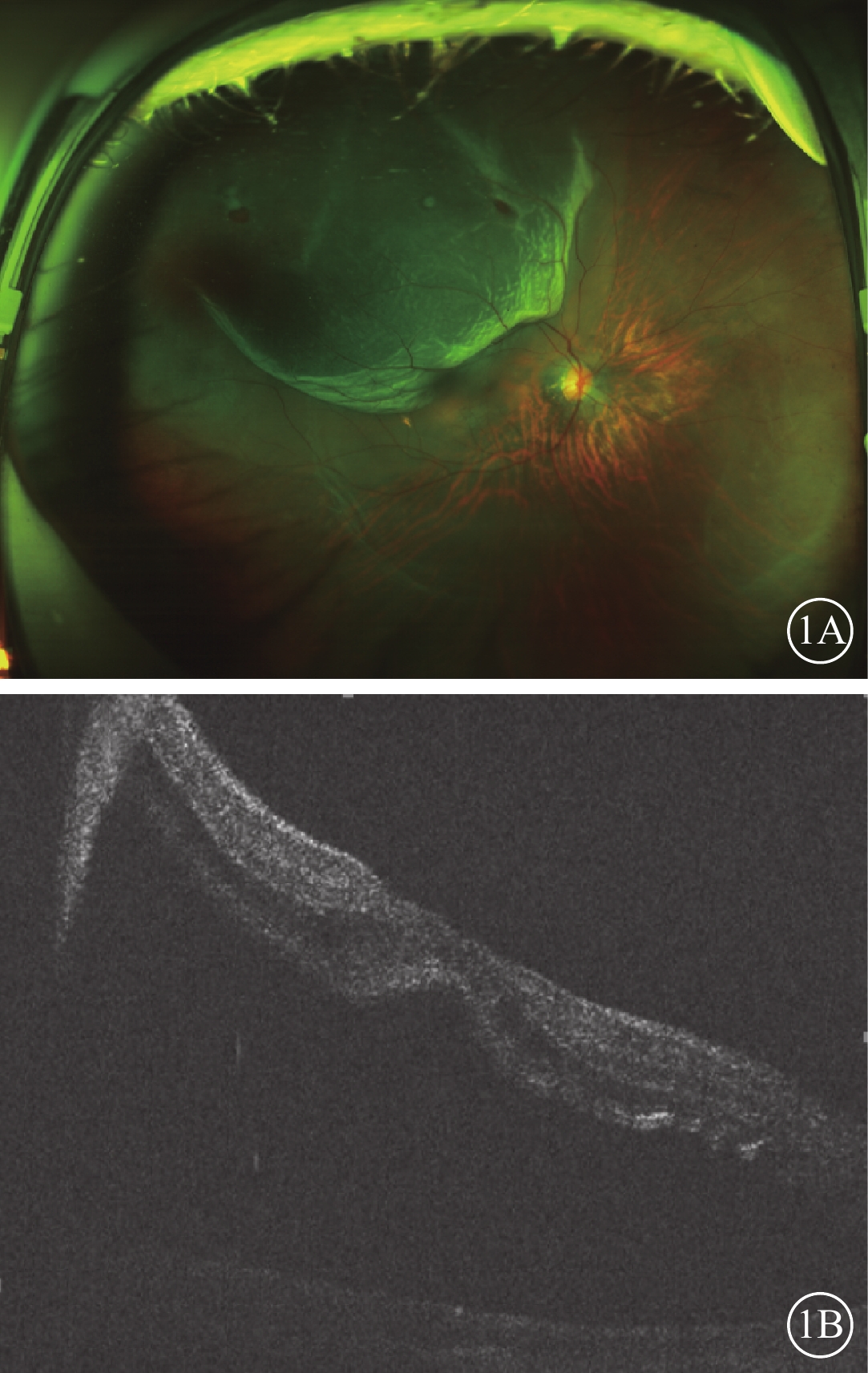 圖1
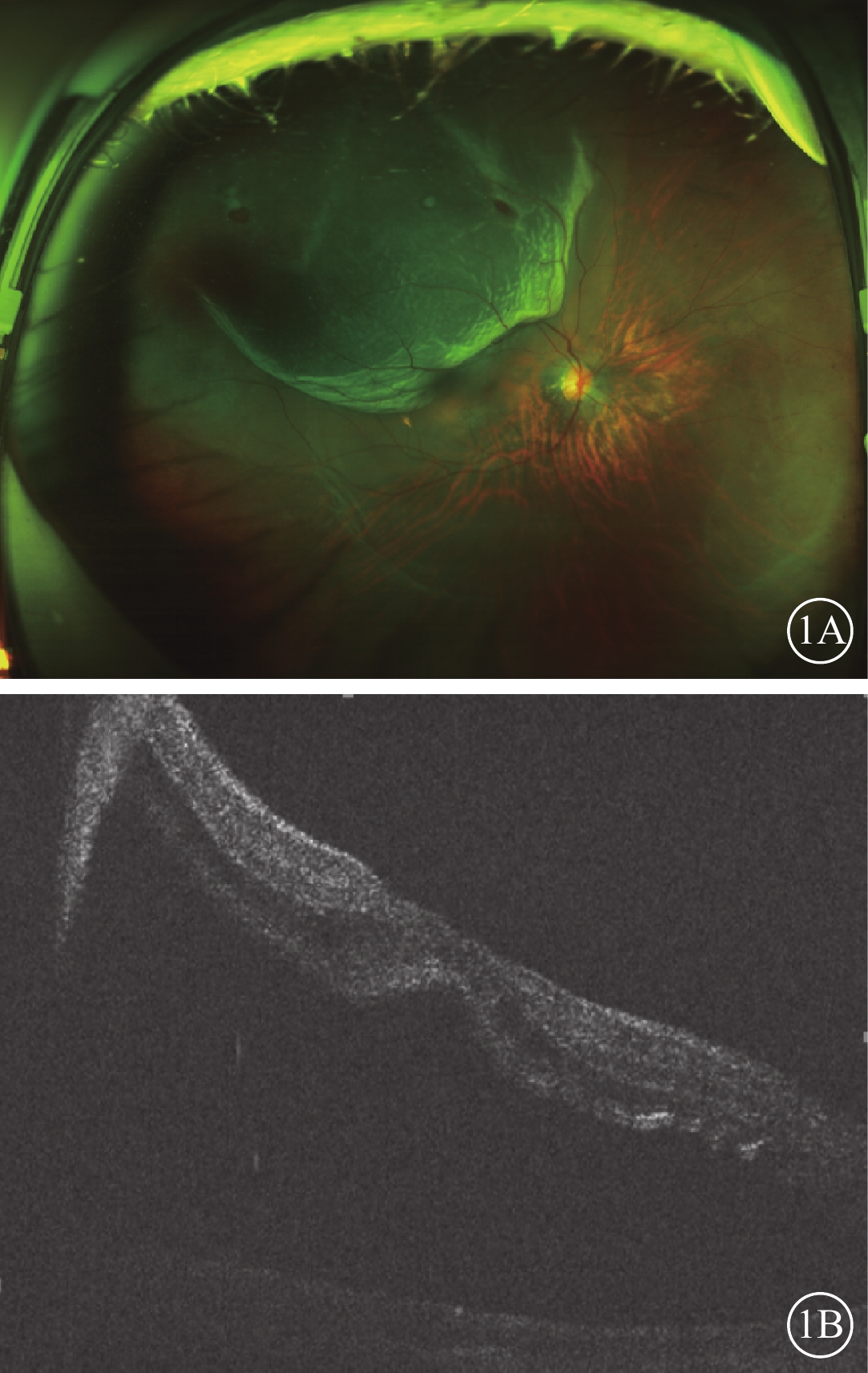
患眼手術前SLO及OCT像。1A示SLO像,可見右眼顳上方視網膜呈青灰色隆起,隆起區可見兩個小圓孔;1B示OCT像,可見黃斑區神經上皮脫離
圖1
患眼手術前SLO及OCT像。1A示SLO像,可見右眼顳上方視網膜呈青灰色隆起,隆起區可見兩個小圓孔;1B示OCT像,可見黃斑區神經上皮脫離
所有患眼在廣域顯微鏡帶內照明系統輔助下行脈絡膜上腔注射透明質酸鈉墊壓手術。手術均由同一位具有豐富手術經驗的醫師完成。患眼經2%利多卡因球后麻醉,在手術顯微鏡下于睫狀體平坦部距角鞏膜緣3.5 mm處并避開裂孔所在象限穿刺25G套管(圖2A),插入光纖照明,放置非接觸廣角系統,仔細檢查全視網膜,尋找視網膜裂孔及變性區(圖2B)并進行定位。對應視網膜裂孔處先行鞏膜外冷凍(圖2C),再根據視網膜脫離隆起較高區域選擇放液部位穿刺放出適量視網膜下液;在裂孔所在象限于兩條直肌之間,距角鞏膜緣6~8 mm處做4~6 mm結膜小切口,分離Tenon’s囊暴露其下鞏膜,做1~2 mm鞏膜板層小切口,分離剩余板層鞏膜(圖2D)。待恰巧穿透鞏膜后,應用自帶鈍性針頭將醫用透明質酸鈉凝膠(德國Bausch Lomb公司)置入鞏膜下、脈絡膜上腔(圖2E)。在顯微鏡直視下緩慢將透明質酸鈉推注入脈絡膜上腔,待顯微鏡下觀察到脈絡膜形成局限性嵴樣隆起并確認視網膜裂孔位于該嵴上(圖2F)后拔出鈍性針頭,8-0可吸收線縫合鞏膜切口及結膜切口各1針。再次在顯微鏡直視下檢查視網膜,必要時對裂孔再行激光光凝以加固裂孔周圍視網膜,最后拔出鞏膜穿刺套管。手術結束后囑患者向裂孔方側臥休息2周,確保裂孔始終呈低位。手術后1周內根據復查情況安排患者行視網膜激光光凝進一步加固裂孔周圍視網膜。
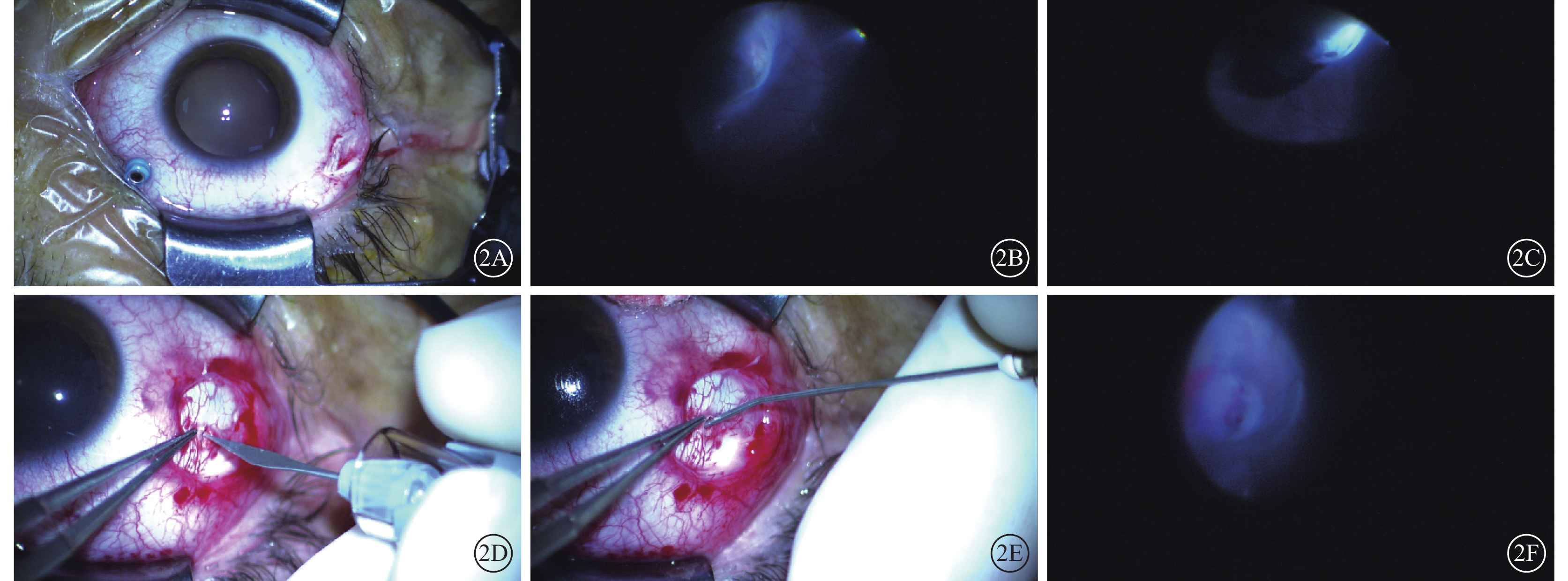 圖2
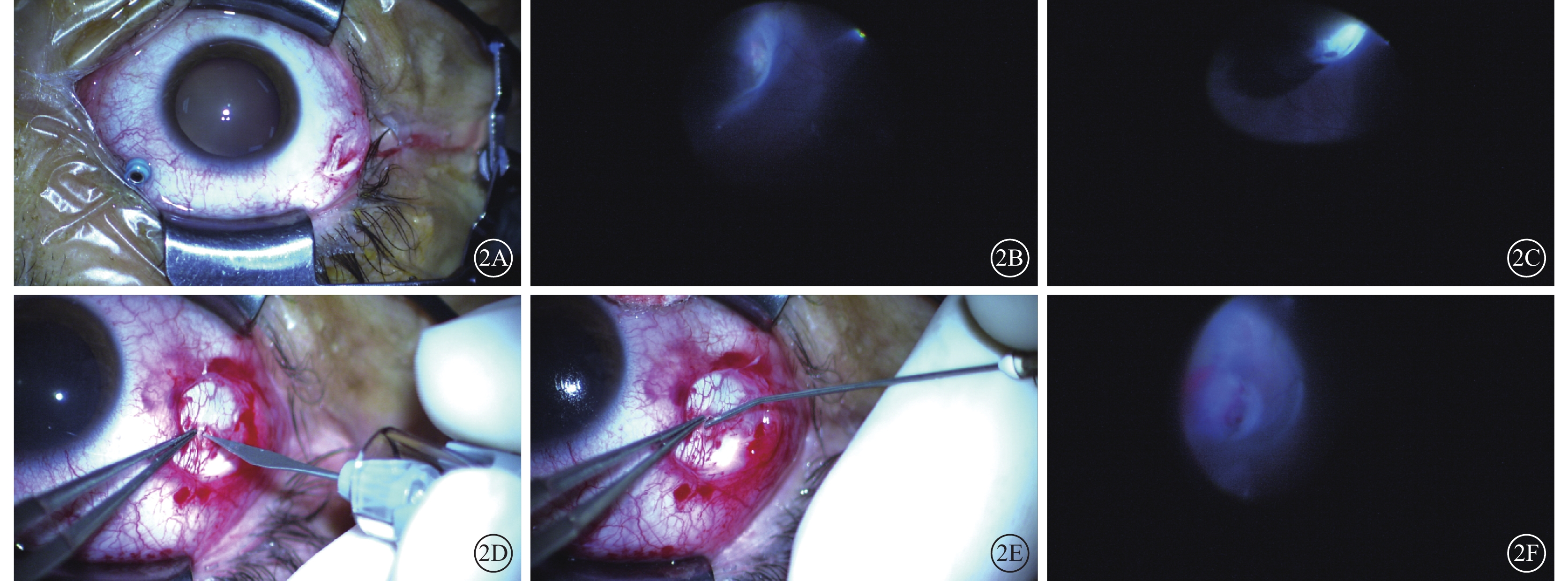
手術操作圖。2A示于睫狀體平坦部距角鞏膜緣3.5 mm處穿刺25G套管;2B示顯微鏡下檢查全視網膜,定位視網膜裂孔;2C示顯微鏡下對視網膜裂孔行鞏膜外冷凍;2D示在視網膜裂孔區域做2 mm鞏膜板層切口,分離剩余板層鞏膜;2E示通過自帶鈍性針頭將醫用透明質酸鈉凝膠置入鞏膜下及脈絡膜上腔;2F示顯微鏡下確認脈絡膜形成局限性嵴樣隆起且視網膜裂孔位于該嵴上
圖2
手術操作圖。2A示于睫狀體平坦部距角鞏膜緣3.5 mm處穿刺25G套管;2B示顯微鏡下檢查全視網膜,定位視網膜裂孔;2C示顯微鏡下對視網膜裂孔行鞏膜外冷凍;2D示在視網膜裂孔區域做2 mm鞏膜板層切口,分離剩余板層鞏膜;2E示通過自帶鈍性針頭將醫用透明質酸鈉凝膠置入鞏膜下及脈絡膜上腔;2F示顯微鏡下確認脈絡膜形成局限性嵴樣隆起且視網膜裂孔位于該嵴上
手術后1 d,1、2周及1、2個月,采用與手術前相同的設備和方法行眼科相關檢查,密切觀察患眼手術后裂孔位置、結膜外觀及視網膜解剖復位情況。以手術后1周為視網膜復位與否的觀察時間點。以雙目間接檢眼鏡、SLO檢查結果確定裂孔是否閉合,以眼部B型超聲、雙目間接檢眼鏡、OCT及SLO檢查結果確定視網膜是否復位。視網膜完全復位:OCT示神經上皮層下無積液,眼部B型超聲未見異常帶狀回聲,雙目間接檢眼鏡及SLO見視網膜復貼、視網膜顏色紅潤。視網膜部分復位:OCT示黃斑區視網膜下少許積液,但較手術前明顯改善;眼部B型超聲可有或無淺帶狀局限性回聲;雙目間接檢眼鏡及SLO見視網膜基本復貼,裂孔封閉良好。視網膜未復位:OCT示神經上皮層下大量積液;眼部B型超聲見明顯帶狀回聲;雙目間接檢眼鏡及SLO見視網膜青灰色隆起,裂孔未封閉。
2 結果
12只眼手術時間18~25 min。手術中患者配合良好,未訴明顯肌肉牽拉痛及其他疼痛感。手術中出現視網膜下少許出血3只眼,其中伴輕度玻璃體積血2只眼,均于手術后1周~1個月內逐漸吸收;未發生脈絡膜上腔暴發性出血和醫源性視網膜裂孔。手術后1周內進行補充激光光凝加固裂孔周圍視網膜7只眼。
12只眼中,視網膜完全復位(圖3A)6只眼(50.00%),部分復位伴黃斑區視網膜下液(圖3B)4只眼(33.33%),未復位2只眼(16.67%)。視網膜部分復位伴黃斑區視網膜下液患眼原視網膜裂孔均位于脈絡膜墊壓嵴上,裂孔封閉;給予密切隨訪,視網膜下液隨時間延長逐漸吸收。視網膜未復位的2只眼均為高度近視眼,其中1只眼因脫離時間較長已形成3個裂孔且視網膜下見增生條帶,另1只眼為2 DD大小的馬蹄樣裂孔且視網膜脫離范圍累及4個象限;其采用玻璃體切割聯合硅油填充手術或鞏膜外硅膠墊壓手術復位視網膜。
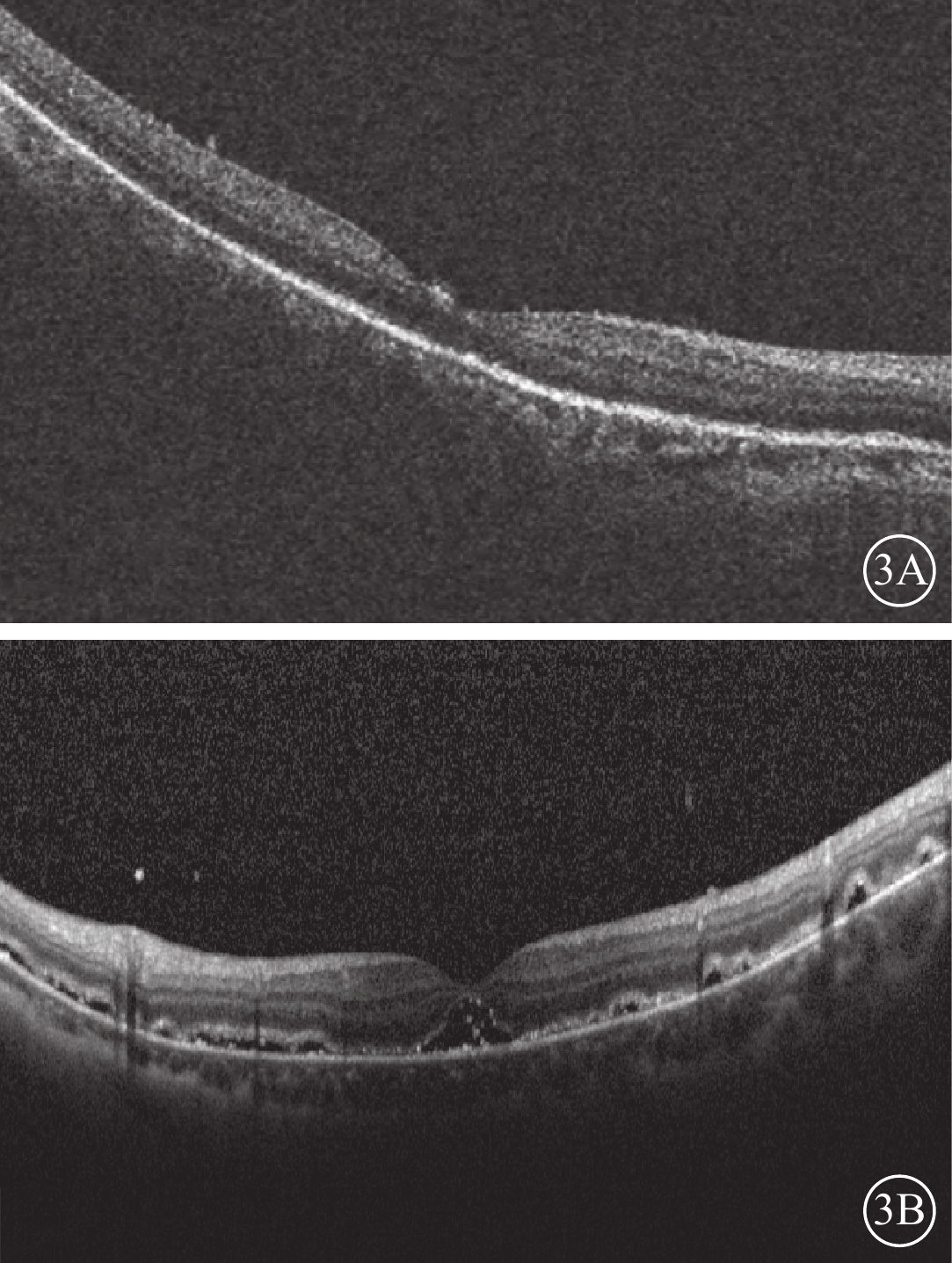 圖3
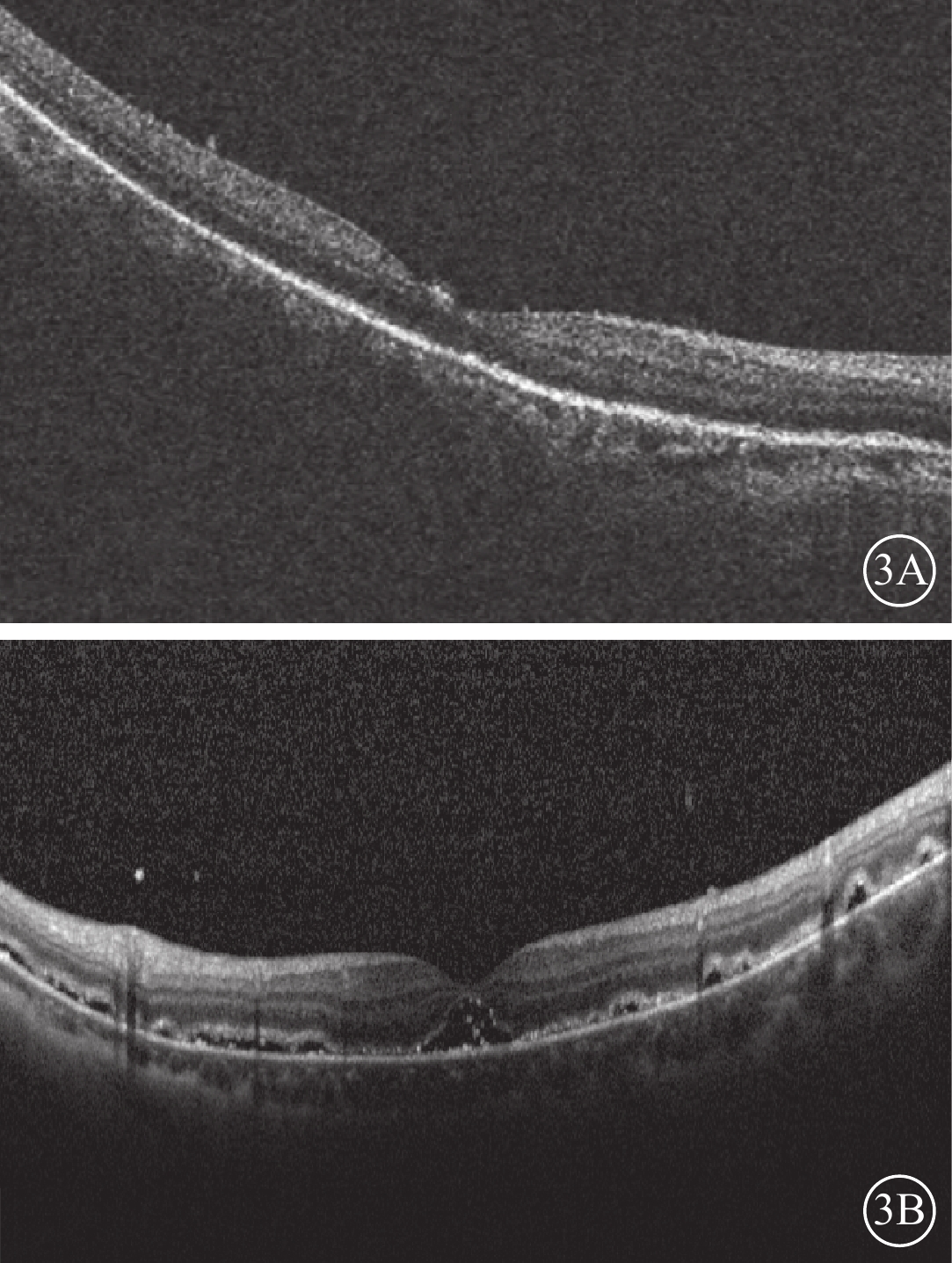
患眼手術后1周OCT像。3A示黃斑區神經上皮完整復位;3B示視網膜部分復位,黃斑區視網膜下少許積液
圖3
患眼手術后1周OCT像。3A示黃斑區神經上皮完整復位;3B示視網膜部分復位,黃斑區視網膜下少許積液
12只眼中,手術后1周,墊壓嵴隆起形態較好且能有效頂壓裂孔10只眼,墊壓嵴形態扁平、裂孔閉合不佳且裂孔周圍視網膜淺脫離2只眼。手術后2周,墊壓嵴明顯變小6只眼,墊壓嵴基本消失4只眼。手術后1個月,所有患眼墊壓嵴完全消失,脈絡膜平復;其中10只眼視網膜裂孔緣瘢痕形成,裂孔封閉。
手術后1 d,所有患眼眼壓均較手術前有所提高。其中,眼壓在正常范圍(10~21 mmHg)內11只眼;輕度超出正常范圍1只眼(24.8 mmHg),觀察1周后眼壓恢復正常。所有患眼隨訪期間均未出現遲發性出血、感染性眼內炎、眼壓升高、白內障、葡萄膜炎、眼球運動障礙、鞏膜暴露、結膜肉芽腫等并發癥。
3 討論
常規SB手術中使用不可吸收的固體硅膠或硅海綿長期頂壓球壁不僅可造成眼球形態改變從而引起屈光狀態變化,還可能引起高眼壓、脈絡膜和睫狀體脫離、復視、斜視、黃斑區皺褶、眼球破裂、眼部缺血、玻璃體積血甚至眼內炎等并發癥[2-6]。本研究取消了鞏膜壁固定放置硅膠或硅海綿,在國內首次公開采用已被廣泛運用于臨床內眼手術的透明質酸鈉[7-10],利用其凝膠狀態又可吸收的特性,將其注入脈絡膜上腔墊壓脈絡膜成嵴,從而起到短時間頂壓視網膜裂孔、促進視網膜復位的作用。結果顯示,12只眼手術時間18~25 min,手術耗時相對較短;僅有3只眼手術中出現視網膜下少許出血,其中伴輕度玻璃體積血2只眼,均于手術后1個月內逐漸吸收。這證明了脈絡膜上腔注射透明質酸鈉墊壓法治療RRD的安全性。
Schaal等[11]統計分析發現,常規SB手術治療322例原發性視網膜脫離患者的視網膜復位率為86%。本組50.00%的患眼視網膜完全復位,33.33%的患眼視網膜部分復位。這說明本手術方式能取得與常規SB手術相似的視網膜復位率。而與常規SB手術比較,本手術方式的優勢在于以下幾個方面。(1)提升患者的舒適度。由于本手術中不需要在裂孔周圍鞏膜外固定硅膠或硅海綿,因而不會牽拉肌肉或暴露眼球,提升了患者在手術中和手術后的舒適度。本組所有患者手術中均未訴明顯肌肉牽拉痛及其他疼痛感。(2)對裂孔位置沒有要求。常規SB手術為求頂壓效果通常需要視網膜裂孔位于赤道部或以前。本手術方式注射透明質酸鈉的部位為角鞏膜緣以后6~8 mm,不受裂孔位置限制。(3)切口小,與之相關的并發癥少。常規外路手術需沿角鞏膜緣剪開1個象限甚至全周剪開球結膜。若破壞正常結膜結構過多,可能對將來行青光眼、翼狀胬肉等結膜利用率高的手術造成不利影響;若結膜破壞過度,還將影響眼表的淚膜穩定性,從而造成手術后眼干澀、刺痛不適等癥狀[12]。本手術僅在裂孔所在象限做一長約4~6 mm的放射狀結膜切口,發生上述并發癥的可能性小。通過觀察我們發現,僅1只眼手術后1 d眼壓輕度高于正常范圍,但觀察1周后自行恢復正常。整個隨訪期間均未見遲發性出血、感染性眼內炎、眼壓升高等與手術相關的并發癥發生。另外,本手術在廣域顯微鏡帶內照明系統輔助下實施,該系統的使用可以明顯增強顯微鏡放大率和照明視野范圍,能更為清晰全面地觀察眼底,更容易發現全部裂孔,更好地了解視網膜脫離范圍、隆起高度、玻璃體狀態,并能在直視病變的情況下同時對其進行冷凍或光凝處理,操作更簡單、精細、準確、避免損傷健康組織,減少并發癥發生的可能[13-14]。
本組有2只眼手術后視網膜未復位,我們分析其原因可能與以下幾個方面有關。(1)玻璃體液化。2只眼均為高度近視眼,手術前玻璃體液化明顯,因此不再具備良好的頂壓裂孔作用。當1~2周透明質酸鈉吸收后視網膜再脫離,手術效果不能維持。(2)視網膜下增生及視網膜脫離范圍過大。2只眼中,1只眼因脫離時間較長已形成3個裂孔,視網膜下見增生條帶;另1只眼視網膜脫離范圍累及4個象限。(3)裂孔過大及其邊緣卷曲不規則、馬蹄樣裂孔。2只眼中有1只眼為2 DD的馬蹄樣裂孔。馬蹄樣裂孔常常伴隨一側未完全離斷的孔蓋被玻璃體增生牽拉,這可能導致鞏膜外冷凍或視網膜激光光凝無法完全封閉裂孔。由于透明質酸鈉是一種自身吸收較快的手術輔助材料,其形成的脈絡膜嵴一般在1~2周后消失,對裂孔的頂壓作用時間較短。本研究結果顯示,脈絡膜嵴僅能維持1周余,手術后2周復查時嵴已明顯變小或消失,失去頂壓和修復視網膜的作用。因此我們認為,脈絡膜上腔注入透明質酸鈉墊壓手術僅適用于早期單純性RRD,對于伴隨明顯玻璃體液化、PVR、視網膜廣泛脫離以及馬蹄樣帶孔蓋牽拉樣裂孔者應更慎重選擇,嚴格把控手術指征。
本研究結果表明,在廣域顯微鏡帶內照明系統輔助下應用脈絡膜上腔注射透明質酸鈉墊壓手術治療單純性RRD安全有效。但由于本研究樣本量較小、隨訪時間較短,且未對患者手術前后的視力進行定量統計分析,有關該手術方式治療單純性RRD的療效有待今后更大樣本量的病例對照研究加以驗證。
鞏膜扣帶手術(SB)和玻璃體切割手術是治療孔源性視網膜脫離(RRD)的兩類常規手術方式。與玻璃體切割手術相比,SB手術具有副作用小、對玻璃體擾動少、手術后高眼壓發生率低等優勢,且兩者治療效果相似;因此,SB被認為是治療早期單純性RRD的首選術式之一[1]。常規SB手術是采用間接檢眼鏡定位視網膜裂孔,并需要在鞏膜壁外固定置入硅膠帶或硅膠海綿墊壓視網膜裂孔,但因其對鞏膜壁的持續施壓,可造成眼球變形、眼軸變長導致屈光度變化、眼球運動障礙、斜視、眼前節缺血等并發癥,甚至出現異物肉芽腫或因植入物不可吸收可能出現異物被排斥、感染、脫落等一系列并發癥[2]。探尋一種操作簡便、并發癥少且能同樣達到促使視網膜復位的視網膜脫離修復手術具有重要的臨床意義。本研究采用脈絡膜上腔注射透明質酸鈉墊壓手術對一組單純性RRD進行了治療,對其視網膜復位情況進行了觀察。現將結果報道如下。
1 對象和方法
2018年10月至2019年2月在四川大學華西醫院眼科臨床確診為單純性RRD患者12例12只眼納入本研究。其中,男性7例,女性5例。年齡15~66歲,平均年齡(32.40±14.81)歲。年齡15~30歲7例,31~50歲3例,50歲以上3例。病程6~30 d,平均病程(19.58±13.48)d。
納入標準:(1)屈光間質無明顯混濁,可窺清眼底;(2)單純性裂孔性視網膜脫離;(3)單個裂孔或多個裂孔累及1個或多個象限;(3)裂孔位于視網膜中周部附近;(4)增生性玻璃體視網膜病變(PVR)≤C2。排除標準:(1)屈光間質混濁,無法窺清眼底或局部混濁影響操作;(2)IOL眼;(3)周邊裂孔巨大,邊緣卷曲明顯,裂孔進入后極部區域;(4)PVR≥C3;(5)復發性視網膜脫離或伴隨其他阻塞性或感染性眼底病變。
所有患眼行BCVA、眼壓、眼部B型超聲、雙目間接檢眼鏡、OCT及掃描激光檢眼鏡(SLO)檢查。12只眼中,BCVA<0.1、0.1~0.4、>0.4各4只眼(33.33%)。眼壓<10 mmHg(1 mmHg=0.133 kPa)4只眼(33.33%),10~15 mmHg 5只眼(41.67%),>15 mmHg 3只眼(25.00%)。視網膜脫離范圍累及1個象限(圖1A)3只眼(25.00%),累及2個象限7只眼(58.33%),累及3、4個象限各1只眼(8.33%)。視網膜脫離已累及黃斑(圖1B)8只眼(66.67%)。視網膜裂孔位于顳上方7只眼(58.33%),位于顳下方3只眼(25.00%),位于鼻上方2只眼(16.67%)。裂孔為小圓孔8只眼(66.67%),馬蹄樣裂孔3只眼(25.00%),不規則裂孔1只眼(8.33%)。PVR A級4只眼(33.33%),B級6只眼(50.00%),C1級2只眼(16.67%)。正視眼 2只眼(16.67%),近視眼10只眼(83.33%)。屈光度-3.00~-6.00 D 1只眼(8.33%);>-6.00 D 9只眼(75.00%)。
 圖1
患眼手術前SLO及OCT像。1A示SLO像,可見右眼顳上方視網膜呈青灰色隆起,隆起區可見兩個小圓孔;1B示OCT像,可見黃斑區神經上皮脫離
圖1
患眼手術前SLO及OCT像。1A示SLO像,可見右眼顳上方視網膜呈青灰色隆起,隆起區可見兩個小圓孔;1B示OCT像,可見黃斑區神經上皮脫離
所有患眼在廣域顯微鏡帶內照明系統輔助下行脈絡膜上腔注射透明質酸鈉墊壓手術。手術均由同一位具有豐富手術經驗的醫師完成。患眼經2%利多卡因球后麻醉,在手術顯微鏡下于睫狀體平坦部距角鞏膜緣3.5 mm處并避開裂孔所在象限穿刺25G套管(圖2A),插入光纖照明,放置非接觸廣角系統,仔細檢查全視網膜,尋找視網膜裂孔及變性區(圖2B)并進行定位。對應視網膜裂孔處先行鞏膜外冷凍(圖2C),再根據視網膜脫離隆起較高區域選擇放液部位穿刺放出適量視網膜下液;在裂孔所在象限于兩條直肌之間,距角鞏膜緣6~8 mm處做4~6 mm結膜小切口,分離Tenon’s囊暴露其下鞏膜,做1~2 mm鞏膜板層小切口,分離剩余板層鞏膜(圖2D)。待恰巧穿透鞏膜后,應用自帶鈍性針頭將醫用透明質酸鈉凝膠(德國Bausch Lomb公司)置入鞏膜下、脈絡膜上腔(圖2E)。在顯微鏡直視下緩慢將透明質酸鈉推注入脈絡膜上腔,待顯微鏡下觀察到脈絡膜形成局限性嵴樣隆起并確認視網膜裂孔位于該嵴上(圖2F)后拔出鈍性針頭,8-0可吸收線縫合鞏膜切口及結膜切口各1針。再次在顯微鏡直視下檢查視網膜,必要時對裂孔再行激光光凝以加固裂孔周圍視網膜,最后拔出鞏膜穿刺套管。手術結束后囑患者向裂孔方側臥休息2周,確保裂孔始終呈低位。手術后1周內根據復查情況安排患者行視網膜激光光凝進一步加固裂孔周圍視網膜。
 圖2
手術操作圖。2A示于睫狀體平坦部距角鞏膜緣3.5 mm處穿刺25G套管;2B示顯微鏡下檢查全視網膜,定位視網膜裂孔;2C示顯微鏡下對視網膜裂孔行鞏膜外冷凍;2D示在視網膜裂孔區域做2 mm鞏膜板層切口,分離剩余板層鞏膜;2E示通過自帶鈍性針頭將醫用透明質酸鈉凝膠置入鞏膜下及脈絡膜上腔;2F示顯微鏡下確認脈絡膜形成局限性嵴樣隆起且視網膜裂孔位于該嵴上
圖2
手術操作圖。2A示于睫狀體平坦部距角鞏膜緣3.5 mm處穿刺25G套管;2B示顯微鏡下檢查全視網膜,定位視網膜裂孔;2C示顯微鏡下對視網膜裂孔行鞏膜外冷凍;2D示在視網膜裂孔區域做2 mm鞏膜板層切口,分離剩余板層鞏膜;2E示通過自帶鈍性針頭將醫用透明質酸鈉凝膠置入鞏膜下及脈絡膜上腔;2F示顯微鏡下確認脈絡膜形成局限性嵴樣隆起且視網膜裂孔位于該嵴上
手術后1 d,1、2周及1、2個月,采用與手術前相同的設備和方法行眼科相關檢查,密切觀察患眼手術后裂孔位置、結膜外觀及視網膜解剖復位情況。以手術后1周為視網膜復位與否的觀察時間點。以雙目間接檢眼鏡、SLO檢查結果確定裂孔是否閉合,以眼部B型超聲、雙目間接檢眼鏡、OCT及SLO檢查結果確定視網膜是否復位。視網膜完全復位:OCT示神經上皮層下無積液,眼部B型超聲未見異常帶狀回聲,雙目間接檢眼鏡及SLO見視網膜復貼、視網膜顏色紅潤。視網膜部分復位:OCT示黃斑區視網膜下少許積液,但較手術前明顯改善;眼部B型超聲可有或無淺帶狀局限性回聲;雙目間接檢眼鏡及SLO見視網膜基本復貼,裂孔封閉良好。視網膜未復位:OCT示神經上皮層下大量積液;眼部B型超聲見明顯帶狀回聲;雙目間接檢眼鏡及SLO見視網膜青灰色隆起,裂孔未封閉。
2 結果
12只眼手術時間18~25 min。手術中患者配合良好,未訴明顯肌肉牽拉痛及其他疼痛感。手術中出現視網膜下少許出血3只眼,其中伴輕度玻璃體積血2只眼,均于手術后1周~1個月內逐漸吸收;未發生脈絡膜上腔暴發性出血和醫源性視網膜裂孔。手術后1周內進行補充激光光凝加固裂孔周圍視網膜7只眼。
12只眼中,視網膜完全復位(圖3A)6只眼(50.00%),部分復位伴黃斑區視網膜下液(圖3B)4只眼(33.33%),未復位2只眼(16.67%)。視網膜部分復位伴黃斑區視網膜下液患眼原視網膜裂孔均位于脈絡膜墊壓嵴上,裂孔封閉;給予密切隨訪,視網膜下液隨時間延長逐漸吸收。視網膜未復位的2只眼均為高度近視眼,其中1只眼因脫離時間較長已形成3個裂孔且視網膜下見增生條帶,另1只眼為2 DD大小的馬蹄樣裂孔且視網膜脫離范圍累及4個象限;其采用玻璃體切割聯合硅油填充手術或鞏膜外硅膠墊壓手術復位視網膜。
 圖3
患眼手術后1周OCT像。3A示黃斑區神經上皮完整復位;3B示視網膜部分復位,黃斑區視網膜下少許積液
圖3
患眼手術后1周OCT像。3A示黃斑區神經上皮完整復位;3B示視網膜部分復位,黃斑區視網膜下少許積液
12只眼中,手術后1周,墊壓嵴隆起形態較好且能有效頂壓裂孔10只眼,墊壓嵴形態扁平、裂孔閉合不佳且裂孔周圍視網膜淺脫離2只眼。手術后2周,墊壓嵴明顯變小6只眼,墊壓嵴基本消失4只眼。手術后1個月,所有患眼墊壓嵴完全消失,脈絡膜平復;其中10只眼視網膜裂孔緣瘢痕形成,裂孔封閉。
手術后1 d,所有患眼眼壓均較手術前有所提高。其中,眼壓在正常范圍(10~21 mmHg)內11只眼;輕度超出正常范圍1只眼(24.8 mmHg),觀察1周后眼壓恢復正常。所有患眼隨訪期間均未出現遲發性出血、感染性眼內炎、眼壓升高、白內障、葡萄膜炎、眼球運動障礙、鞏膜暴露、結膜肉芽腫等并發癥。
3 討論
常規SB手術中使用不可吸收的固體硅膠或硅海綿長期頂壓球壁不僅可造成眼球形態改變從而引起屈光狀態變化,還可能引起高眼壓、脈絡膜和睫狀體脫離、復視、斜視、黃斑區皺褶、眼球破裂、眼部缺血、玻璃體積血甚至眼內炎等并發癥[2-6]。本研究取消了鞏膜壁固定放置硅膠或硅海綿,在國內首次公開采用已被廣泛運用于臨床內眼手術的透明質酸鈉[7-10],利用其凝膠狀態又可吸收的特性,將其注入脈絡膜上腔墊壓脈絡膜成嵴,從而起到短時間頂壓視網膜裂孔、促進視網膜復位的作用。結果顯示,12只眼手術時間18~25 min,手術耗時相對較短;僅有3只眼手術中出現視網膜下少許出血,其中伴輕度玻璃體積血2只眼,均于手術后1個月內逐漸吸收。這證明了脈絡膜上腔注射透明質酸鈉墊壓法治療RRD的安全性。
Schaal等[11]統計分析發現,常規SB手術治療322例原發性視網膜脫離患者的視網膜復位率為86%。本組50.00%的患眼視網膜完全復位,33.33%的患眼視網膜部分復位。這說明本手術方式能取得與常規SB手術相似的視網膜復位率。而與常規SB手術比較,本手術方式的優勢在于以下幾個方面。(1)提升患者的舒適度。由于本手術中不需要在裂孔周圍鞏膜外固定硅膠或硅海綿,因而不會牽拉肌肉或暴露眼球,提升了患者在手術中和手術后的舒適度。本組所有患者手術中均未訴明顯肌肉牽拉痛及其他疼痛感。(2)對裂孔位置沒有要求。常規SB手術為求頂壓效果通常需要視網膜裂孔位于赤道部或以前。本手術方式注射透明質酸鈉的部位為角鞏膜緣以后6~8 mm,不受裂孔位置限制。(3)切口小,與之相關的并發癥少。常規外路手術需沿角鞏膜緣剪開1個象限甚至全周剪開球結膜。若破壞正常結膜結構過多,可能對將來行青光眼、翼狀胬肉等結膜利用率高的手術造成不利影響;若結膜破壞過度,還將影響眼表的淚膜穩定性,從而造成手術后眼干澀、刺痛不適等癥狀[12]。本手術僅在裂孔所在象限做一長約4~6 mm的放射狀結膜切口,發生上述并發癥的可能性小。通過觀察我們發現,僅1只眼手術后1 d眼壓輕度高于正常范圍,但觀察1周后自行恢復正常。整個隨訪期間均未見遲發性出血、感染性眼內炎、眼壓升高等與手術相關的并發癥發生。另外,本手術在廣域顯微鏡帶內照明系統輔助下實施,該系統的使用可以明顯增強顯微鏡放大率和照明視野范圍,能更為清晰全面地觀察眼底,更容易發現全部裂孔,更好地了解視網膜脫離范圍、隆起高度、玻璃體狀態,并能在直視病變的情況下同時對其進行冷凍或光凝處理,操作更簡單、精細、準確、避免損傷健康組織,減少并發癥發生的可能[13-14]。
本組有2只眼手術后視網膜未復位,我們分析其原因可能與以下幾個方面有關。(1)玻璃體液化。2只眼均為高度近視眼,手術前玻璃體液化明顯,因此不再具備良好的頂壓裂孔作用。當1~2周透明質酸鈉吸收后視網膜再脫離,手術效果不能維持。(2)視網膜下增生及視網膜脫離范圍過大。2只眼中,1只眼因脫離時間較長已形成3個裂孔,視網膜下見增生條帶;另1只眼視網膜脫離范圍累及4個象限。(3)裂孔過大及其邊緣卷曲不規則、馬蹄樣裂孔。2只眼中有1只眼為2 DD的馬蹄樣裂孔。馬蹄樣裂孔常常伴隨一側未完全離斷的孔蓋被玻璃體增生牽拉,這可能導致鞏膜外冷凍或視網膜激光光凝無法完全封閉裂孔。由于透明質酸鈉是一種自身吸收較快的手術輔助材料,其形成的脈絡膜嵴一般在1~2周后消失,對裂孔的頂壓作用時間較短。本研究結果顯示,脈絡膜嵴僅能維持1周余,手術后2周復查時嵴已明顯變小或消失,失去頂壓和修復視網膜的作用。因此我們認為,脈絡膜上腔注入透明質酸鈉墊壓手術僅適用于早期單純性RRD,對于伴隨明顯玻璃體液化、PVR、視網膜廣泛脫離以及馬蹄樣帶孔蓋牽拉樣裂孔者應更慎重選擇,嚴格把控手術指征。
本研究結果表明,在廣域顯微鏡帶內照明系統輔助下應用脈絡膜上腔注射透明質酸鈉墊壓手術治療單純性RRD安全有效。但由于本研究樣本量較小、隨訪時間較短,且未對患者手術前后的視力進行定量統計分析,有關該手術方式治療單純性RRD的療效有待今后更大樣本量的病例對照研究加以驗證。