引用本文: 張哲, 劉竹青, 劉巨平, 東莉潔, 朱依萌, 黃亮瑜, 蘇睿虹, 趙今稚, 張曉敏, 李筱榮. 二甲雙胍聯合抗血管內皮生長因子藥物治療糖尿病視網膜病變的可能協同作用. 中華眼底病雜志, 2018, 34(5): 453-457. doi: 10.3760/cma.j.issn.1005-1015.2018.05.008 復制
抗血管內皮生長因子(VEGF)藥物治療糖尿病黃斑水腫(DME)有較好療效,但部分患者可能呈現反復發作、經久不愈的狀態[1]。二甲雙胍作為應用最廣泛的口服降糖藥之一,主要通過促進葡萄糖在脂肪組織的攝取,同時降低腸道吸收葡萄糖等來發揮降糖作用[2]。我們在臨床工作中發現,服用二甲雙胍的糖尿病視網膜病變(DR)患者對抗VEGF藥物治療的反應明顯優于未服用二甲雙胍者。據此我們推測二甲雙胍可能具有協同抗VEGF藥物治療的作用。為此,我們將二甲雙胍與抗VEGF藥物聯合應用于VEGF誘導的視網膜血管內皮細胞中,旨在從體外細胞實驗的角度探討二甲雙胍聯合抗VEGF藥物治療DR的可能協同作用。現將結果報道如下。
1 對象和方法
1.1 臨床資料回顧
2016年10~12月在我院行玻璃體腔注射抗VEGF藥物治療的DME患者10例12只眼納入本研究。所有患者均符合DR及DME的診斷標準[3, 4]。排除標準:(1)屈光度>?8.0 D以上;(2)眼壓>25 mmHg(1 mmHg=0.133 kPa);(3)有老年性黃斑變性、青光眼、角膜炎、結膜炎、葡萄膜炎等影響視力的其他眼病;(4)經光相干斷層掃描檢查證實存在黃斑前膜、玻璃體黃斑牽拉以及視網膜色素上皮萎縮、視網膜下纖維化或瘢痕等結構性損害;(5)前3個月內接受過眼內抗VEGF藥物治療;(6)前3個月內接受過眼內或眼周和全身系統性皮質類固醇激素治療;(7)眼部曾行玻璃體切割手術或鞏膜扣帶手術,白內障手術、Nd:YAG激光光凝治療時間短于3個月;(8)存在控制較差的糖尿病、高血壓以及心肌梗死、腦血管意外、腎衰竭等全身情況較差,研究者評估不能完成試驗者;(9)服用二甲雙胍時間短于1個月。
患者中,男性4例5只眼,女性6例7只眼。年齡50~76歲,平均年齡(62.9±7.7)歲。病程6~36個月,平均病程(16.4±6.1)個月。將患者隨機分為單純治療組(單純康柏西普治療)和聯合治療組(康柏西普+二甲雙胍)。治療前,兩組患者年齡、病程、視力、黃斑區中心凹視網膜厚度(CRT)比較,差異無統計學意義(P>0.05)(表1)。治療后隨訪3個月,對比分析兩組患者治療后的視力、CRT變化。
1.2 體外細胞實驗
恒河猴視網膜血管內皮細胞(RF-6A,天津醫科大學眼科研究所);磷酸鹽緩沖液(PBS)、RPMI1640培養液(上海源培生物科技股份有限公司);胰蛋白酶、胎牛血清、青鏈霉素、谷氨酰胺(美國Gibco公司);噻唑藍(MTT)試劑盒(北京索萊寶科技有限公司);6、96孔板(美國Life technologies公司);康柏西普(成都康弘藥業集團股份有限公司);二甲雙胍(美國Sigma公司);Trizol試劑盒(美國Invitrogen公司)。
實驗分為對照組(正常細胞)、VEGF組(50 ng/ml的VEGF)、單獨組(50 ng/ml的VEGF+2.5 μg/ml的康柏西普)、聯合組(50 ng/ml的VEGF+2.5 μg/ml的康柏西普+2.0 mmol/L的二甲雙胍)進行。采用含4.5 ml胎牛血清、0.45 ml雙抗、0.45 ml谷氨酰胺的RPMI1640培養液培養細胞,置于37 ℃、5%CO2培養箱中培養,3~5 d傳代1次,取對數生長期細胞用于實驗。將細胞培養24 h后,饑餓過夜,按實驗分組給予干預刺激72 h。
細胞生存力實驗。以細胞密度1×104個/孔接種于96孔板,24 h后更換為無血清培養基,饑餓過夜后按實驗分組予以干預刺激。每組3個復孔,實驗重復3次。培養72 h后棄培養基,加入90 μl新鮮培養液,再加入10 μl MTT溶液,繼續培養4 h后棄上清液,再加入100 μl二甲基亞砜充分震蕩混勻后,酶標儀490 nm處檢測各組吸光度[A,舊稱光密度(OD)]值。
細胞劃痕實驗。以細胞密度6×105個/孔接種于6孔板,每孔最終體系為2 ml,待生長融合為單層細胞后,用100~1000 μl微量加樣槍頭于每孔中央行“十”字形劃痕,PBS沖洗后拍照。按實驗分組予干預刺激,常規培養24 h后于相同位置再次拍照,觀察各孔細胞向裸區遷移情況,用cellSens Standard軟件測量裸區面積。實驗重復3次,按以下公式計算遷移率。遷移率=(S0-St)/S0×100%(S0:原始裸區面積,St:各時間點裸區面積)。
采用半定量實時逆轉錄(qRT)-聚合酶鏈反應(PCR)檢測各組細胞VEGF受體(VEGFR)2、蛋白激酶C(PKC)-α及PKC-β的mRNA表達。依據實驗分組準備細胞,行總RNA提取,超微量分光光度計檢測其濃度。將A260/A280比值介于1.8~2.0之間視為良好,可用于后續逆轉錄反應。提取各組細胞的總RNA,經逆轉錄反應得到cDNA作為模板。以磷酸甘油醛脫氫酶(GAPDH)作為內參,應用Primer軟件設計引物序列(表2)。通過實時定量PCR法比較各組細胞中靶基因的相對表達量。根據擴增曲線,輸出循環閾值(CT),依照公式2‐ΔΔCT法進行數據分析。
1.3 統計學處理
采用SPSS 22.0軟件進行統計分析,計量數據用均數±標準差(
 )表示。因患者間存在個體差異,采用CRT恢復率對兩組患者治療后CRT的變化進行統計分析。CRT恢復率=(治療前CRT-治療后CRT)/治療前CRT。兩組患者治療后CRT恢復率比較采用 t 檢驗。體外細胞實驗的組間比較采用單因素方差分析。P≤0.05為差異有統計學意義。
)表示。因患者間存在個體差異,采用CRT恢復率對兩組患者治療后CRT的變化進行統計分析。CRT恢復率=(治療前CRT-治療后CRT)/治療前CRT。兩組患者治療后CRT恢復率比較采用 t 檢驗。體外細胞實驗的組間比較采用單因素方差分析。P≤0.05為差異有統計學意義。
2 結果
治療后1個月,單純治療組、聯合治療組患眼CRT均較治療前明顯下降;但兩組間CRT恢復率比較,差異無統計學意義(t=?0.669,P>0.05)。治療后3個月,聯合治療組患者CRT恢復率明顯優于單純治療組,差異有統計學意義(t=?2.462,P<0.05)(表3)。
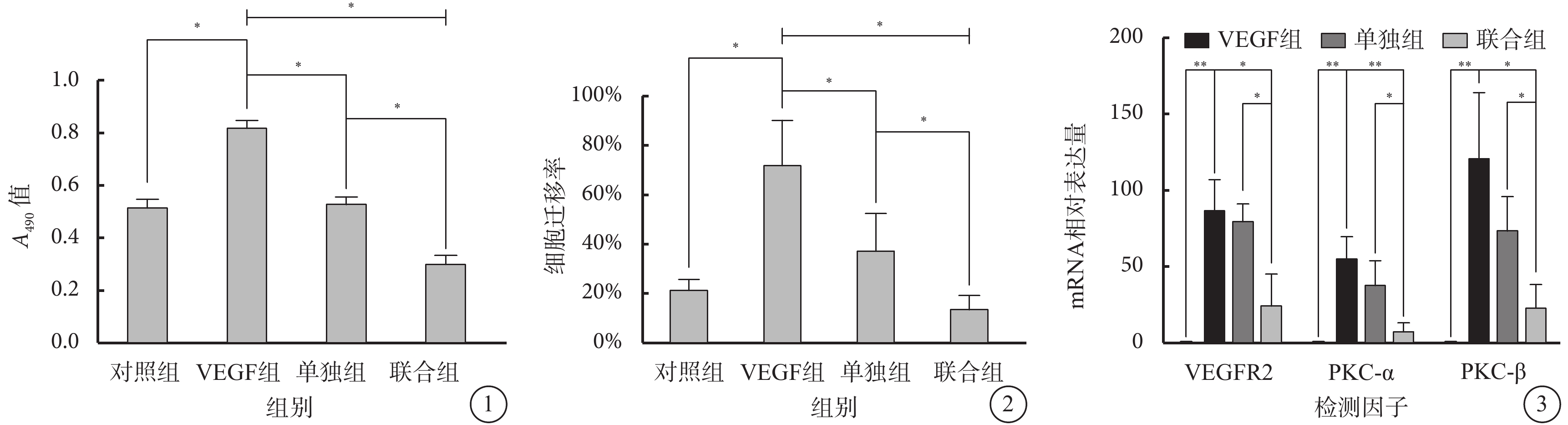
細胞生存力實驗結果顯示,4組間細胞A490值比較,差異有統計學意義(F=202.2,P<0.000)。組間兩兩比較,VEGF組細胞A490值較對照組明顯升高,單獨組、聯合組細胞A490值較VEGF組明顯降低,聯合組細胞A490值較單獨組進一步降低,差異均有統計學意義(P<0.000)(圖1)。
細胞劃痕實驗結果顯示,4組間細胞遷移率比較,差異有統計學意義(F=18.60,P<0.05)。組間兩兩比較,VEGF組細胞遷移率較對照組明顯升高(P=0.001),單獨組、聯合組細胞遷移率較VEGF組明顯降低(P=0.042、0.001),聯合組細胞遷移率較單獨組進一步降低(P=0.001 ),差異均有統計學意義(圖2)。
qRT-PCR檢測結果顯示,4組間細胞VEGFR2、PKC-α、PKC-β mRNA表達量比較,差異均有統計學意義(F=20.56、15.15、13.31,P<0.05)。組間兩兩比較,VEGF組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較對照組明顯升高(P=0.002、0.003、0.009),聯合組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較VEGF組、單獨組明顯降低(P=0.022、0.006、0.021、0.017、0.042、0.037),差異均有統計學意義;單獨組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較VEGF組有所降低,但差異無統計學意義(P=0.641、0.229、0.167)(圖3)。
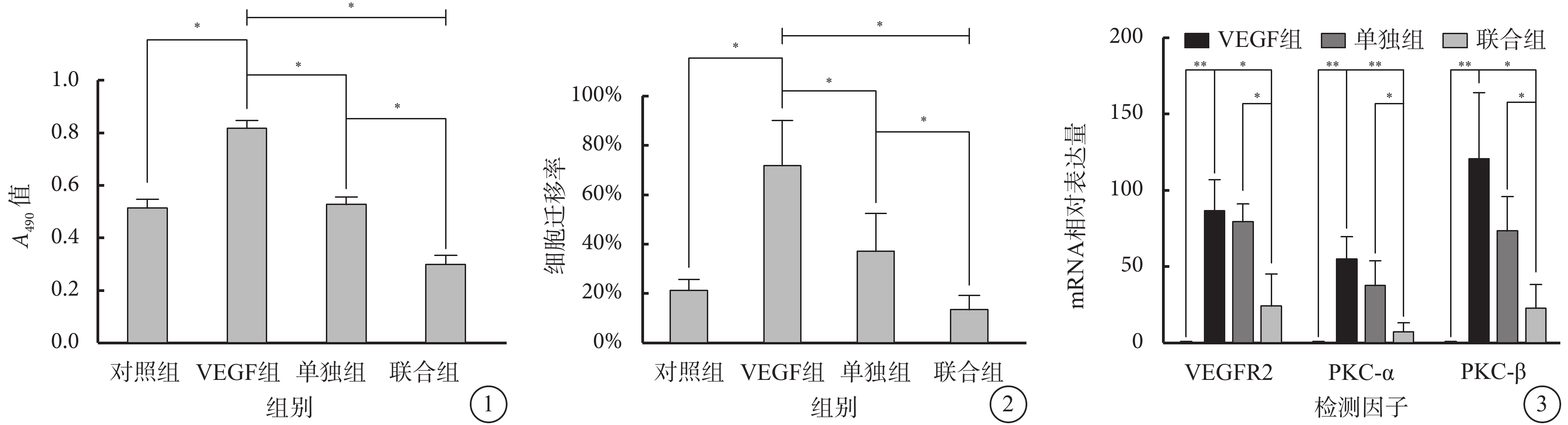 圖1
各組細胞 A490 值比較。*P<0.05 圖 2 各組細胞遷移率比較。*P<0.05 圖 3 各組 VEGFR2、PKC-α、PKC-β mRNA 表達量比較。*P<0.05;**P<0.01
圖1
各組細胞 A490 值比較。*P<0.05 圖 2 各組細胞遷移率比較。*P<0.05 圖 3 各組 VEGFR2、PKC-α、PKC-β mRNA 表達量比較。*P<0.05;**P<0.01
3 討論
近年來的研究結果顯示,二甲雙胍的作用不止單單降低血糖,而是有著更為廣泛的生物學作用,包括通過激活腺苷酸活化蛋白激酶來減弱內毒素誘導的急性心肌炎的發生以及抑制糖基化終產物(AGEs)誘導的炎癥反應[5, 6]。Lee等[7]在一項前瞻性研究中發現,服用二甲雙胍的2型糖尿病患者其患結直腸癌、肝癌及胰腺癌等惡性腫瘤的風險降低。Bowler等[8]通過一項大型回顧性研究發現,服用二甲雙胍的2型糖尿病患者惡性腫瘤死亡率低于使用磺脲類及胰島素降糖者。除此之外,二甲雙胍在眼科疾病中的治療作用也引人關注。有研究將DR患者分為單獨治療組(單純激光光凝治療)和聯合治療組(激光光凝聯合二甲雙胍治療),結果顯示聯合治療組患者生活質量提高更為顯著,視力提高者明顯多于單獨治療組[9]。另有研究發現,在氧誘導視網膜病變模型中,二甲雙胍可以極大降低VEGFR2的水平;同時,體外實驗也證實二甲雙胍可以顯著降低VEGF-A的水平[7, 10]。上述研究結果均提示二甲雙胍對全身性疾病或眼部疾病均有著潛在的抑制作用。從本研究臨床回顧性資料來看,接受玻璃體腔注射康柏西普的患者,其CRT在注射后1、3個月均有下降;而同時服用二甲雙胍的患者治療后3個月CRT恢復率較未服用二甲雙胍者明顯升高,結合康柏西普的藥理作用,我們考慮治療后3個月,二甲雙胍可能作用于下游其他靶點,對康柏西普的治療效果起到延續作用。因此,我們繼續在體外細胞實驗中探索二甲雙胍可能協同抗VEGF的具體機制。
鑒于VEGF在DR進程及新生血管形成中的重要作用[11, 12],本研究選擇VEGF誘導血管內皮細胞以模擬DR患者的眼部微環境特征。我們首先利用細胞生存力實驗、劃痕實驗來觀察聯合應用二甲雙胍對細胞增生、遷移等生物學特征的影響。實驗結果顯示,聯合組可以顯著抑制VEGF誘導的血管內皮細胞增生及遷移,且其效果優于單獨組。考慮糖尿病帶來的一系列并發癥與高血糖狀態激活PKC有關,二甲雙胍可以通過抑制PKC-煙酰胺腺嘌呤二核苷酸磷酸氧化酶途徑來減弱高糖誘導的氧化應激反應,并可抑制高糖誘導的內皮細胞PKC-β2轉位;同時,VEGFR系統的激活后亦伴隨PKC活化[13-17]。所以,本研究以VEGFR2表達及PKC活化程度的改變為切入點進一步探討二甲雙胍發揮協同作用的潛在分子機制。實驗結果顯示,與VEGF組比較,單獨組和聯合組均可下調VEGFR2、PKC-α、PKC-β的mRNA表達水平,但聯合組較單獨組下降更明顯。因此我們推測,一定程度上,二甲雙胍可能通過抑制VEGFR及PKC表達的作用,發揮與抗VEGF藥物的協同作用。
本研究首次證明聯合應用二甲雙胍與抗VEGF藥物可以抑制VEGF所誘導的視網膜血管內皮細胞增生及遷移,抑制VEGFR2、PKC-α、PKC-β的表達。為了全面而深入的探討二甲雙胍協同抗VEGF藥物的作用機制,日后我們還將納入更多的細胞模型,包括高糖誘導視網膜血管內皮細胞,抑或AGEs誘導視網膜血管內皮細胞等,以期能夠通過多種方式模擬DR患者的眼部微環境,進而幫助我們多角度并全方位的了解二甲雙胍在DR中的生物學作用。
抗血管內皮生長因子(VEGF)藥物治療糖尿病黃斑水腫(DME)有較好療效,但部分患者可能呈現反復發作、經久不愈的狀態[1]。二甲雙胍作為應用最廣泛的口服降糖藥之一,主要通過促進葡萄糖在脂肪組織的攝取,同時降低腸道吸收葡萄糖等來發揮降糖作用[2]。我們在臨床工作中發現,服用二甲雙胍的糖尿病視網膜病變(DR)患者對抗VEGF藥物治療的反應明顯優于未服用二甲雙胍者。據此我們推測二甲雙胍可能具有協同抗VEGF藥物治療的作用。為此,我們將二甲雙胍與抗VEGF藥物聯合應用于VEGF誘導的視網膜血管內皮細胞中,旨在從體外細胞實驗的角度探討二甲雙胍聯合抗VEGF藥物治療DR的可能協同作用。現將結果報道如下。
1 對象和方法
1.1 臨床資料回顧
2016年10~12月在我院行玻璃體腔注射抗VEGF藥物治療的DME患者10例12只眼納入本研究。所有患者均符合DR及DME的診斷標準[3, 4]。排除標準:(1)屈光度>?8.0 D以上;(2)眼壓>25 mmHg(1 mmHg=0.133 kPa);(3)有老年性黃斑變性、青光眼、角膜炎、結膜炎、葡萄膜炎等影響視力的其他眼病;(4)經光相干斷層掃描檢查證實存在黃斑前膜、玻璃體黃斑牽拉以及視網膜色素上皮萎縮、視網膜下纖維化或瘢痕等結構性損害;(5)前3個月內接受過眼內抗VEGF藥物治療;(6)前3個月內接受過眼內或眼周和全身系統性皮質類固醇激素治療;(7)眼部曾行玻璃體切割手術或鞏膜扣帶手術,白內障手術、Nd:YAG激光光凝治療時間短于3個月;(8)存在控制較差的糖尿病、高血壓以及心肌梗死、腦血管意外、腎衰竭等全身情況較差,研究者評估不能完成試驗者;(9)服用二甲雙胍時間短于1個月。
患者中,男性4例5只眼,女性6例7只眼。年齡50~76歲,平均年齡(62.9±7.7)歲。病程6~36個月,平均病程(16.4±6.1)個月。將患者隨機分為單純治療組(單純康柏西普治療)和聯合治療組(康柏西普+二甲雙胍)。治療前,兩組患者年齡、病程、視力、黃斑區中心凹視網膜厚度(CRT)比較,差異無統計學意義(P>0.05)(表1)。治療后隨訪3個月,對比分析兩組患者治療后的視力、CRT變化。
1.2 體外細胞實驗
恒河猴視網膜血管內皮細胞(RF-6A,天津醫科大學眼科研究所);磷酸鹽緩沖液(PBS)、RPMI1640培養液(上海源培生物科技股份有限公司);胰蛋白酶、胎牛血清、青鏈霉素、谷氨酰胺(美國Gibco公司);噻唑藍(MTT)試劑盒(北京索萊寶科技有限公司);6、96孔板(美國Life technologies公司);康柏西普(成都康弘藥業集團股份有限公司);二甲雙胍(美國Sigma公司);Trizol試劑盒(美國Invitrogen公司)。
實驗分為對照組(正常細胞)、VEGF組(50 ng/ml的VEGF)、單獨組(50 ng/ml的VEGF+2.5 μg/ml的康柏西普)、聯合組(50 ng/ml的VEGF+2.5 μg/ml的康柏西普+2.0 mmol/L的二甲雙胍)進行。采用含4.5 ml胎牛血清、0.45 ml雙抗、0.45 ml谷氨酰胺的RPMI1640培養液培養細胞,置于37 ℃、5%CO2培養箱中培養,3~5 d傳代1次,取對數生長期細胞用于實驗。將細胞培養24 h后,饑餓過夜,按實驗分組給予干預刺激72 h。
細胞生存力實驗。以細胞密度1×104個/孔接種于96孔板,24 h后更換為無血清培養基,饑餓過夜后按實驗分組予以干預刺激。每組3個復孔,實驗重復3次。培養72 h后棄培養基,加入90 μl新鮮培養液,再加入10 μl MTT溶液,繼續培養4 h后棄上清液,再加入100 μl二甲基亞砜充分震蕩混勻后,酶標儀490 nm處檢測各組吸光度[A,舊稱光密度(OD)]值。
細胞劃痕實驗。以細胞密度6×105個/孔接種于6孔板,每孔最終體系為2 ml,待生長融合為單層細胞后,用100~1000 μl微量加樣槍頭于每孔中央行“十”字形劃痕,PBS沖洗后拍照。按實驗分組予干預刺激,常規培養24 h后于相同位置再次拍照,觀察各孔細胞向裸區遷移情況,用cellSens Standard軟件測量裸區面積。實驗重復3次,按以下公式計算遷移率。遷移率=(S0-St)/S0×100%(S0:原始裸區面積,St:各時間點裸區面積)。
采用半定量實時逆轉錄(qRT)-聚合酶鏈反應(PCR)檢測各組細胞VEGF受體(VEGFR)2、蛋白激酶C(PKC)-α及PKC-β的mRNA表達。依據實驗分組準備細胞,行總RNA提取,超微量分光光度計檢測其濃度。將A260/A280比值介于1.8~2.0之間視為良好,可用于后續逆轉錄反應。提取各組細胞的總RNA,經逆轉錄反應得到cDNA作為模板。以磷酸甘油醛脫氫酶(GAPDH)作為內參,應用Primer軟件設計引物序列(表2)。通過實時定量PCR法比較各組細胞中靶基因的相對表達量。根據擴增曲線,輸出循環閾值(CT),依照公式2‐ΔΔCT法進行數據分析。
1.3 統計學處理
采用SPSS 22.0軟件進行統計分析,計量數據用均數±標準差(
 )表示。因患者間存在個體差異,采用CRT恢復率對兩組患者治療后CRT的變化進行統計分析。CRT恢復率=(治療前CRT-治療后CRT)/治療前CRT。兩組患者治療后CRT恢復率比較采用 t 檢驗。體外細胞實驗的組間比較采用單因素方差分析。P≤0.05為差異有統計學意義。
)表示。因患者間存在個體差異,采用CRT恢復率對兩組患者治療后CRT的變化進行統計分析。CRT恢復率=(治療前CRT-治療后CRT)/治療前CRT。兩組患者治療后CRT恢復率比較采用 t 檢驗。體外細胞實驗的組間比較采用單因素方差分析。P≤0.05為差異有統計學意義。
2 結果
治療后1個月,單純治療組、聯合治療組患眼CRT均較治療前明顯下降;但兩組間CRT恢復率比較,差異無統計學意義(t=?0.669,P>0.05)。治療后3個月,聯合治療組患者CRT恢復率明顯優于單純治療組,差異有統計學意義(t=?2.462,P<0.05)(表3)。
細胞生存力實驗結果顯示,4組間細胞A490值比較,差異有統計學意義(F=202.2,P<0.000)。組間兩兩比較,VEGF組細胞A490值較對照組明顯升高,單獨組、聯合組細胞A490值較VEGF組明顯降低,聯合組細胞A490值較單獨組進一步降低,差異均有統計學意義(P<0.000)(圖1)。
細胞劃痕實驗結果顯示,4組間細胞遷移率比較,差異有統計學意義(F=18.60,P<0.05)。組間兩兩比較,VEGF組細胞遷移率較對照組明顯升高(P=0.001),單獨組、聯合組細胞遷移率較VEGF組明顯降低(P=0.042、0.001),聯合組細胞遷移率較單獨組進一步降低(P=0.001 ),差異均有統計學意義(圖2)。
qRT-PCR檢測結果顯示,4組間細胞VEGFR2、PKC-α、PKC-β mRNA表達量比較,差異均有統計學意義(F=20.56、15.15、13.31,P<0.05)。組間兩兩比較,VEGF組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較對照組明顯升高(P=0.002、0.003、0.009),聯合組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較VEGF組、單獨組明顯降低(P=0.022、0.006、0.021、0.017、0.042、0.037),差異均有統計學意義;單獨組細胞VEGFR2、PKC-α、PKC-β mRNA表達量較VEGF組有所降低,但差異無統計學意義(P=0.641、0.229、0.167)(圖3)。
 圖1
各組細胞 A490 值比較。*P<0.05 圖 2 各組細胞遷移率比較。*P<0.05 圖 3 各組 VEGFR2、PKC-α、PKC-β mRNA 表達量比較。*P<0.05;**P<0.01
圖1
各組細胞 A490 值比較。*P<0.05 圖 2 各組細胞遷移率比較。*P<0.05 圖 3 各組 VEGFR2、PKC-α、PKC-β mRNA 表達量比較。*P<0.05;**P<0.01
3 討論
近年來的研究結果顯示,二甲雙胍的作用不止單單降低血糖,而是有著更為廣泛的生物學作用,包括通過激活腺苷酸活化蛋白激酶來減弱內毒素誘導的急性心肌炎的發生以及抑制糖基化終產物(AGEs)誘導的炎癥反應[5, 6]。Lee等[7]在一項前瞻性研究中發現,服用二甲雙胍的2型糖尿病患者其患結直腸癌、肝癌及胰腺癌等惡性腫瘤的風險降低。Bowler等[8]通過一項大型回顧性研究發現,服用二甲雙胍的2型糖尿病患者惡性腫瘤死亡率低于使用磺脲類及胰島素降糖者。除此之外,二甲雙胍在眼科疾病中的治療作用也引人關注。有研究將DR患者分為單獨治療組(單純激光光凝治療)和聯合治療組(激光光凝聯合二甲雙胍治療),結果顯示聯合治療組患者生活質量提高更為顯著,視力提高者明顯多于單獨治療組[9]。另有研究發現,在氧誘導視網膜病變模型中,二甲雙胍可以極大降低VEGFR2的水平;同時,體外實驗也證實二甲雙胍可以顯著降低VEGF-A的水平[7, 10]。上述研究結果均提示二甲雙胍對全身性疾病或眼部疾病均有著潛在的抑制作用。從本研究臨床回顧性資料來看,接受玻璃體腔注射康柏西普的患者,其CRT在注射后1、3個月均有下降;而同時服用二甲雙胍的患者治療后3個月CRT恢復率較未服用二甲雙胍者明顯升高,結合康柏西普的藥理作用,我們考慮治療后3個月,二甲雙胍可能作用于下游其他靶點,對康柏西普的治療效果起到延續作用。因此,我們繼續在體外細胞實驗中探索二甲雙胍可能協同抗VEGF的具體機制。
鑒于VEGF在DR進程及新生血管形成中的重要作用[11, 12],本研究選擇VEGF誘導血管內皮細胞以模擬DR患者的眼部微環境特征。我們首先利用細胞生存力實驗、劃痕實驗來觀察聯合應用二甲雙胍對細胞增生、遷移等生物學特征的影響。實驗結果顯示,聯合組可以顯著抑制VEGF誘導的血管內皮細胞增生及遷移,且其效果優于單獨組。考慮糖尿病帶來的一系列并發癥與高血糖狀態激活PKC有關,二甲雙胍可以通過抑制PKC-煙酰胺腺嘌呤二核苷酸磷酸氧化酶途徑來減弱高糖誘導的氧化應激反應,并可抑制高糖誘導的內皮細胞PKC-β2轉位;同時,VEGFR系統的激活后亦伴隨PKC活化[13-17]。所以,本研究以VEGFR2表達及PKC活化程度的改變為切入點進一步探討二甲雙胍發揮協同作用的潛在分子機制。實驗結果顯示,與VEGF組比較,單獨組和聯合組均可下調VEGFR2、PKC-α、PKC-β的mRNA表達水平,但聯合組較單獨組下降更明顯。因此我們推測,一定程度上,二甲雙胍可能通過抑制VEGFR及PKC表達的作用,發揮與抗VEGF藥物的協同作用。
本研究首次證明聯合應用二甲雙胍與抗VEGF藥物可以抑制VEGF所誘導的視網膜血管內皮細胞增生及遷移,抑制VEGFR2、PKC-α、PKC-β的表達。為了全面而深入的探討二甲雙胍協同抗VEGF藥物的作用機制,日后我們還將納入更多的細胞模型,包括高糖誘導視網膜血管內皮細胞,抑或AGEs誘導視網膜血管內皮細胞等,以期能夠通過多種方式模擬DR患者的眼部微環境,進而幫助我們多角度并全方位的了解二甲雙胍在DR中的生物學作用。