引用本文: 丁恩亮, 韓曉蕾, 郝玉華. 單眼視網膜色素變性合并對側眼增生型糖尿病視網膜病變一例. 中華眼底病雜志, 2018, 34(4): 394-395. doi: 10.3760/cma.j.issn.1005-1015.2018.04.018 復制
患者女,38歲。因右眼視物不清伴夜盲10余年,左眼視物不清3年并加重20 d于2016年7月來我院就診。既往2型糖尿病6年,口服藥物控制,血糖控制不理想;家族中無類似疾病者。眼部檢查,右眼視力0.25,左眼視力0.04;均不能矯正。雙眼外眼及眼前節檢查未見異常。右眼視盤顏色淡;視網膜色澤灰暗,血管纖細尤以動脈為著,中周部大量骨細胞樣色素沉著,未見出血及滲出,黃斑中心凹反光消失。左眼玻璃體大量積血;眼底模糊可見視盤充血,邊界不清楚,視盤前及上下血管弓大片新生血管膜,顳上牽拉視網膜脫離,黃斑中心凹反光消失不見(圖1)。熒光素眼底血管造影(FFA)檢查,右眼視網膜血管纖細,中周部視網膜可見斑駁狀透見熒光,其間夾雜多量熒光遮蔽;未見出血、滲出及熒光素滲漏;左眼玻璃體積血部分熒光遮蔽,大量新生血管膜,不規則團狀熒光素滲漏,中周部及周邊部大片無灌注區,未見色素遮蔽熒光(圖2)。視網膜電圖(ERG)檢查,雙眼a、b波振幅降低,潛伏期延長(圖3)。右眼視野檢查,管狀視野(圖4)。診斷:右眼視網膜色素變性(RP);左眼增生型糖尿病視網膜病變(PDR Ⅵ期)。
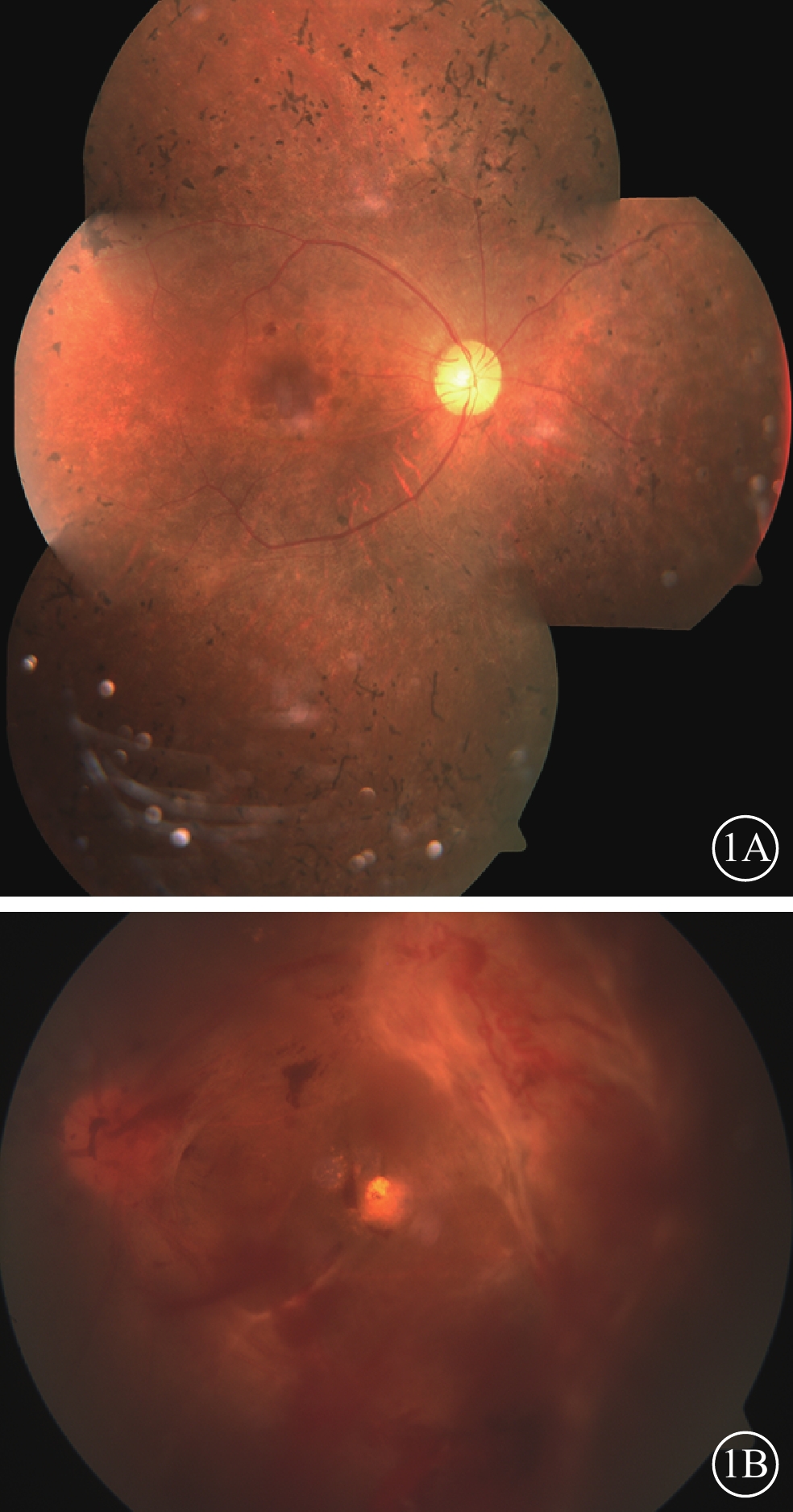 圖1
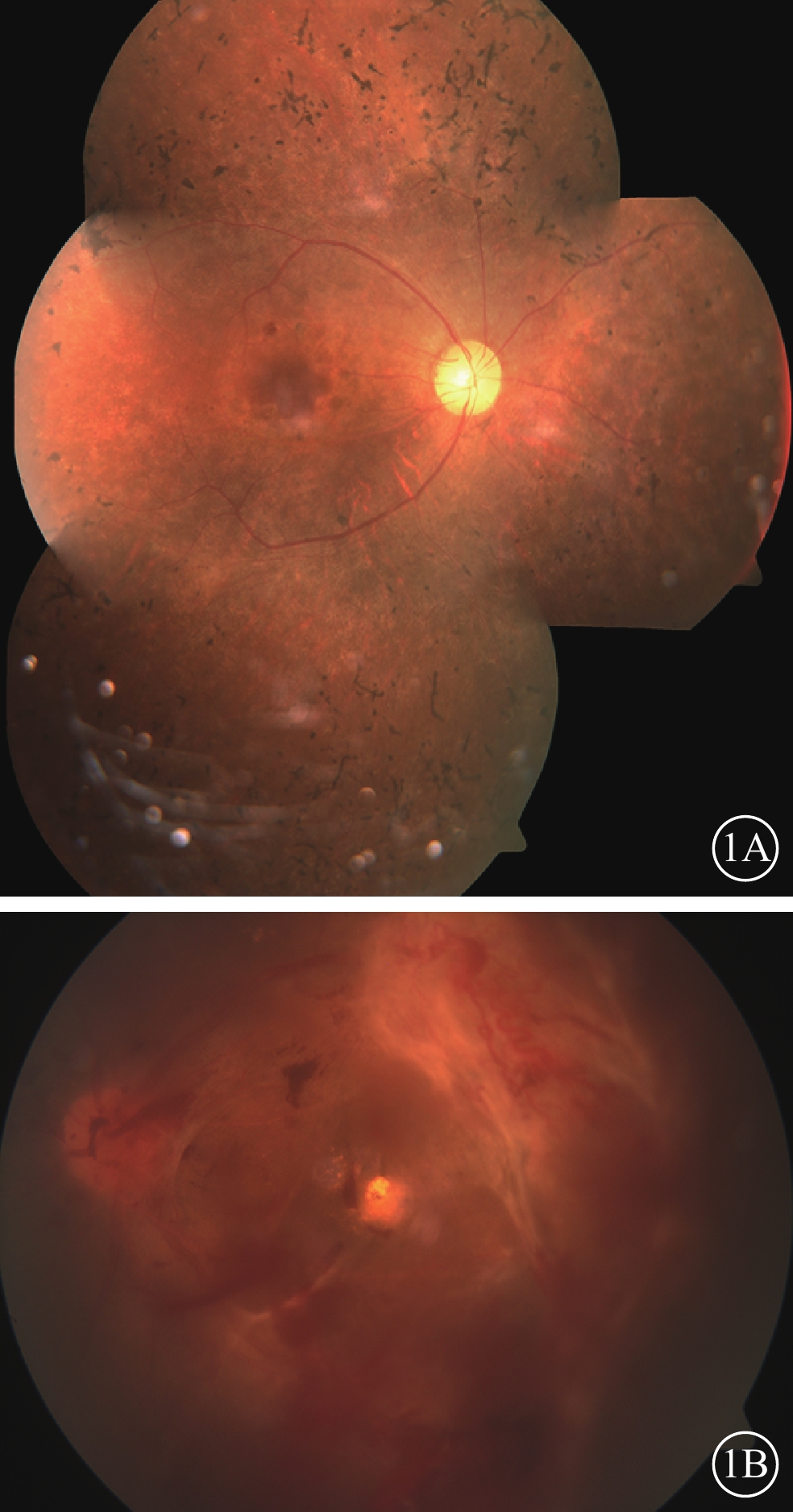
雙眼彩色眼底像 1A.右眼,中周部視網膜大量骨細胞樣色素沉著,未見明顯出血及滲出;1B.左眼,玻璃體積血,視網膜大片新生血管膜
圖1
雙眼彩色眼底像 1A.右眼,中周部視網膜大量骨細胞樣色素沉著,未見明顯出血及滲出;1B.左眼,玻璃體積血,視網膜大片新生血管膜
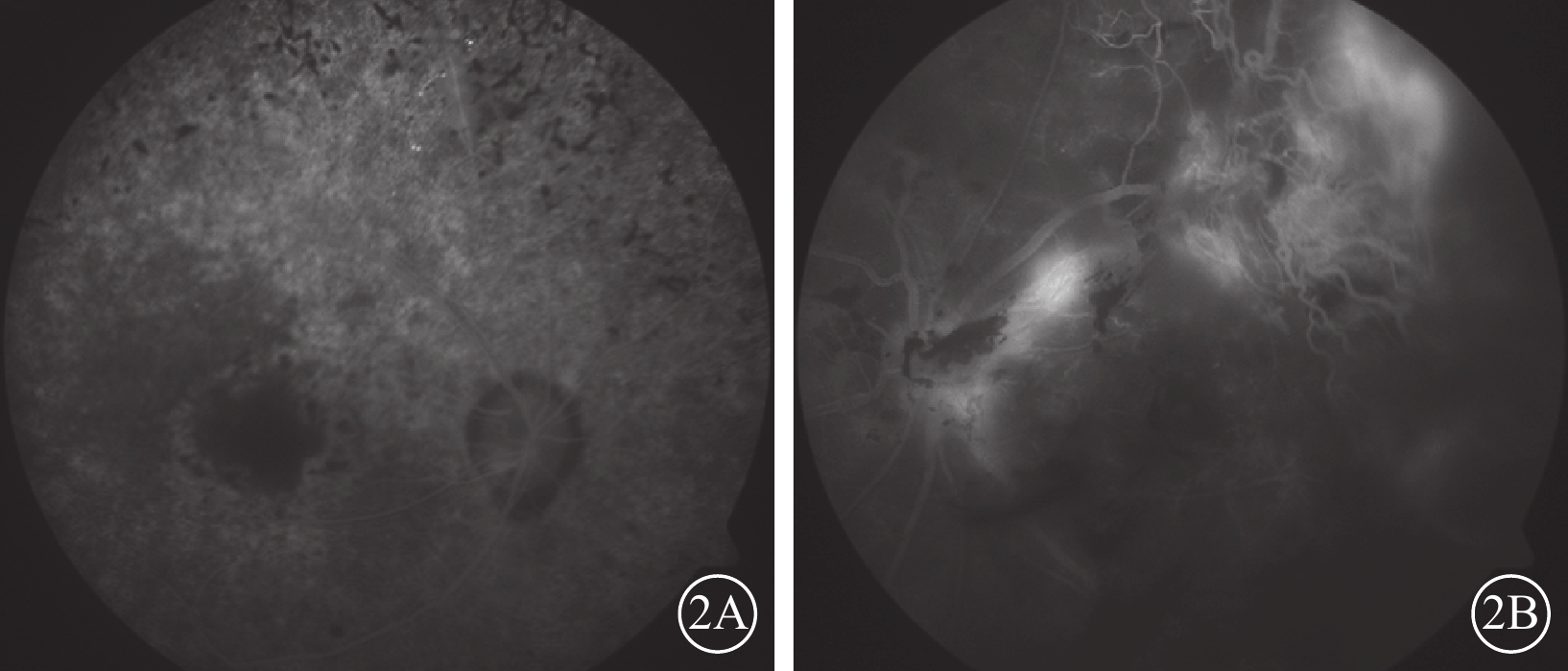 圖2
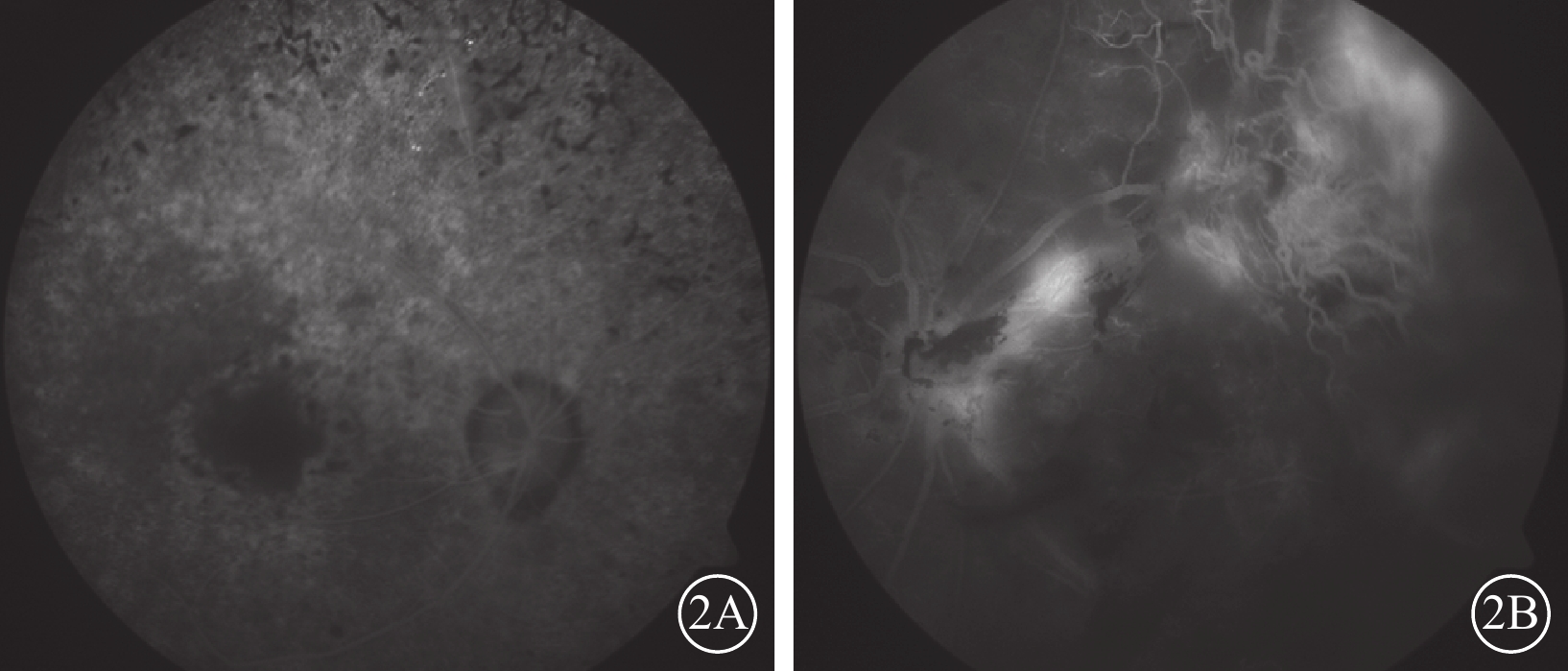
雙眼FFA 像 2A.右眼,中周部視網膜可見斑駁狀透見熒光,期間夾雜多量熒光遮蔽;2B.左眼,視盤旁及顳上血管弓新生血管膜熒光素滲漏
圖2
雙眼FFA 像 2A.右眼,中周部視網膜可見斑駁狀透見熒光,期間夾雜多量熒光遮蔽;2B.左眼,視盤旁及顳上血管弓新生血管膜熒光素滲漏
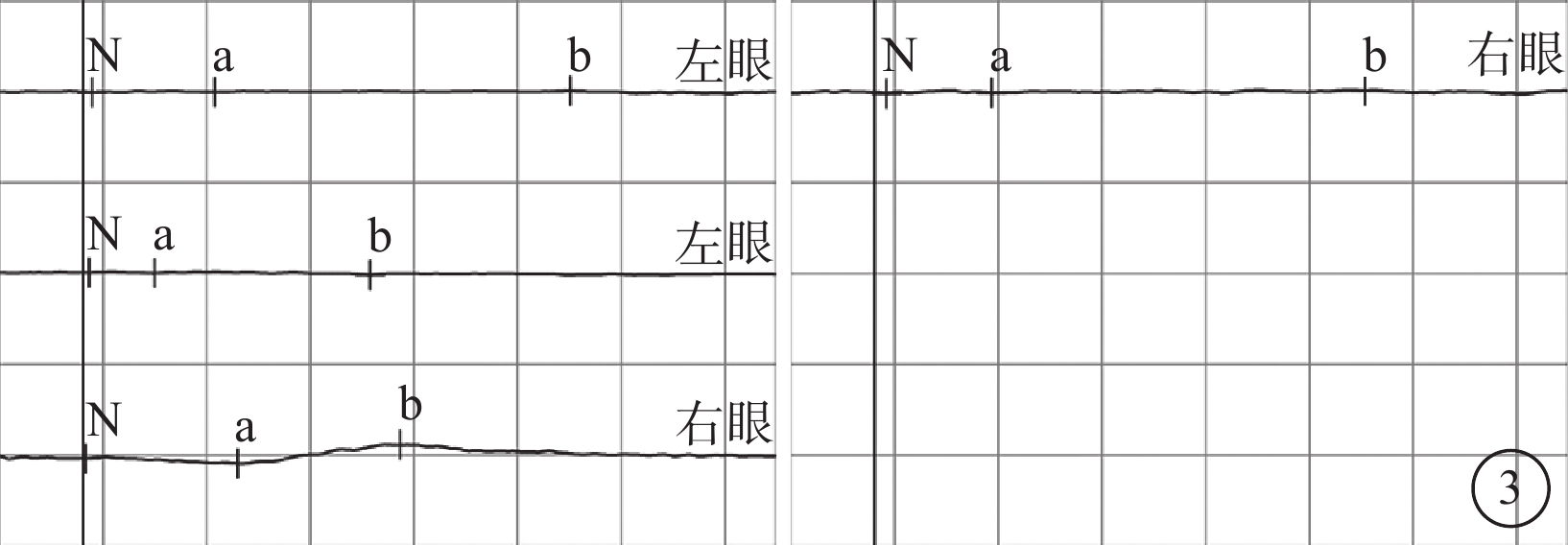 圖3
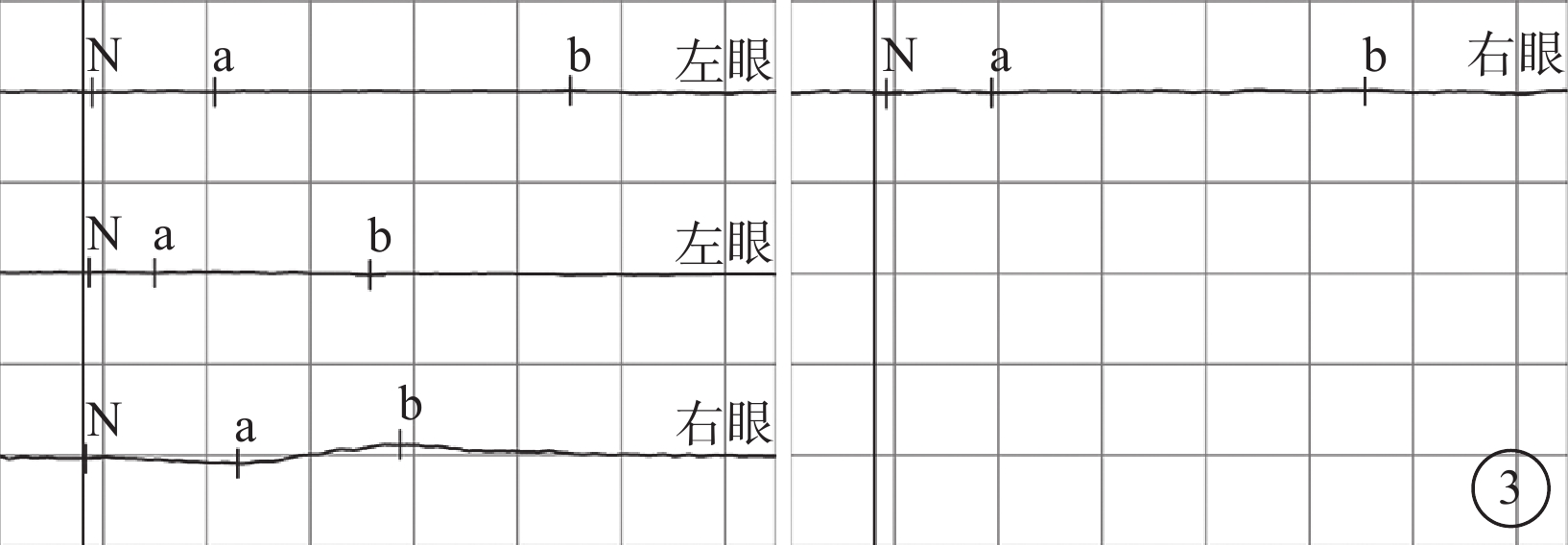
患者手術前雙眼ERG像 a、b波振幅降低,潛伏期延長
圖3
患者手術前雙眼ERG像 a、b波振幅降低,潛伏期延長
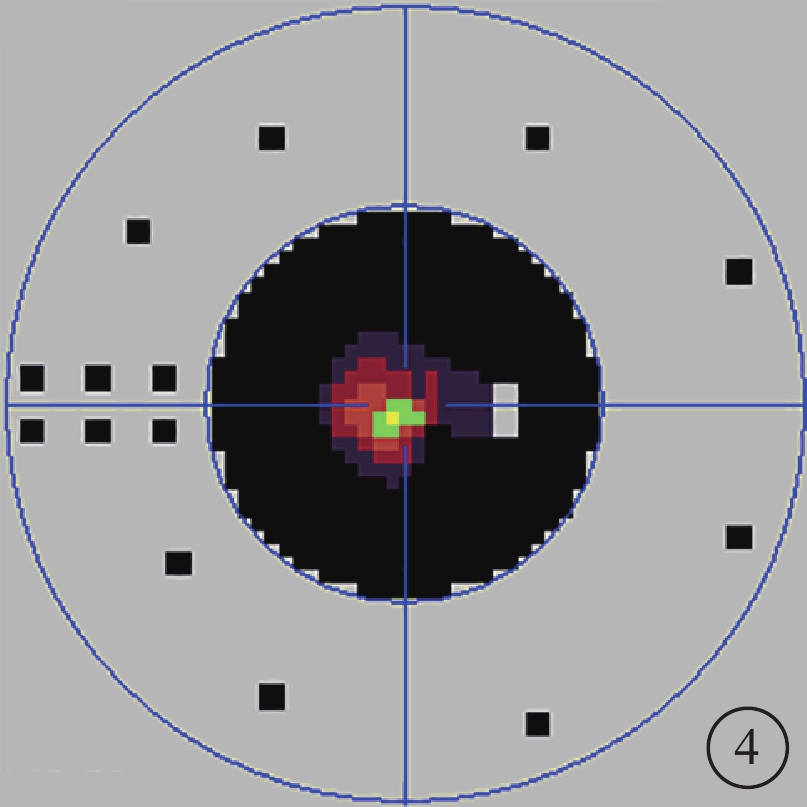 圖4
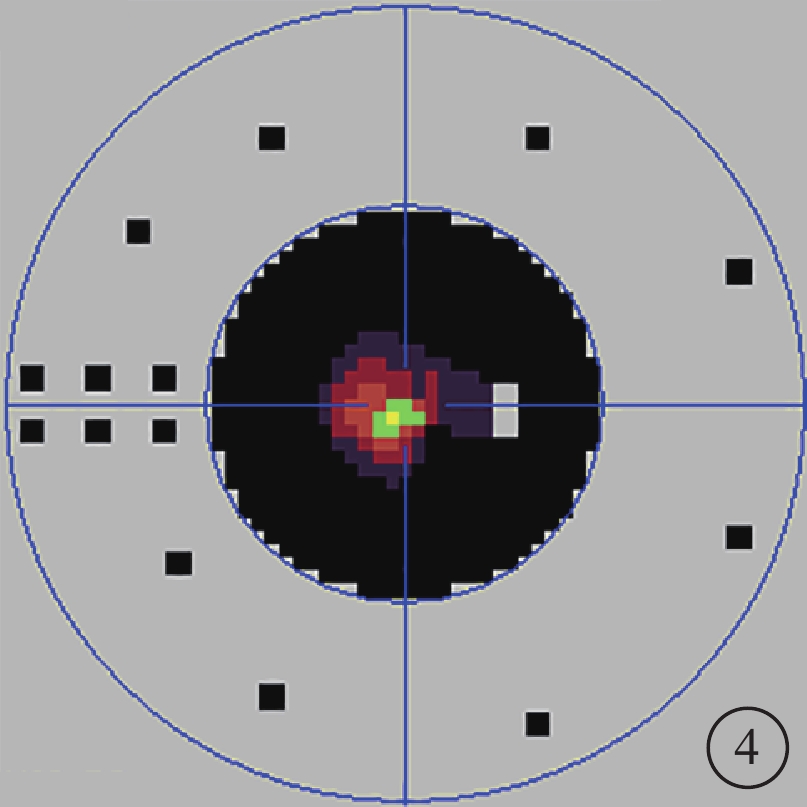
患者右眼視野像。管狀視野
圖4
患者右眼視野像。管狀視野
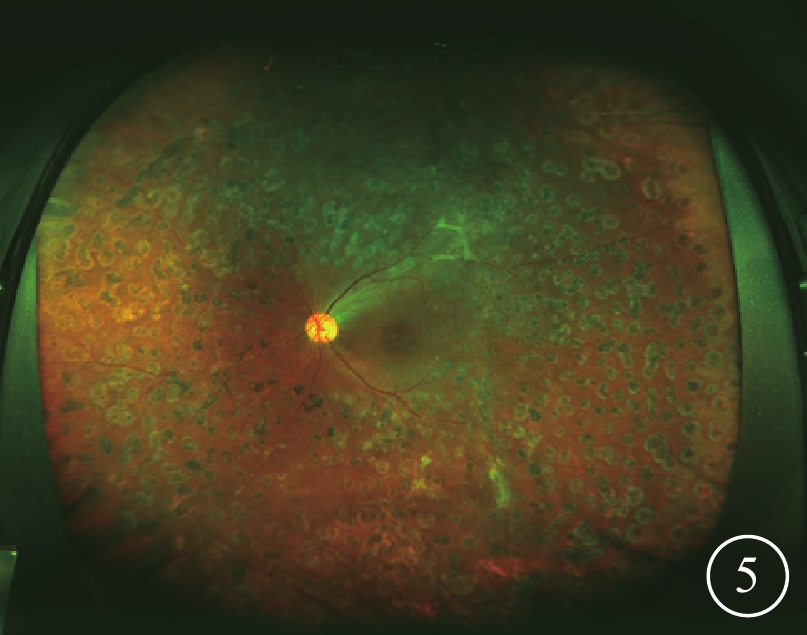
明確診斷后,左眼玻璃體腔注射雷珠單抗促進新生血管消退,5 d后行玻璃體切割手術。手術中對廣泛的新生血管增生膜進行剝膜處理,周邊視網膜行激光光凝治療(參數:150 mW,200 μm,0.2 s,902點)。手術后規律復查;1個月內左眼補充完成全視網膜激光光凝(PRP)。手術后8個月復查,右眼視力0.25,左眼視力0.3。右眼眼底同前。左眼玻璃體腔清晰;視盤邊界清楚,顏色橘紅,杯盤比0.3;視網膜血管走行及比例大致正常,激光光凝斑清晰,未見骨細胞樣色素沉著;黃斑中心凹反光不清(圖5)。
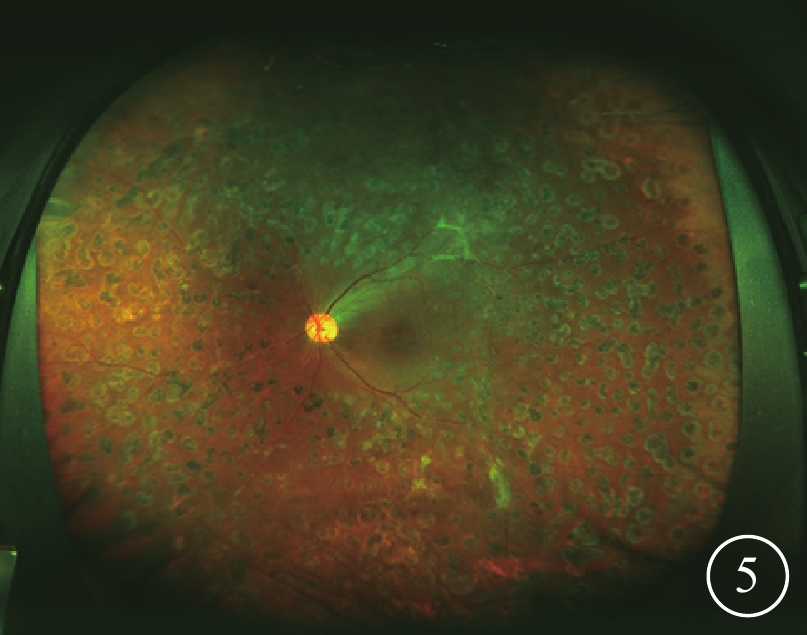 圖5
患者左眼手術后廣角彩色眼底像。視網膜激光光凝斑清晰,未見骨細胞樣色素沉著
圖5
患者左眼手術后廣角彩色眼底像。視網膜激光光凝斑清晰,未見骨細胞樣色素沉著
討論 原發性RP是一組進行性遺傳性營養不良性退行性病變,通常為雙眼發病,極少數患者為單眼發病[1]。而繼發性RP可為單眼發病,通常有長期服藥史(吩噻嗪等)、后天性梅毒和某些急性傳染病(如天花、麻疹、猩紅熱、流行性腮腺炎等)、外傷史等因素導致[2]。本例患者右眼視力逐漸下降伴夜盲10余年,尤其在左眼視力下降后右眼夜盲癥狀更加明顯。詳細詢問患者家族史及既往史發現家族中無RP患者,亦無可導致繼發性RP的因素如外傷、長期服藥史(吩噻嗪等)、后天性梅毒和某些急性傳染病(如天花、麻疹、猩紅熱、流行性腮腺炎等)。根據患者右眼視力逐漸下降、夜盲等癥狀以及眼底特征、視野及ERG結果,我們考慮為單眼原發性RP。
通常情況下糖尿病視網膜病變(DR)也為雙眼同時患病,病變程度可不相等。本例患者左眼PDR合并牽拉性視網膜脫離,而右眼僅見典型RP改變,未見微動脈瘤、滲出及出血。RP對DR的進展是否有抑制作用尚無定論,類似病例較少見。有研究表明,RP和早期非增生型DR(NPDR)血管退行性病變的相互作用,可能會導致在并存RP時NPDR的加重;后期DR,伴發RP會減少需氧量,改善相對缺血狀態,從而減緩PDR的發展[3]。目前國內外零星病例報道,RP患者合并糖尿病者,雖有數年甚至數十年糖尿病史,并已有嚴重糖尿病腎病及糖尿病周圍神經病變但卻未發生DR或僅表現為輕微DR。從某種意義上RP對DR的進展可能有一定的抑制作用,其可能原因分析如下:(1)視網膜光感受器細胞特別是視桿細胞是高耗氧細胞,而RP患者光感受器細胞的凋亡降低了氧的需求量,使視網膜處于相對高氧狀態,從一定程度上延緩了DR發展成為PDR,并導致了視網膜血管萎縮。Padnick-silver等[4]研究也證實了此點。(2)RP患者視網膜色素上皮(RPE)細胞大量破壞導致眼底骨細胞樣色素改變,而RPE可以分泌多種生長因子,其中血管內皮生長因子(VEGF)的重要來源即是RPE細胞。RP患者RPE細胞的破壞減少了VEGF的產生,特別是VEGF-A的產生,導致視網膜血管變細,甚至纖維化改變。由此防止了新生血管產生,阻止DR的發生及發展[5]。(3)Arden[6]認為RP可能在基因、減少糖基化和自由基的生成等方面延緩了DR的進展。(4)我們推斷視網膜光感受器細胞和RPE細胞的廣泛破壞缺失與DR患者接受PRP治療來降低視網膜氧的需求量以達到防止新生血管產生的目的有異曲同工之作用。
既往報道的單側RP病例,其中相當一部分或許并非是真正意義的單側原發性RP,可能是雙眼發病極為不平衡。我們將持續關注本例患者的病情變化及后續治療。RP延緩DR發展的作用可能有多方面的因素,尚有待更多的病例研究及進一步的探討。
患者女,38歲。因右眼視物不清伴夜盲10余年,左眼視物不清3年并加重20 d于2016年7月來我院就診。既往2型糖尿病6年,口服藥物控制,血糖控制不理想;家族中無類似疾病者。眼部檢查,右眼視力0.25,左眼視力0.04;均不能矯正。雙眼外眼及眼前節檢查未見異常。右眼視盤顏色淡;視網膜色澤灰暗,血管纖細尤以動脈為著,中周部大量骨細胞樣色素沉著,未見出血及滲出,黃斑中心凹反光消失。左眼玻璃體大量積血;眼底模糊可見視盤充血,邊界不清楚,視盤前及上下血管弓大片新生血管膜,顳上牽拉視網膜脫離,黃斑中心凹反光消失不見(圖1)。熒光素眼底血管造影(FFA)檢查,右眼視網膜血管纖細,中周部視網膜可見斑駁狀透見熒光,其間夾雜多量熒光遮蔽;未見出血、滲出及熒光素滲漏;左眼玻璃體積血部分熒光遮蔽,大量新生血管膜,不規則團狀熒光素滲漏,中周部及周邊部大片無灌注區,未見色素遮蔽熒光(圖2)。視網膜電圖(ERG)檢查,雙眼a、b波振幅降低,潛伏期延長(圖3)。右眼視野檢查,管狀視野(圖4)。診斷:右眼視網膜色素變性(RP);左眼增生型糖尿病視網膜病變(PDR Ⅵ期)。
 圖1
雙眼彩色眼底像 1A.右眼,中周部視網膜大量骨細胞樣色素沉著,未見明顯出血及滲出;1B.左眼,玻璃體積血,視網膜大片新生血管膜
圖1
雙眼彩色眼底像 1A.右眼,中周部視網膜大量骨細胞樣色素沉著,未見明顯出血及滲出;1B.左眼,玻璃體積血,視網膜大片新生血管膜
 圖2
雙眼FFA 像 2A.右眼,中周部視網膜可見斑駁狀透見熒光,期間夾雜多量熒光遮蔽;2B.左眼,視盤旁及顳上血管弓新生血管膜熒光素滲漏
圖2
雙眼FFA 像 2A.右眼,中周部視網膜可見斑駁狀透見熒光,期間夾雜多量熒光遮蔽;2B.左眼,視盤旁及顳上血管弓新生血管膜熒光素滲漏
 圖3
患者手術前雙眼ERG像 a、b波振幅降低,潛伏期延長
圖3
患者手術前雙眼ERG像 a、b波振幅降低,潛伏期延長
 圖4
患者右眼視野像。管狀視野
圖4
患者右眼視野像。管狀視野
明確診斷后,左眼玻璃體腔注射雷珠單抗促進新生血管消退,5 d后行玻璃體切割手術。手術中對廣泛的新生血管增生膜進行剝膜處理,周邊視網膜行激光光凝治療(參數:150 mW,200 μm,0.2 s,902點)。手術后規律復查;1個月內左眼補充完成全視網膜激光光凝(PRP)。手術后8個月復查,右眼視力0.25,左眼視力0.3。右眼眼底同前。左眼玻璃體腔清晰;視盤邊界清楚,顏色橘紅,杯盤比0.3;視網膜血管走行及比例大致正常,激光光凝斑清晰,未見骨細胞樣色素沉著;黃斑中心凹反光不清(圖5)。
 圖5
患者左眼手術后廣角彩色眼底像。視網膜激光光凝斑清晰,未見骨細胞樣色素沉著
圖5
患者左眼手術后廣角彩色眼底像。視網膜激光光凝斑清晰,未見骨細胞樣色素沉著
討論 原發性RP是一組進行性遺傳性營養不良性退行性病變,通常為雙眼發病,極少數患者為單眼發病[1]。而繼發性RP可為單眼發病,通常有長期服藥史(吩噻嗪等)、后天性梅毒和某些急性傳染病(如天花、麻疹、猩紅熱、流行性腮腺炎等)、外傷史等因素導致[2]。本例患者右眼視力逐漸下降伴夜盲10余年,尤其在左眼視力下降后右眼夜盲癥狀更加明顯。詳細詢問患者家族史及既往史發現家族中無RP患者,亦無可導致繼發性RP的因素如外傷、長期服藥史(吩噻嗪等)、后天性梅毒和某些急性傳染病(如天花、麻疹、猩紅熱、流行性腮腺炎等)。根據患者右眼視力逐漸下降、夜盲等癥狀以及眼底特征、視野及ERG結果,我們考慮為單眼原發性RP。
通常情況下糖尿病視網膜病變(DR)也為雙眼同時患病,病變程度可不相等。本例患者左眼PDR合并牽拉性視網膜脫離,而右眼僅見典型RP改變,未見微動脈瘤、滲出及出血。RP對DR的進展是否有抑制作用尚無定論,類似病例較少見。有研究表明,RP和早期非增生型DR(NPDR)血管退行性病變的相互作用,可能會導致在并存RP時NPDR的加重;后期DR,伴發RP會減少需氧量,改善相對缺血狀態,從而減緩PDR的發展[3]。目前國內外零星病例報道,RP患者合并糖尿病者,雖有數年甚至數十年糖尿病史,并已有嚴重糖尿病腎病及糖尿病周圍神經病變但卻未發生DR或僅表現為輕微DR。從某種意義上RP對DR的進展可能有一定的抑制作用,其可能原因分析如下:(1)視網膜光感受器細胞特別是視桿細胞是高耗氧細胞,而RP患者光感受器細胞的凋亡降低了氧的需求量,使視網膜處于相對高氧狀態,從一定程度上延緩了DR發展成為PDR,并導致了視網膜血管萎縮。Padnick-silver等[4]研究也證實了此點。(2)RP患者視網膜色素上皮(RPE)細胞大量破壞導致眼底骨細胞樣色素改變,而RPE可以分泌多種生長因子,其中血管內皮生長因子(VEGF)的重要來源即是RPE細胞。RP患者RPE細胞的破壞減少了VEGF的產生,特別是VEGF-A的產生,導致視網膜血管變細,甚至纖維化改變。由此防止了新生血管產生,阻止DR的發生及發展[5]。(3)Arden[6]認為RP可能在基因、減少糖基化和自由基的生成等方面延緩了DR的進展。(4)我們推斷視網膜光感受器細胞和RPE細胞的廣泛破壞缺失與DR患者接受PRP治療來降低視網膜氧的需求量以達到防止新生血管產生的目的有異曲同工之作用。
既往報道的單側RP病例,其中相當一部分或許并非是真正意義的單側原發性RP,可能是雙眼發病極為不平衡。我們將持續關注本例患者的病情變化及后續治療。RP延緩DR發展的作用可能有多方面的因素,尚有待更多的病例研究及進一步的探討。