引用本文: 郝琳琳, 肖輝, 陳翔熙, 米蘭, 廖玲玲, 劉杏. 原發性開角型青光眼與原發性慢性閉角型青光眼活體篩板厚度和篩板前表面深度的比較. 中華眼底病雜志, 2016, 32(6): 619-623. doi: 10.3760/cma.j.issn.1005-1015.2016.06.013 復制
篩板是青光眼視神經損害的原發部位,由于其深埋于視盤之下不易直接觀察,既往研究僅局限于動物實驗或人尸體眼篩板的病理組織學觀察[1, 2]。隨著頻域光相干斷層掃描(OCT)增強深部成像技術(EDI)(EDI-OCT)的應用,已觀察到活體篩板的形態變化[3, 4]。目前國外相關研究多集中于開角型青光眼篩板形態觀察,發現篩板出現明顯后凸變薄且篩板的結構缺損與視野進展相關[5-9]。說明篩板因素在青光眼發生發展中有重要作用。原發性開角型青光眼(POAG)和原發性慢性閉角型青光眼(CPACG)病程以及視神經和視野損害均相似,但兩者有關結構改變和視功能的損害相關性是否存在差異,目前仍不明確。因此,我們應用EDI-OCT對一組POAG和CPACG患者的篩板進行了觀察測量,并與正常對照者相應部位的篩板進行了比較。現將結果報道如下。
1 對象和方法
2015年4~12月在中山眼科中心門診確診的POAG患者73例73只眼(POAG組)、CPACG患者64例64只眼(CPACG組)以及正常人40名40只眼(正常對照組)納入研究。所有受檢者均獲知情同意并簽署相應文件。
所有受檢者均行最佳矯正視力、眼壓、裂隙燈顯微鏡、前房角鏡、90D前置鏡、屈光度、頻域OCT檢查和眼軸長度(AL)測定。眼壓檢查為Goldmann壓平眼壓計;屈光度檢查為電腦驗光儀RM-100型(日本Topcon公司);AL測定為A型超聲波儀US-1800型(日本Nidek公司);視野檢查為Humphrey自動視野計750i型(德國Zeiss公司)。
POAG組納入標準:(1) Goldmann壓平眼壓計測量眼壓 > 21 mmHg (1 mmHg=0.133 kPa);(2)具有青光眼視盤改變和視網膜神經纖維層(RNFL)缺損;(3)具有青光眼性視野缺損;(4)前房角為開角。CPACG組納入標準:(1)具有淺前房、窄房角的眼部解剖特征;(2)有反復眼壓輕度或中度升高的癥狀或無癥狀;(3)房角鏡檢查可見房角狹窄或房角粘連,Goldmann壓平眼壓計測量眼壓 > 21 mmHg;(4)進展期至晚期可見類似POAG的視盤及視野損害;(5)眼前節不存在急性高眼壓造成的缺血性損害特征。正常對照組納入標準:(1)裸眼或矯正視力≥1.0,屈光度球鏡-6.00~+2.00 D,柱鏡-1.00~+ 1.00 D;(2)視盤杯盤比(C/D)≤0.6,雙眼C/D差值≤0.2,眼底檢查未見異常;(3) Goldmann壓平眼壓計測量眼壓 < 21 mmHg;(4) Humphrey自動視野計視野檢查正常,頻域OCT檢查RNFL厚度正常。排除標準:(1)繼發性青光眼;(2)屈光度球鏡>+2.00 D或 < -6.00 D,或柱鏡>+1.00 D或 < -1.00 D;(3)既往有眼部手術史;(4)眼內存在炎癥反應;(5)合并其他視網膜、脈絡膜或視神經疾病,嚴重屈光間質混濁、明顯全身疾病、顱內疾病、或其他可能影響頻域OCT檢查的神經和精神疾病;(6)相關檢查配合不佳者或圖像成像不佳者。POAG組73例73只眼中,男性39例39只眼,女性34例34只眼;平均年齡(59.68±12.07)歲。CPACG組64例64只眼中,男性25例25只眼,女性39例39只眼;平均年齡(58.69±9.33)歲。正常對照組40名40只眼中,男性15名15只眼,女性25名25只眼;平均年齡(60.53±10.36)歲。3組受檢者之間性別構成比(χ2=2.07)、平均年齡(F=0.38)比較,差異均無統計學意義(P > 0.05)。3組受檢眼頻域OCT測量時眼壓、AL、RNFL厚度值及平均視野缺損(MD)值比較,差異均有統計學意義(F=15.67、21.15、44.40、27.99,P < 0.05)(圖 1)。3組受檢眼之間兩兩比較,POAG組受檢眼與CPACG組受檢眼平均眼壓、RNFL厚度值、MD值差異無統計學意義(t=1.07、3.69、1.67,P > 0.05),AL差異有統計學意義(t=0.16,P < 0.01);POAG組受檢眼與正常對照組受檢眼AL差異無統計學意義(t=0.18,P > 0.05);CPACG組受檢眼與正常對照組受檢眼AL差異有統計學意義(t=0.17,P < 0.01);POAG組、CPACG組受檢眼與正常對照組受檢眼平均眼壓、RNFL厚度值、MD值差異均有統計學意義(t=1.25、4.25、1.91、1.26、4.34、1.92,P < 0.01) (圖 1)。
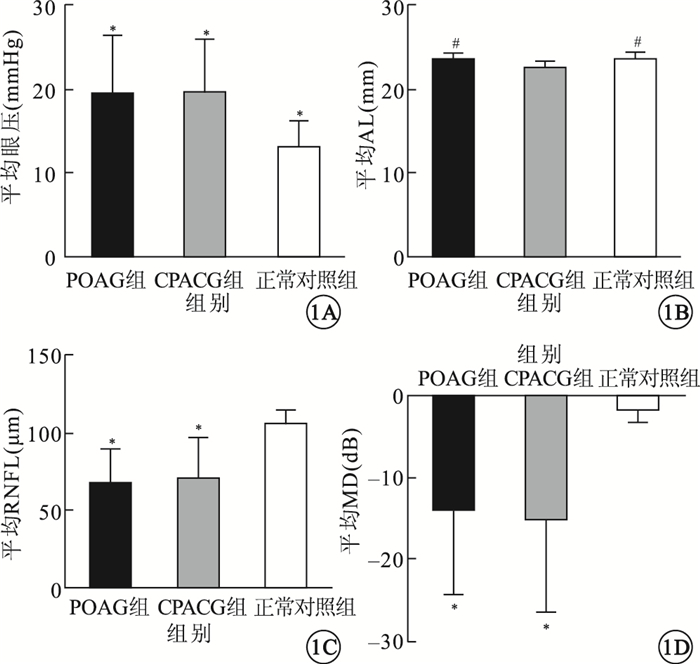 圖1
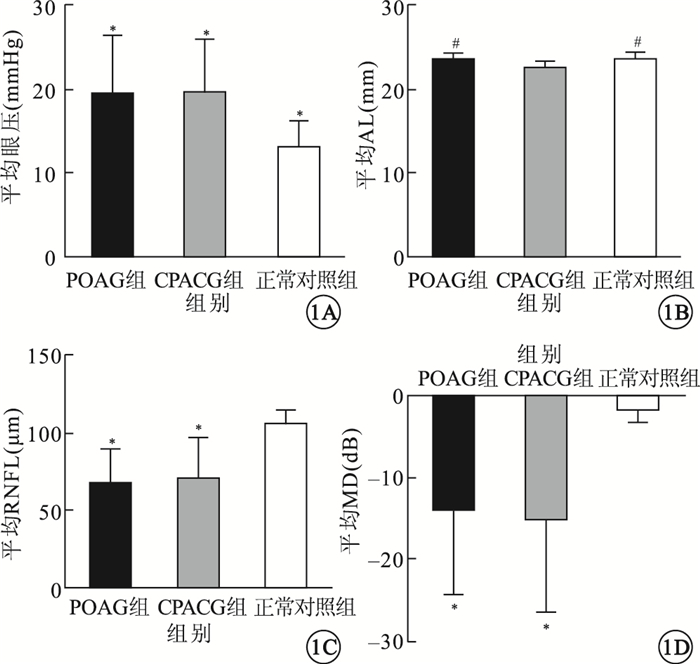
3組受檢眼之間平均眼壓、AL、RNFL值、MD值比較。1A.平均眼壓;1B.平均AL;1C.平均RNFL厚度;1D.平均MD。*與正常對照組比較,P < 0.05;#與CPACG組比較,P < 0.05
圖1
3組受檢眼之間平均眼壓、AL、RNFL值、MD值比較。1A.平均眼壓;1B.平均AL;1C.平均RNFL厚度;1D.平均MD。*與正常對照組比較,P < 0.05;#與CPACG組比較,P < 0.05
眼壓測量后2~3 h采用德國Heidelberg公司頻域OCT儀測量篩板厚度(LCT)及篩板前表面深度(ALCSD)。入射光為紅外光,波長870 nm,選擇EDI模式。掃描速度40 000 A掃描/s,軸向分辨率5 μm,橫向分辨率6 μm。患者注視鏡頭內視盤注視點,以20°掃描角度對視盤中央行放射狀掃描,開啟ART,獲得6條高分辨率的篩板B掃描圖像,每幅圖像由30幀圖像疊加降噪以獲得最佳圖像質量,選取圖像清晰者保存。以視盤為中心行直徑3.4 mm環形掃描,每幅圖像由100幀圖像疊加而成,應用系統自帶軟件分析計算視盤周圍全周RNFL厚度。
頻域OCT圖像中視盤深部板層狀強反射定義為篩板;強反射結構的前后界面分別定義為篩板的前后表面[4]。篩板前后表面之間的距離定義為LCT。以視盤邊緣Bruch膜開口連線作為參考平面。篩板前表面與參考平面間的垂直距離定義為ALCSD。以每條掃描徑線參考平面上的中心點及距離中心點兩側各100 μm的旁中心點為測量點,每一只眼共獲得6個中心點LCT及ALCSD,12個旁中心點LCT及ALCSD。分別以6個篩板中心點LCT、ALCSD的平均值為中央LCT (CLCT)及中央ALCSD (CALCSD),12個篩板旁中心點LCT、ALCSD的平均值為旁中央LCT (P-CLCT)及旁中央ALCSD (P-CALCSD)。以CLCT與P-CLCT的平均值為平均LCT (MLCT),CALCSD與P-CALCSD的平均值為平均ALCSD (MALCSD)。每一只眼均由同一位熟練觀察者測量掃描數據并獲取平均值。將所獲得圖像導入Adobe Photoshop CS6進行測量(圖 2)。
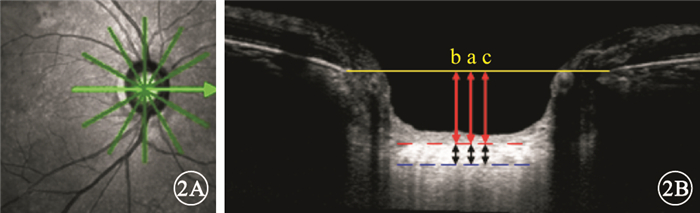 圖2
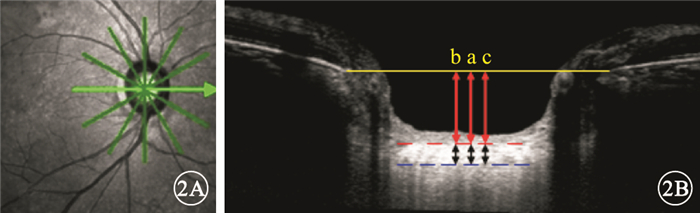
篩板測量示意圖。1A.視盤紅外反射像,水平(綠箭)及放射狀(綠線)掃描。2B.視盤水平掃描頻域OCT像,紅色虛線為篩板前表面,藍色虛線為篩板后表面,紅、藍色虛線之間距離為LCT (黑箭頭之間);黃色線為參考平面,黃色線與紅色虛線之間距離為ALCSD (紅色箭頭之間);a、b、c:測量點,分別為參考平面的中心點、距中心點顳側及鼻側(或下方及上方)各100 μm的旁中心點
圖2
篩板測量示意圖。1A.視盤紅外反射像,水平(綠箭)及放射狀(綠線)掃描。2B.視盤水平掃描頻域OCT像,紅色虛線為篩板前表面,藍色虛線為篩板后表面,紅、藍色虛線之間距離為LCT (黑箭頭之間);黃色線為參考平面,黃色線與紅色虛線之間距離為ALCSD (紅色箭頭之間);a、b、c:測量點,分別為參考平面的中心點、距中心點顳側及鼻側(或下方及上方)各100 μm的旁中心點
由測量者A、測量者B 2名不同測量者在不同時間分別獨立對正常對照組中的20名受檢者的20只受檢眼進行篩板數據測量,獲得不同測量者篩板測量的可重復性數據;測量者A、測量者B分別在不同時間對所測量的正常對照組中的20只受檢眼重復測量3次,每一次測量的間隔時間≥10 d,獲得同一測量者篩板測量的可重復性數據。
應用SPSS 17.0統計軟件進行統計學分析處理,對所有數據進行正態性檢驗,呈正態分布且符合方差齊性的多組數據之間差異比較采用單因素方差分析;基本信息組間兩兩比較采用最小顯著差法t檢驗;以同一測量者內和不同測量者之間的類內相關系數(ICC)分析測量數據的可重復性。P < 0.05為差異有統計學意義。
2 結果
測量者A、測量者B分別測得的MLCT值為(209.17±17.93)、(211.20±17.22) μm;MALCSD值為(393.87±144.52)、(393.47±145.13)μm。不同測量者之間測量的MLCT值[ICC=0.945,95%可信區間(CI)為0.908~0.967]、MALCSD值(ICC=0.994,95%可信區間為0.990~0.996)的可重復性較好(P < 0.01)。測量者A 3次測量的MLCT值(ICC=0.961,95%CI為0.940~0.975)、MALCSD值(ICC=0.996,95%CI為0.988~0.996),測量者B 3次測量的MLCT值(ICC=0.957,95%CI為0.940~0.973)、MALCSD值(ICC=0.998,95%CI為0.987~0.999)可重復性均較好(P < 0.01)(表 1, 2)。
POAG組、CPACG組、正常對照組受檢眼CLCT、P-CLCT、MLCT、CALCSD、P-ALCSD、MALCSD值之間比較,差異均有統計學意義(F=63.92、67.93、63.69、16.42、15.45、15.28,P < 0.05) (圖 2)。3組受檢眼之間兩兩比較,POAG組受檢眼與CPACG組受檢眼CALCSD、P-ALCSD、MALCSD值之間差異無統計學意義(t=0.62、0.64、0.63,P > 0.05)。POAG組受檢眼CLCT、P-CLCT、MLCT較CPACG組受檢眼薄,差異有統計學意義(t=-2.04、-2.24、-1.96,P=0.03)。POAG組、CPACG組受檢眼CLCT、P-CLCT、MLCT較正常對照組受檢眼變薄,差異有統計學意義(t=-11.78、-12.29、-11.76、-9.84、-9.97、-9.88,P < 0.01);CALCSD、P-ALCSD、MALCSD較正常對照組受檢眼加深,差異有統計學意義(t=5.81、5.69、5.65、5.16、4.98、4.96,P < 0.01) (圖 3)。
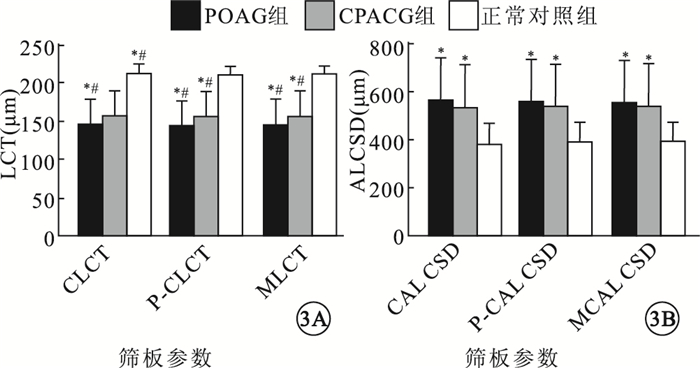 圖3
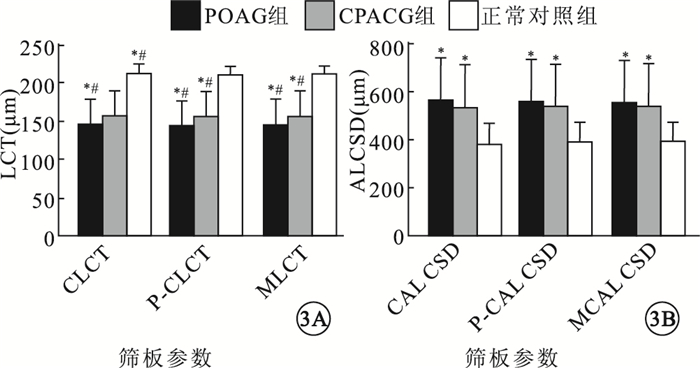
3組受檢眼之間LCT、ALCSD值比較。3A.LCT值;3B.ALCSD值。*與正常對照組比較,P < 0.05;#POAG組與CPACG組比較,P < 0.05
圖3
3組受檢眼之間LCT、ALCSD值比較。3A.LCT值;3B.ALCSD值。*與正常對照組比較,P < 0.05;#POAG組與CPACG組比較,P < 0.05
3 討論
青光眼視神經損害的特點是視網膜神經節細胞(RGC)進行性喪失[10]。RGC早期變化包括軸突代謝物質的剝奪及軸漿流運輸阻斷等[11]。篩板作為RGC軸突通過的管道,其形態學變化極有可能通過阻斷軸漿流運輸而引起RGC的損傷[1, 12-14]。應用EDI-OCT技術進行活體篩板形態結構測量國外已有報道[3, 4],國內報道較少。在應用于臨床研究之前,為衡量及評價觀察者信度及復測信度,需進行可重復性檢驗[15]。國外研究報道EDI-OCT測量LCT可重復性的ICC值在0.831~0.966[16, 17],ALCSD的ICC值在0.990~0.998[18, 19]。本研究中同一測量者內及不同測量者之間的可重復性ICC值均 > 0.90。與上述文獻報道結果相近,說明應用EDI-OCT測量篩板結構參數的可重復性較好。
Qiugley等[1]觀察了15只青光眼的病理組織結構,認為青光眼RNFL損害的原因在于篩板阻斷了軸漿流運輸;隨后又應用掃描電子纖維鏡對不同程度視野缺損及RNFL缺損青光眼篩板形態進行觀察,發現在青光眼視野缺損前就已出現篩板板層的壓縮,隨病程進展篩板整體后凹,呈“U”型改變[20]。Quigley等[2]應用掃描電子顯微鏡對一組相同視野缺損程度的POAG尸體眼測量的平均LCT、ALCSD值分別為(148.00±58.00)、(535.00±126.00) μm。Lee等[19]應用EDI-OCT對一組相同視野缺損程度POAG患眼行青光眼手術半年后的LCT、ALCSD進行了測量,平均LCT值變化范圍在(169.39±24.70)~(204.75±26.43) μm,ALCSD值在(503.90±142.67)~(614.58±179.57)μm。Park等[16, 20]應用EDI-OCT測量比較了49只正常眼及137只青光眼LCT,發現青光眼篩板較正常眼明顯變薄;其后又對比了正常眼與可疑青光眼及不同病程POAG患眼的活體篩板結構,結果顯示可疑青光眼及POAG患眼ALCSD整體加深,篩板后移主要發生在可疑青光眼及早中期POAG患眼。另有研究顯示正常眼壓性青光眼同樣出現LCT變薄,ALCSD增加[21, 22]。本研究中POAG組受檢眼篩板參數與上述文獻報道相近,同時也顯示POAG組、CPACG組受檢眼LCT較正常對照組受檢眼變薄,ALCSD較正常對照組受檢眼加深。青光眼篩板的結構改變可能是由于慢性眼壓升高及篩板組織重塑所致[2]。
目前國內外關于CPACG活體篩板結構的研究報道尚少。本研究結果顯示,CPACG組受檢眼LCT較正常對照組受檢眼薄,ALCS較正常對照組受檢眼深。說明在高眼壓的作用下CPACG同樣存在篩板結構的改變。為了觀察2種慢性眼壓升高青光眼類型篩板結構的差異,我們比較了相同眼壓、相同視野損害和RNFL損害狀態下POAG和CPACG的LCT和ALCSD,結果顯示CPACG組受檢眼LCT較POAG組受檢眼增厚,但ALCSD深度無差異,造成這些差異的原因尚不清楚。既往研究報道,正常人AL與LCT無相關性,而高度近視患眼篩板較正常人變薄[23, 24]。但目前尚未見短AL與LCT關系的報道,所以尚未明了CPACG患眼AL短是否導致其LCT與POAG患眼LCT差異的原因。此外導致兩者LCT差異的原因可能跟這2種類型青光眼性視神經損傷的機制不同有關。既往研究認為,CPACG的特殊解剖結構易形成相對瞳孔阻滯導致房角狹窄關閉引起眼壓升高造成視功能損傷,主要為機械性壓力所致;而POAG視功能損害的多因素學說則認為,眼壓升高是青光眼視功能損害的基本因素,但并不是唯一因素,年齡、種族、糖尿病、高血壓、血管痙攣、眼動脈低灌注壓、跨篩板壓差以及血液流變學異常等都可以單獨或與眼壓共同作用導致視神經損傷[25, 26]。本研究結果也提示除了眼壓因素,可能存在其他如血管因素作用于篩板,導致POAG患眼LCT較CPACG患眼LCT變薄;而兩組間ALCSD的差異并沒有統計學意義,具體原因還有待于進一步深入研究。
本研究尚存在一定的局限性。本研究是橫斷面研究且樣本量有限, 目前尚不能確定CPACG篩板與POAG差異的原因,尚需進行大樣本前瞻性縱向研究。
篩板是青光眼視神經損害的原發部位,由于其深埋于視盤之下不易直接觀察,既往研究僅局限于動物實驗或人尸體眼篩板的病理組織學觀察[1, 2]。隨著頻域光相干斷層掃描(OCT)增強深部成像技術(EDI)(EDI-OCT)的應用,已觀察到活體篩板的形態變化[3, 4]。目前國外相關研究多集中于開角型青光眼篩板形態觀察,發現篩板出現明顯后凸變薄且篩板的結構缺損與視野進展相關[5-9]。說明篩板因素在青光眼發生發展中有重要作用。原發性開角型青光眼(POAG)和原發性慢性閉角型青光眼(CPACG)病程以及視神經和視野損害均相似,但兩者有關結構改變和視功能的損害相關性是否存在差異,目前仍不明確。因此,我們應用EDI-OCT對一組POAG和CPACG患者的篩板進行了觀察測量,并與正常對照者相應部位的篩板進行了比較。現將結果報道如下。
1 對象和方法
2015年4~12月在中山眼科中心門診確診的POAG患者73例73只眼(POAG組)、CPACG患者64例64只眼(CPACG組)以及正常人40名40只眼(正常對照組)納入研究。所有受檢者均獲知情同意并簽署相應文件。
所有受檢者均行最佳矯正視力、眼壓、裂隙燈顯微鏡、前房角鏡、90D前置鏡、屈光度、頻域OCT檢查和眼軸長度(AL)測定。眼壓檢查為Goldmann壓平眼壓計;屈光度檢查為電腦驗光儀RM-100型(日本Topcon公司);AL測定為A型超聲波儀US-1800型(日本Nidek公司);視野檢查為Humphrey自動視野計750i型(德國Zeiss公司)。
POAG組納入標準:(1) Goldmann壓平眼壓計測量眼壓 > 21 mmHg (1 mmHg=0.133 kPa);(2)具有青光眼視盤改變和視網膜神經纖維層(RNFL)缺損;(3)具有青光眼性視野缺損;(4)前房角為開角。CPACG組納入標準:(1)具有淺前房、窄房角的眼部解剖特征;(2)有反復眼壓輕度或中度升高的癥狀或無癥狀;(3)房角鏡檢查可見房角狹窄或房角粘連,Goldmann壓平眼壓計測量眼壓 > 21 mmHg;(4)進展期至晚期可見類似POAG的視盤及視野損害;(5)眼前節不存在急性高眼壓造成的缺血性損害特征。正常對照組納入標準:(1)裸眼或矯正視力≥1.0,屈光度球鏡-6.00~+2.00 D,柱鏡-1.00~+ 1.00 D;(2)視盤杯盤比(C/D)≤0.6,雙眼C/D差值≤0.2,眼底檢查未見異常;(3) Goldmann壓平眼壓計測量眼壓 < 21 mmHg;(4) Humphrey自動視野計視野檢查正常,頻域OCT檢查RNFL厚度正常。排除標準:(1)繼發性青光眼;(2)屈光度球鏡>+2.00 D或 < -6.00 D,或柱鏡>+1.00 D或 < -1.00 D;(3)既往有眼部手術史;(4)眼內存在炎癥反應;(5)合并其他視網膜、脈絡膜或視神經疾病,嚴重屈光間質混濁、明顯全身疾病、顱內疾病、或其他可能影響頻域OCT檢查的神經和精神疾病;(6)相關檢查配合不佳者或圖像成像不佳者。POAG組73例73只眼中,男性39例39只眼,女性34例34只眼;平均年齡(59.68±12.07)歲。CPACG組64例64只眼中,男性25例25只眼,女性39例39只眼;平均年齡(58.69±9.33)歲。正常對照組40名40只眼中,男性15名15只眼,女性25名25只眼;平均年齡(60.53±10.36)歲。3組受檢者之間性別構成比(χ2=2.07)、平均年齡(F=0.38)比較,差異均無統計學意義(P > 0.05)。3組受檢眼頻域OCT測量時眼壓、AL、RNFL厚度值及平均視野缺損(MD)值比較,差異均有統計學意義(F=15.67、21.15、44.40、27.99,P < 0.05)(圖 1)。3組受檢眼之間兩兩比較,POAG組受檢眼與CPACG組受檢眼平均眼壓、RNFL厚度值、MD值差異無統計學意義(t=1.07、3.69、1.67,P > 0.05),AL差異有統計學意義(t=0.16,P < 0.01);POAG組受檢眼與正常對照組受檢眼AL差異無統計學意義(t=0.18,P > 0.05);CPACG組受檢眼與正常對照組受檢眼AL差異有統計學意義(t=0.17,P < 0.01);POAG組、CPACG組受檢眼與正常對照組受檢眼平均眼壓、RNFL厚度值、MD值差異均有統計學意義(t=1.25、4.25、1.91、1.26、4.34、1.92,P < 0.01) (圖 1)。
 圖1
3組受檢眼之間平均眼壓、AL、RNFL值、MD值比較。1A.平均眼壓;1B.平均AL;1C.平均RNFL厚度;1D.平均MD。*與正常對照組比較,P < 0.05;#與CPACG組比較,P < 0.05
圖1
3組受檢眼之間平均眼壓、AL、RNFL值、MD值比較。1A.平均眼壓;1B.平均AL;1C.平均RNFL厚度;1D.平均MD。*與正常對照組比較,P < 0.05;#與CPACG組比較,P < 0.05
眼壓測量后2~3 h采用德國Heidelberg公司頻域OCT儀測量篩板厚度(LCT)及篩板前表面深度(ALCSD)。入射光為紅外光,波長870 nm,選擇EDI模式。掃描速度40 000 A掃描/s,軸向分辨率5 μm,橫向分辨率6 μm。患者注視鏡頭內視盤注視點,以20°掃描角度對視盤中央行放射狀掃描,開啟ART,獲得6條高分辨率的篩板B掃描圖像,每幅圖像由30幀圖像疊加降噪以獲得最佳圖像質量,選取圖像清晰者保存。以視盤為中心行直徑3.4 mm環形掃描,每幅圖像由100幀圖像疊加而成,應用系統自帶軟件分析計算視盤周圍全周RNFL厚度。
頻域OCT圖像中視盤深部板層狀強反射定義為篩板;強反射結構的前后界面分別定義為篩板的前后表面[4]。篩板前后表面之間的距離定義為LCT。以視盤邊緣Bruch膜開口連線作為參考平面。篩板前表面與參考平面間的垂直距離定義為ALCSD。以每條掃描徑線參考平面上的中心點及距離中心點兩側各100 μm的旁中心點為測量點,每一只眼共獲得6個中心點LCT及ALCSD,12個旁中心點LCT及ALCSD。分別以6個篩板中心點LCT、ALCSD的平均值為中央LCT (CLCT)及中央ALCSD (CALCSD),12個篩板旁中心點LCT、ALCSD的平均值為旁中央LCT (P-CLCT)及旁中央ALCSD (P-CALCSD)。以CLCT與P-CLCT的平均值為平均LCT (MLCT),CALCSD與P-CALCSD的平均值為平均ALCSD (MALCSD)。每一只眼均由同一位熟練觀察者測量掃描數據并獲取平均值。將所獲得圖像導入Adobe Photoshop CS6進行測量(圖 2)。
 圖2
篩板測量示意圖。1A.視盤紅外反射像,水平(綠箭)及放射狀(綠線)掃描。2B.視盤水平掃描頻域OCT像,紅色虛線為篩板前表面,藍色虛線為篩板后表面,紅、藍色虛線之間距離為LCT (黑箭頭之間);黃色線為參考平面,黃色線與紅色虛線之間距離為ALCSD (紅色箭頭之間);a、b、c:測量點,分別為參考平面的中心點、距中心點顳側及鼻側(或下方及上方)各100 μm的旁中心點
圖2
篩板測量示意圖。1A.視盤紅外反射像,水平(綠箭)及放射狀(綠線)掃描。2B.視盤水平掃描頻域OCT像,紅色虛線為篩板前表面,藍色虛線為篩板后表面,紅、藍色虛線之間距離為LCT (黑箭頭之間);黃色線為參考平面,黃色線與紅色虛線之間距離為ALCSD (紅色箭頭之間);a、b、c:測量點,分別為參考平面的中心點、距中心點顳側及鼻側(或下方及上方)各100 μm的旁中心點
由測量者A、測量者B 2名不同測量者在不同時間分別獨立對正常對照組中的20名受檢者的20只受檢眼進行篩板數據測量,獲得不同測量者篩板測量的可重復性數據;測量者A、測量者B分別在不同時間對所測量的正常對照組中的20只受檢眼重復測量3次,每一次測量的間隔時間≥10 d,獲得同一測量者篩板測量的可重復性數據。
應用SPSS 17.0統計軟件進行統計學分析處理,對所有數據進行正態性檢驗,呈正態分布且符合方差齊性的多組數據之間差異比較采用單因素方差分析;基本信息組間兩兩比較采用最小顯著差法t檢驗;以同一測量者內和不同測量者之間的類內相關系數(ICC)分析測量數據的可重復性。P < 0.05為差異有統計學意義。
2 結果
測量者A、測量者B分別測得的MLCT值為(209.17±17.93)、(211.20±17.22) μm;MALCSD值為(393.87±144.52)、(393.47±145.13)μm。不同測量者之間測量的MLCT值[ICC=0.945,95%可信區間(CI)為0.908~0.967]、MALCSD值(ICC=0.994,95%可信區間為0.990~0.996)的可重復性較好(P < 0.01)。測量者A 3次測量的MLCT值(ICC=0.961,95%CI為0.940~0.975)、MALCSD值(ICC=0.996,95%CI為0.988~0.996),測量者B 3次測量的MLCT值(ICC=0.957,95%CI為0.940~0.973)、MALCSD值(ICC=0.998,95%CI為0.987~0.999)可重復性均較好(P < 0.01)(表 1, 2)。
POAG組、CPACG組、正常對照組受檢眼CLCT、P-CLCT、MLCT、CALCSD、P-ALCSD、MALCSD值之間比較,差異均有統計學意義(F=63.92、67.93、63.69、16.42、15.45、15.28,P < 0.05) (圖 2)。3組受檢眼之間兩兩比較,POAG組受檢眼與CPACG組受檢眼CALCSD、P-ALCSD、MALCSD值之間差異無統計學意義(t=0.62、0.64、0.63,P > 0.05)。POAG組受檢眼CLCT、P-CLCT、MLCT較CPACG組受檢眼薄,差異有統計學意義(t=-2.04、-2.24、-1.96,P=0.03)。POAG組、CPACG組受檢眼CLCT、P-CLCT、MLCT較正常對照組受檢眼變薄,差異有統計學意義(t=-11.78、-12.29、-11.76、-9.84、-9.97、-9.88,P < 0.01);CALCSD、P-ALCSD、MALCSD較正常對照組受檢眼加深,差異有統計學意義(t=5.81、5.69、5.65、5.16、4.98、4.96,P < 0.01) (圖 3)。
 圖3
3組受檢眼之間LCT、ALCSD值比較。3A.LCT值;3B.ALCSD值。*與正常對照組比較,P < 0.05;#POAG組與CPACG組比較,P < 0.05
圖3
3組受檢眼之間LCT、ALCSD值比較。3A.LCT值;3B.ALCSD值。*與正常對照組比較,P < 0.05;#POAG組與CPACG組比較,P < 0.05
3 討論
青光眼視神經損害的特點是視網膜神經節細胞(RGC)進行性喪失[10]。RGC早期變化包括軸突代謝物質的剝奪及軸漿流運輸阻斷等[11]。篩板作為RGC軸突通過的管道,其形態學變化極有可能通過阻斷軸漿流運輸而引起RGC的損傷[1, 12-14]。應用EDI-OCT技術進行活體篩板形態結構測量國外已有報道[3, 4],國內報道較少。在應用于臨床研究之前,為衡量及評價觀察者信度及復測信度,需進行可重復性檢驗[15]。國外研究報道EDI-OCT測量LCT可重復性的ICC值在0.831~0.966[16, 17],ALCSD的ICC值在0.990~0.998[18, 19]。本研究中同一測量者內及不同測量者之間的可重復性ICC值均 > 0.90。與上述文獻報道結果相近,說明應用EDI-OCT測量篩板結構參數的可重復性較好。
Qiugley等[1]觀察了15只青光眼的病理組織結構,認為青光眼RNFL損害的原因在于篩板阻斷了軸漿流運輸;隨后又應用掃描電子纖維鏡對不同程度視野缺損及RNFL缺損青光眼篩板形態進行觀察,發現在青光眼視野缺損前就已出現篩板板層的壓縮,隨病程進展篩板整體后凹,呈“U”型改變[20]。Quigley等[2]應用掃描電子顯微鏡對一組相同視野缺損程度的POAG尸體眼測量的平均LCT、ALCSD值分別為(148.00±58.00)、(535.00±126.00) μm。Lee等[19]應用EDI-OCT對一組相同視野缺損程度POAG患眼行青光眼手術半年后的LCT、ALCSD進行了測量,平均LCT值變化范圍在(169.39±24.70)~(204.75±26.43) μm,ALCSD值在(503.90±142.67)~(614.58±179.57)μm。Park等[16, 20]應用EDI-OCT測量比較了49只正常眼及137只青光眼LCT,發現青光眼篩板較正常眼明顯變薄;其后又對比了正常眼與可疑青光眼及不同病程POAG患眼的活體篩板結構,結果顯示可疑青光眼及POAG患眼ALCSD整體加深,篩板后移主要發生在可疑青光眼及早中期POAG患眼。另有研究顯示正常眼壓性青光眼同樣出現LCT變薄,ALCSD增加[21, 22]。本研究中POAG組受檢眼篩板參數與上述文獻報道相近,同時也顯示POAG組、CPACG組受檢眼LCT較正常對照組受檢眼變薄,ALCSD較正常對照組受檢眼加深。青光眼篩板的結構改變可能是由于慢性眼壓升高及篩板組織重塑所致[2]。
目前國內外關于CPACG活體篩板結構的研究報道尚少。本研究結果顯示,CPACG組受檢眼LCT較正常對照組受檢眼薄,ALCS較正常對照組受檢眼深。說明在高眼壓的作用下CPACG同樣存在篩板結構的改變。為了觀察2種慢性眼壓升高青光眼類型篩板結構的差異,我們比較了相同眼壓、相同視野損害和RNFL損害狀態下POAG和CPACG的LCT和ALCSD,結果顯示CPACG組受檢眼LCT較POAG組受檢眼增厚,但ALCSD深度無差異,造成這些差異的原因尚不清楚。既往研究報道,正常人AL與LCT無相關性,而高度近視患眼篩板較正常人變薄[23, 24]。但目前尚未見短AL與LCT關系的報道,所以尚未明了CPACG患眼AL短是否導致其LCT與POAG患眼LCT差異的原因。此外導致兩者LCT差異的原因可能跟這2種類型青光眼性視神經損傷的機制不同有關。既往研究認為,CPACG的特殊解剖結構易形成相對瞳孔阻滯導致房角狹窄關閉引起眼壓升高造成視功能損傷,主要為機械性壓力所致;而POAG視功能損害的多因素學說則認為,眼壓升高是青光眼視功能損害的基本因素,但并不是唯一因素,年齡、種族、糖尿病、高血壓、血管痙攣、眼動脈低灌注壓、跨篩板壓差以及血液流變學異常等都可以單獨或與眼壓共同作用導致視神經損傷[25, 26]。本研究結果也提示除了眼壓因素,可能存在其他如血管因素作用于篩板,導致POAG患眼LCT較CPACG患眼LCT變薄;而兩組間ALCSD的差異并沒有統計學意義,具體原因還有待于進一步深入研究。
本研究尚存在一定的局限性。本研究是橫斷面研究且樣本量有限, 目前尚不能確定CPACG篩板與POAG差異的原因,尚需進行大樣本前瞻性縱向研究。