引用本文: 葉祖科, 尹小芳, 羅書科, 盧彥. 葡萄膜炎繼發視盤新生血管一例. 中華眼底病雜志, 2016, 32(4): 436-437. doi: 10.3760/cma.j.issn.1005-1015.2016.04.024 復制
患者女,20歲。因右眼突發視矇伴眼前黑影遮擋5 d來我院眼科就診。既往無眼病、全身病及家族疾病史。眼部檢查:右眼視力0.06,-0.75DC×180矯正無提高;左眼視力0.6,-0.75DS矯正1.0。右眼眼壓13.0 mmHg(1 mmHg=0.133 kPa),左眼眼壓 14.0 mmHg。裂隙燈顯微鏡檢查,雙眼球結膜輕度充血,角膜透明,散在塵狀角膜后沉著物,房水閃輝(+),房水細胞(+),虹膜無粘連,瞳孔大小正常、直接對光反射正常,晶狀體透明。右眼玻璃體血性混濁,眼底可見視盤新生血管,其余結構觀察不清。左眼玻璃體未見混濁,視網膜未見明顯異常。熒光素眼底血管造影(FFA)檢查,右眼視盤可見新生血管強熒光,下方視網膜前出血遮蔽熒光;隨造影時間延長,視盤新生血管熒光素滲漏,黃斑區及周邊視網膜小血管擴張、熒光素滲漏,未見無灌注區;晚期視盤見彌漫性強熒光,黃斑區花瓣樣熒光素積存(圖 1)。左眼早期視盤及周邊視網膜散在小血管擴張、熒光素滲漏;晚期視盤呈強熒光,邊界清晰,黃斑區未見熒光素積存。頻域光相干斷層掃描(SD-OCT)檢查,右眼視網膜前大量顆粒狀強反射,黃斑視網膜增厚,層間可見弱反射腔隙;左眼未見明顯異常。全身檢查以及血尿常規、肝腎功能、紅細胞沉降率、C反應蛋白、紅斑狼瘡相關自身抗體、類風濕因子、抗鏈球菌溶血素O、補體、免疫球蛋白、人類白細胞抗原B27、抗中性粒細胞胞漿抗體以及乙肝、丙肝、梅毒、艾滋病病原體4項等實驗室輔助檢查未見異常。頭顱核磁共振、胸部X線片檢查未見異常。診斷:雙眼全葡萄膜炎,右眼玻璃體積血,雙眼屈光不正。
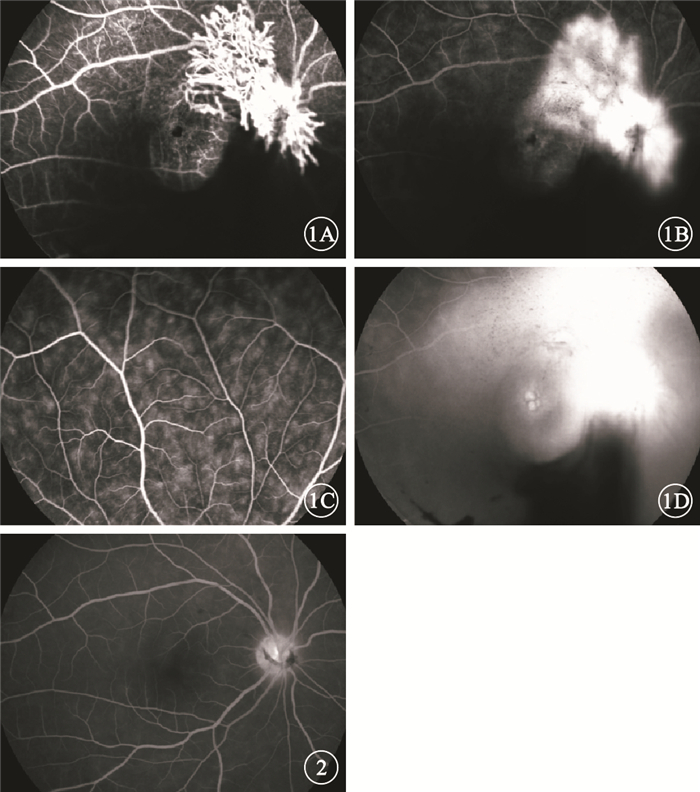 圖1
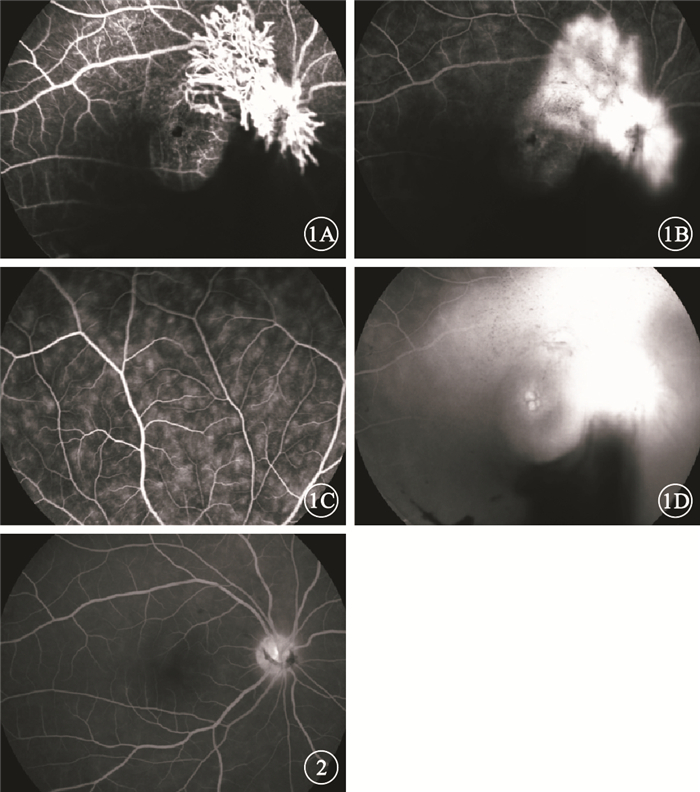
右眼FFA像。1A. 21 s, 視盤新生血管性強熒光,下方視網膜前出血遮蔽熒光;1B. 2 min 2 s,視盤新生血管熒光素滲漏;1C. 2 min 24 s,周邊視網膜小血管擴張、滲漏,未見無灌注區;1D. 21 min 1 s,視盤彌漫性強熒光,黃斑區花瓣樣熒光素積存 圖 2 糖皮質激素治療 12周右眼FFA像。19 min 58 s,視盤邊界尚清,其表面小片膜狀遮蔽熒光,未見新生血管性強熒光黃斑區未見熒光素積存
圖1
右眼FFA像。1A. 21 s, 視盤新生血管性強熒光,下方視網膜前出血遮蔽熒光;1B. 2 min 2 s,視盤新生血管熒光素滲漏;1C. 2 min 24 s,周邊視網膜小血管擴張、滲漏,未見無灌注區;1D. 21 min 1 s,視盤彌漫性強熒光,黃斑區花瓣樣熒光素積存 圖 2 糖皮質激素治療 12周右眼FFA像。19 min 58 s,視盤邊界尚清,其表面小片膜狀遮蔽熒光,未見新生血管性強熒光黃斑區未見熒光素積存
收入院治療,雙眼局部妥布霉素地塞米松滴眼液、普拉洛芬滴眼液抗炎治療;住院第3天起給予全身甲基強的松龍120 mg 靜脈滴注,1次/d,持續5 d;之后劑量減為80 mg 靜脈滴注,1次/d,持續3 d。住院第12天出院,出院時右眼矯正視力0.3,左眼矯正視力1.0。雙眼眼前節未見明顯異常。右眼玻璃體積血減少,視盤新生血管較前減小。出院后,按1.2 mg/kg 劑量給予醋酸潑尼松60 mg口服,1次/d,持續7 d;以后醋酸潑尼松每周減量5 mg;減至10 mg,1次/d維持治療。糖皮質激素治療12周復查,雙眼矯正視力1.0。右眼后極部玻璃體積血完全吸收,視盤殘留小片白色膜狀物,新生血管完全消退。右眼SD-OCT復查未見明顯異常。FFA復查,右眼早期視盤可見小片膜狀遮蔽熒光,視網膜散在小血管熒光素滲漏;晚期視盤稍強熒光,邊界尚清,黃斑未見熒光素積存(圖 2)。左眼未見明顯異常。
討論????葡萄膜炎繼發眼底新生血管,臨床上較為少見,發生率約為0.77%;低齡、后或全葡萄膜炎、活動性炎癥增加了其發生的風險[1]。本例患者為年輕女性,雙眼存在前房炎癥反應,FFA見右眼視盤新生血管強熒光,視網膜彌漫小血管熒光素滲漏;左眼視盤、視網膜血管也有不同程度熒光素滲漏。雙眼均未見無灌注區。葡萄膜炎診斷成立。盡管其以玻璃體積血和視盤新生血管首診,但未合并眼底缺血性病變。
本例患者右眼視盤新生血管成因尚不明確。既往文獻報道了慢性葡萄膜炎繼發視盤新生血管,FFA未發現眼底存在血管阻塞或無灌注區[2-4]。Tugal-Tutkun等[5]報道了26例Behets病繼發視盤新生血管,87%為炎癥相關而無眼底缺血表現。本例患者FFA未見眼底無灌注區,與文獻報道相符。但患者以往并無慢性葡萄膜炎病史,也未發現全身感染或免疫性疾病證據。急性起病的視盤新生血管發生機制尚需進一步探討。已有研究發現,并發黃斑囊樣水腫的葡萄膜炎患者玻璃 體腔內血管內皮生長因子(VEGF)含量明顯增高,炎癥可以是獨立刺激因素,通過多種途徑促進VEGF釋放[6, 7]。分析本例患者的視盤新生血管、黃斑囊樣水腫形成可能與眼底VEGF水平異常有關。
葡萄膜炎繼發視盤新生血管,治療前需仔細鑒別。FFA對于判斷有無眼底缺血性病變十分重要。此外,還需注意有無全身潛在感染或免疫性疾病可能。治療上,對于無眼底缺血者,糖皮質激素治療效果顯著[2-4]。本例患者全身糖皮質激素抗炎治療3個月,新生血管完全消退。Kuo和Cunningham[8]認為所有此類病例都值得嘗試局部或全身糖皮質激素治療,只有FFA明確存在眼底無灌注區時需聯合激光光凝治療。該病治療過程還需嚴密隨訪觀察,注意復查FFA了解病變進展情況,警惕眼底繼發性缺血改變及新生血管復發的危險。
患者女,20歲。因右眼突發視矇伴眼前黑影遮擋5 d來我院眼科就診。既往無眼病、全身病及家族疾病史。眼部檢查:右眼視力0.06,-0.75DC×180矯正無提高;左眼視力0.6,-0.75DS矯正1.0。右眼眼壓13.0 mmHg(1 mmHg=0.133 kPa),左眼眼壓 14.0 mmHg。裂隙燈顯微鏡檢查,雙眼球結膜輕度充血,角膜透明,散在塵狀角膜后沉著物,房水閃輝(+),房水細胞(+),虹膜無粘連,瞳孔大小正常、直接對光反射正常,晶狀體透明。右眼玻璃體血性混濁,眼底可見視盤新生血管,其余結構觀察不清。左眼玻璃體未見混濁,視網膜未見明顯異常。熒光素眼底血管造影(FFA)檢查,右眼視盤可見新生血管強熒光,下方視網膜前出血遮蔽熒光;隨造影時間延長,視盤新生血管熒光素滲漏,黃斑區及周邊視網膜小血管擴張、熒光素滲漏,未見無灌注區;晚期視盤見彌漫性強熒光,黃斑區花瓣樣熒光素積存(圖 1)。左眼早期視盤及周邊視網膜散在小血管擴張、熒光素滲漏;晚期視盤呈強熒光,邊界清晰,黃斑區未見熒光素積存。頻域光相干斷層掃描(SD-OCT)檢查,右眼視網膜前大量顆粒狀強反射,黃斑視網膜增厚,層間可見弱反射腔隙;左眼未見明顯異常。全身檢查以及血尿常規、肝腎功能、紅細胞沉降率、C反應蛋白、紅斑狼瘡相關自身抗體、類風濕因子、抗鏈球菌溶血素O、補體、免疫球蛋白、人類白細胞抗原B27、抗中性粒細胞胞漿抗體以及乙肝、丙肝、梅毒、艾滋病病原體4項等實驗室輔助檢查未見異常。頭顱核磁共振、胸部X線片檢查未見異常。診斷:雙眼全葡萄膜炎,右眼玻璃體積血,雙眼屈光不正。
 圖1
右眼FFA像。1A. 21 s, 視盤新生血管性強熒光,下方視網膜前出血遮蔽熒光;1B. 2 min 2 s,視盤新生血管熒光素滲漏;1C. 2 min 24 s,周邊視網膜小血管擴張、滲漏,未見無灌注區;1D. 21 min 1 s,視盤彌漫性強熒光,黃斑區花瓣樣熒光素積存 圖 2 糖皮質激素治療 12周右眼FFA像。19 min 58 s,視盤邊界尚清,其表面小片膜狀遮蔽熒光,未見新生血管性強熒光黃斑區未見熒光素積存
圖1
右眼FFA像。1A. 21 s, 視盤新生血管性強熒光,下方視網膜前出血遮蔽熒光;1B. 2 min 2 s,視盤新生血管熒光素滲漏;1C. 2 min 24 s,周邊視網膜小血管擴張、滲漏,未見無灌注區;1D. 21 min 1 s,視盤彌漫性強熒光,黃斑區花瓣樣熒光素積存 圖 2 糖皮質激素治療 12周右眼FFA像。19 min 58 s,視盤邊界尚清,其表面小片膜狀遮蔽熒光,未見新生血管性強熒光黃斑區未見熒光素積存
收入院治療,雙眼局部妥布霉素地塞米松滴眼液、普拉洛芬滴眼液抗炎治療;住院第3天起給予全身甲基強的松龍120 mg 靜脈滴注,1次/d,持續5 d;之后劑量減為80 mg 靜脈滴注,1次/d,持續3 d。住院第12天出院,出院時右眼矯正視力0.3,左眼矯正視力1.0。雙眼眼前節未見明顯異常。右眼玻璃體積血減少,視盤新生血管較前減小。出院后,按1.2 mg/kg 劑量給予醋酸潑尼松60 mg口服,1次/d,持續7 d;以后醋酸潑尼松每周減量5 mg;減至10 mg,1次/d維持治療。糖皮質激素治療12周復查,雙眼矯正視力1.0。右眼后極部玻璃體積血完全吸收,視盤殘留小片白色膜狀物,新生血管完全消退。右眼SD-OCT復查未見明顯異常。FFA復查,右眼早期視盤可見小片膜狀遮蔽熒光,視網膜散在小血管熒光素滲漏;晚期視盤稍強熒光,邊界尚清,黃斑未見熒光素積存(圖 2)。左眼未見明顯異常。
討論????葡萄膜炎繼發眼底新生血管,臨床上較為少見,發生率約為0.77%;低齡、后或全葡萄膜炎、活動性炎癥增加了其發生的風險[1]。本例患者為年輕女性,雙眼存在前房炎癥反應,FFA見右眼視盤新生血管強熒光,視網膜彌漫小血管熒光素滲漏;左眼視盤、視網膜血管也有不同程度熒光素滲漏。雙眼均未見無灌注區。葡萄膜炎診斷成立。盡管其以玻璃體積血和視盤新生血管首診,但未合并眼底缺血性病變。
本例患者右眼視盤新生血管成因尚不明確。既往文獻報道了慢性葡萄膜炎繼發視盤新生血管,FFA未發現眼底存在血管阻塞或無灌注區[2-4]。Tugal-Tutkun等[5]報道了26例Behets病繼發視盤新生血管,87%為炎癥相關而無眼底缺血表現。本例患者FFA未見眼底無灌注區,與文獻報道相符。但患者以往并無慢性葡萄膜炎病史,也未發現全身感染或免疫性疾病證據。急性起病的視盤新生血管發生機制尚需進一步探討。已有研究發現,并發黃斑囊樣水腫的葡萄膜炎患者玻璃 體腔內血管內皮生長因子(VEGF)含量明顯增高,炎癥可以是獨立刺激因素,通過多種途徑促進VEGF釋放[6, 7]。分析本例患者的視盤新生血管、黃斑囊樣水腫形成可能與眼底VEGF水平異常有關。
葡萄膜炎繼發視盤新生血管,治療前需仔細鑒別。FFA對于判斷有無眼底缺血性病變十分重要。此外,還需注意有無全身潛在感染或免疫性疾病可能。治療上,對于無眼底缺血者,糖皮質激素治療效果顯著[2-4]。本例患者全身糖皮質激素抗炎治療3個月,新生血管完全消退。Kuo和Cunningham[8]認為所有此類病例都值得嘗試局部或全身糖皮質激素治療,只有FFA明確存在眼底無灌注區時需聯合激光光凝治療。該病治療過程還需嚴密隨訪觀察,注意復查FFA了解病變進展情況,警惕眼底繼發性缺血改變及新生血管復發的危險。