引用本文: 張新芳, 冉瑞金, 李清韜, 劉毅. 116例非動脈炎性前部缺血性視神經病變發病相關因素的回顧性分析. 中華眼底病雜志, 2015, 31(6): 528-531. doi: 10.3760/cma.j.issn.1005-1015.2015.06.004 復制
非動脈炎性前部缺血性視神經病變(NAION)是50歲以上人群常見的視神經病變[1]。近年來通過對NAION的流行病學,發病危險因素等的研究[2],增進了對這一疾病的認識。目前較為明確的危險因素為糖尿病、高血壓、高血脂、心肌梗死等[3, 4]。但不同季節是否對發病率存在影響目前鮮見報道。為此,我們回顧性分析了一組NAION患者的臨床資料。現將結果報道如下。
1 對象和方法
回顧性病例分析。2004年1月至2014年1月臨床診斷為缺血性視神經病變患者169例中臨床資料完整的NAION患者116例134只眼納入研究。其中,門診患者32例,住院患者84例。患者中男性62例,女性54例;年齡45~75歲,平均年齡(61.2±6.8)歲。所有患者均詳細詢問病史、癥狀,行視力、裂隙燈顯微鏡、間接檢眼鏡、視野、熒光素眼底血管造影(FFA)檢查。同時行血壓、血糖、血脂、頭顱MRI或CT檢查。檢查結果符合NAION診斷標準[5]。排除疑似NAION、臨床資料不完整者。
視野檢查采用Humphry視野計,由熟練技師對患者詳細說明操作要求和注意事項并進行操作中監測。測定范圍為60°以內視野。視野檢查中假陰性、假陽性率均<30%;固視丟失率<20%。FFA檢查采用日本Topcon公司TRC-50EX眼底血管造影儀。
回顧分析年齡、視野、FFA、全身及眼部因素、發病月份與NAION的相關性。發病月份為患者主訴癥狀開始時間。全身合并多個疾病者,在統計危險因素時分別以單個危險因素累積相加,如患者同時患有糖尿病、高血壓,統計時在糖尿病和高血壓危險因素中各增加1例。糖尿病、高血壓患者均是發病前相關科室確診或本次住院確診病例。夜間低血壓來自住院患者病歷記錄。
采用SPSS 13.0統計軟件進行統計學分析處理。各組間比較應用擬合優度的χ2檢驗,P<0.05為差異有統計學意義。
2 結果
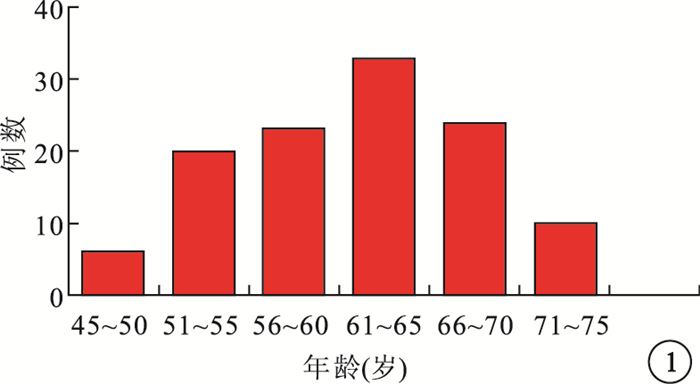
116例患者中,55~70歲80例,占68.97%。其中,61~65歲33例,占28.45%(圖 1)。
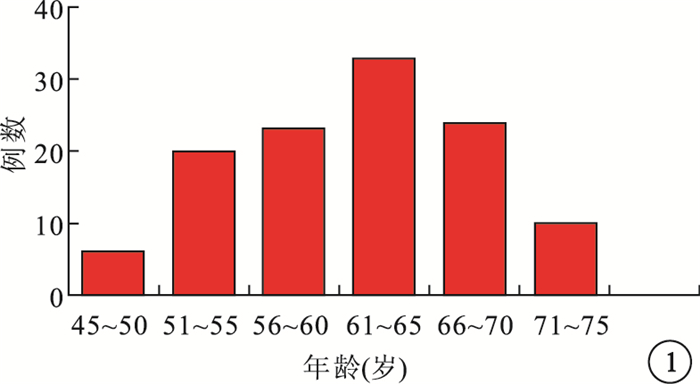 圖1
各年齡段患者分布
圖1
各年齡段患者分布
無全身疾病19例,占16.3%。有全身疾病97例,占83.7%。其中,糖尿病38例,占39.2%;高血壓32例,占32.9%,其中伴有夜間低血壓8例,占8.2%;血脂異常28例,占28.9%;腔隙性腦梗死等腦血管疾病16例,占16.5%;冠心病6例,占6.2%;腎病、關節炎、高眼壓、腫瘤等其他疾病12例,占12.4%。眼局部因素中,既往有白內障手術史3例,占所有患者的2.6%;小視盤5例,占所有患者的4.3%(圖 2)。糖尿病、高血壓構成比與無糖尿病、高血壓構成比比較,差異有統計學意義(χ2=362、259,P<0.05)。高血壓、糖尿病可能為NAION的危險因素。
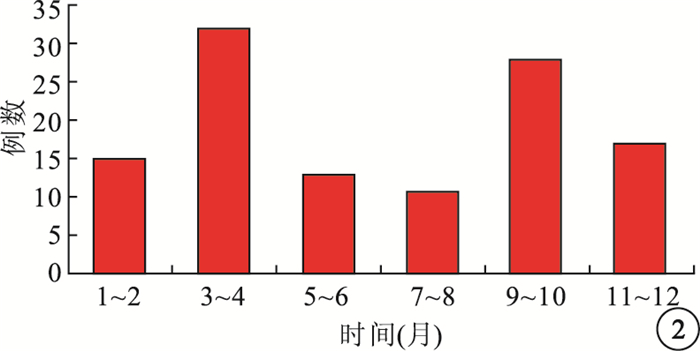
116例患者中,不同月份之間發病有較大差異(圖 2)。3~4、9~10月為發病的高發月份,占全年發病的51.7%。與其他月份發病率比較,差異有統計學意義(χ2=580,P<0.05)。
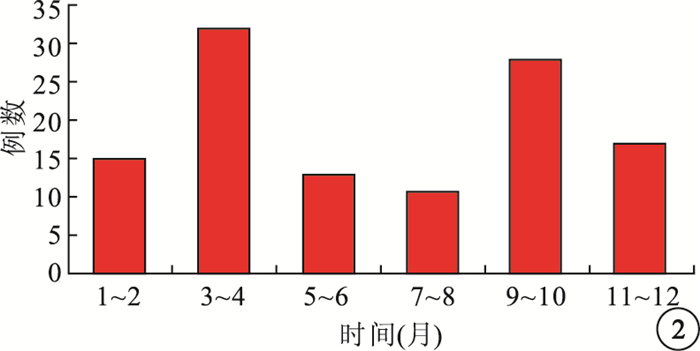 圖2
不同發病月份患者分布
圖2
不同發病月份患者分布
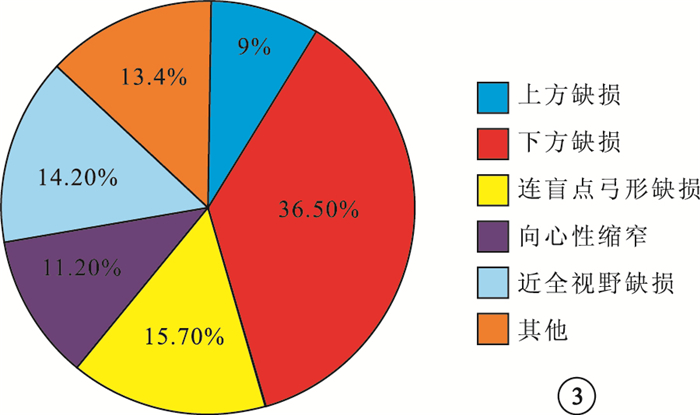
視野檢查結果顯示,下方視野缺損49只眼;上方視野缺損12只眼;與生理盲點相連的弓形視野缺損21只眼;向心性視野縮窄15只眼;近全視野缺損19只眼;不規則視野缺損、中心暗點、多象限視野缺損18只眼(圖 3)。
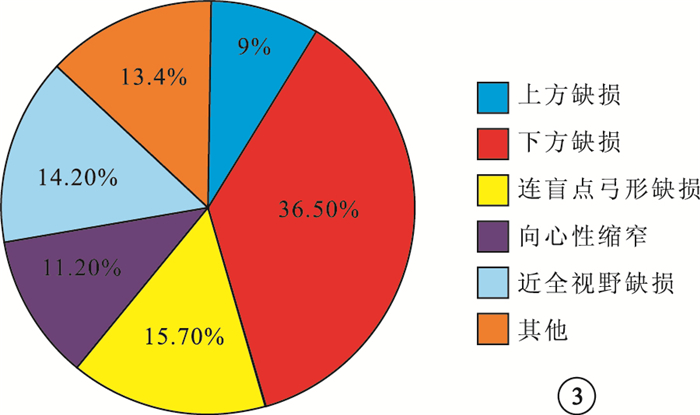 圖3
視野檢查結果
圖3
視野檢查結果
FFA檢查結果顯示,視盤早期弱熒光103只眼,占76.9%;強熒光13只眼;占9.7%;正常熒光18只眼,占13.4%。晚期強熒光110只眼,占82.1%;弱熒光8只眼,占6.0%;正常熒光16只眼,占11.9%。
3 討論
文獻報道NAION發病年齡多在50歲以上[1]。本組患者年齡與文獻報道結果一致。發病年齡較大可能與血管的彈性降低,較易合并高血壓、糖尿病、高血脂等有關。
目前NAION發病機制仍然不清楚,但糖尿病、高血壓、高血脂、心肌梗死、吸煙等為發病的高危因素,其中糖尿病被認為是最危險因素之一[4-6]。國外學者的一項對比研究發現,糖尿病患者NAION的發病率為5%~40%[7]。本組有全身疾病的患者中,伴有糖尿病者39.2%, 在所有危險因素中構成比最高。其原因可能與糖尿病患者長期糖代謝紊亂導致血管內皮細胞損害,小血管血流緩慢,引起毛細血管缺血,進而組織缺血缺氧有關。另外,32.9%的患者伴有高血壓,僅次于糖尿病。本組有糖尿病、高血壓者構成比與無糖尿病、高血壓者構成比差異有統計學意義。提示糖尿病、高血壓是NAION發病的危險因素。Hayreh等[8]研究發現,NAION患者易發生心腦血管疾病,但其納入觀察的病例僅為高血壓、糖尿病患者。國內部分學者認為,全血粘度切變率和血漿粘度升高導致血流阻力增加與NAION發病密切相關[9]。但也有學者認為NAION不是一個獨立的危險因素,不會影響全身并發癥的發生。楊暉等[10]研究發現,NAION患者血脂水平與正常健康者并無統計學意義,高血脂水平不是NAION發病的危險因素。但國外的一項研究結果顯示,一眼發生NAION后,對側眼發病率在5年內較一般人群高15%;糖尿病患者中,另眼發病率則增加20%[11]。這些研究結果說明NAION的發生與心腦血管疾病是否存在相關性尚存在較大爭議,可能存在其他的一些因素。
目前尚無流行病學調查結果顯示NAION發病與季節的相關性。本研究結果顯示,27.6%、24.1%的患者分別在3~4、9~10月發病,占全年發病的一半以上;與其他月份發病率比較,差異有統計學意義。我們推測,此兩個時間段是氣候變化差異較大的春夏及秋冬轉換季節,氣候變化差異較大,引起體內某些因子的代謝水平急劇變化,導致血管收縮、血液動力學的改變以及抗凝機制的異常。文獻報道,腦梗死、心肌梗死等心腦血管疾病的發生與氣溫驟然變化及季節變換存在相關性,而腦梗死、心肌梗死發生的原因主要是高血壓、高血脂[12-14]。王潤生等[15]研究發現,NAION患者血漿內皮素-1濃度顯著高于正常人群。血漿內皮素-1是一種強烈的縮血管物質,我們推測氣候差異變化較大時,血管為適應氣候的變化,應激條件下產生較多的血漿內皮素-1引起血管的收縮可能是這兩個季節發病率較高的原因。當然,更確切的依據,需要更大樣本的進一步研究。
NAION特征性的視野缺損是與生理盲點相連的水平偏盲或垂直偏盲,而非像視路受損后以正中線為界極整齊的偏盲或象限性視野缺損。本研究中,36.5%的患眼下方視野缺損,9.0%的患眼上方視野缺損。楊嘉彬和邱維生[16]報道NAION患眼下方視野缺損為58.34%,而鐘毅敏等[17]的研究結果僅為23.6%。上方、下方視野缺損多與篩板后供應視神經的睫狀后短動脈解剖有關。Olver等[18]認為睫狀后短動脈在篩板后由中間支及側旁支吻合為Zinn-Haller環,環被分為上下兩個部分進入眼內,下方視野缺損較多,表明進入上支的血管較易阻塞,上方視神經纖維易受損。王建民等[19]對一組NAION患眼行FFA檢查,結果發現視盤弱熒光或熒光充盈延遲、缺損區域與視野缺損區域相對應;視盤上方和下方缺血的比例明顯大于鼻側和顳側。說明上方和下方對缺血較為敏感,是上方、下方視野缺損較多的原因。本研究中,76.9%的患眼視盤早期出現弱熒光,82.1%的患眼晚期呈強熒光。結果與文獻報道一致。出現此表現的原因可能與NAION的病程進展以及病理的細微變化有關,提示臨床醫師不能過于依賴單一的輔助檢查結果,作出或排除診斷,需要綜合考慮整個眼部情況。
臨床研究結果顯示,NAION患者杯盤比明顯小于正常人群且多為小視盤,認為當視神經通過視盤和篩板時, 會因空間的狹窄產生擁擠現象, 導致軸漿運輸受阻而發生視盤水腫, 軸索的水腫通過壓迫神經束內小血管和毛細血管, 破壞了動脈的有效灌注,極易誘發NAION [20]。然而,本組患者中小視盤僅5例。其原因可能為,本組小視盤僅為眼底檢查發現明顯小視盤者,而不是將不同大小等級的杯盤比進行對照研究,結果可能會出現誤差。今后我們將對是否合并全身疾病的NAION患者的視盤特征做進一步研究。
非動脈炎性前部缺血性視神經病變(NAION)是50歲以上人群常見的視神經病變[1]。近年來通過對NAION的流行病學,發病危險因素等的研究[2],增進了對這一疾病的認識。目前較為明確的危險因素為糖尿病、高血壓、高血脂、心肌梗死等[3, 4]。但不同季節是否對發病率存在影響目前鮮見報道。為此,我們回顧性分析了一組NAION患者的臨床資料。現將結果報道如下。
1 對象和方法
回顧性病例分析。2004年1月至2014年1月臨床診斷為缺血性視神經病變患者169例中臨床資料完整的NAION患者116例134只眼納入研究。其中,門診患者32例,住院患者84例。患者中男性62例,女性54例;年齡45~75歲,平均年齡(61.2±6.8)歲。所有患者均詳細詢問病史、癥狀,行視力、裂隙燈顯微鏡、間接檢眼鏡、視野、熒光素眼底血管造影(FFA)檢查。同時行血壓、血糖、血脂、頭顱MRI或CT檢查。檢查結果符合NAION診斷標準[5]。排除疑似NAION、臨床資料不完整者。
視野檢查采用Humphry視野計,由熟練技師對患者詳細說明操作要求和注意事項并進行操作中監測。測定范圍為60°以內視野。視野檢查中假陰性、假陽性率均<30%;固視丟失率<20%。FFA檢查采用日本Topcon公司TRC-50EX眼底血管造影儀。
回顧分析年齡、視野、FFA、全身及眼部因素、發病月份與NAION的相關性。發病月份為患者主訴癥狀開始時間。全身合并多個疾病者,在統計危險因素時分別以單個危險因素累積相加,如患者同時患有糖尿病、高血壓,統計時在糖尿病和高血壓危險因素中各增加1例。糖尿病、高血壓患者均是發病前相關科室確診或本次住院確診病例。夜間低血壓來自住院患者病歷記錄。
采用SPSS 13.0統計軟件進行統計學分析處理。各組間比較應用擬合優度的χ2檢驗,P<0.05為差異有統計學意義。
2 結果
116例患者中,55~70歲80例,占68.97%。其中,61~65歲33例,占28.45%(圖 1)。
 圖1
各年齡段患者分布
圖1
各年齡段患者分布
無全身疾病19例,占16.3%。有全身疾病97例,占83.7%。其中,糖尿病38例,占39.2%;高血壓32例,占32.9%,其中伴有夜間低血壓8例,占8.2%;血脂異常28例,占28.9%;腔隙性腦梗死等腦血管疾病16例,占16.5%;冠心病6例,占6.2%;腎病、關節炎、高眼壓、腫瘤等其他疾病12例,占12.4%。眼局部因素中,既往有白內障手術史3例,占所有患者的2.6%;小視盤5例,占所有患者的4.3%(圖 2)。糖尿病、高血壓構成比與無糖尿病、高血壓構成比比較,差異有統計學意義(χ2=362、259,P<0.05)。高血壓、糖尿病可能為NAION的危險因素。
116例患者中,不同月份之間發病有較大差異(圖 2)。3~4、9~10月為發病的高發月份,占全年發病的51.7%。與其他月份發病率比較,差異有統計學意義(χ2=580,P<0.05)。
 圖2
不同發病月份患者分布
圖2
不同發病月份患者分布
視野檢查結果顯示,下方視野缺損49只眼;上方視野缺損12只眼;與生理盲點相連的弓形視野缺損21只眼;向心性視野縮窄15只眼;近全視野缺損19只眼;不規則視野缺損、中心暗點、多象限視野缺損18只眼(圖 3)。
 圖3
視野檢查結果
圖3
視野檢查結果
FFA檢查結果顯示,視盤早期弱熒光103只眼,占76.9%;強熒光13只眼;占9.7%;正常熒光18只眼,占13.4%。晚期強熒光110只眼,占82.1%;弱熒光8只眼,占6.0%;正常熒光16只眼,占11.9%。
3 討論
文獻報道NAION發病年齡多在50歲以上[1]。本組患者年齡與文獻報道結果一致。發病年齡較大可能與血管的彈性降低,較易合并高血壓、糖尿病、高血脂等有關。
目前NAION發病機制仍然不清楚,但糖尿病、高血壓、高血脂、心肌梗死、吸煙等為發病的高危因素,其中糖尿病被認為是最危險因素之一[4-6]。國外學者的一項對比研究發現,糖尿病患者NAION的發病率為5%~40%[7]。本組有全身疾病的患者中,伴有糖尿病者39.2%, 在所有危險因素中構成比最高。其原因可能與糖尿病患者長期糖代謝紊亂導致血管內皮細胞損害,小血管血流緩慢,引起毛細血管缺血,進而組織缺血缺氧有關。另外,32.9%的患者伴有高血壓,僅次于糖尿病。本組有糖尿病、高血壓者構成比與無糖尿病、高血壓者構成比差異有統計學意義。提示糖尿病、高血壓是NAION發病的危險因素。Hayreh等[8]研究發現,NAION患者易發生心腦血管疾病,但其納入觀察的病例僅為高血壓、糖尿病患者。國內部分學者認為,全血粘度切變率和血漿粘度升高導致血流阻力增加與NAION發病密切相關[9]。但也有學者認為NAION不是一個獨立的危險因素,不會影響全身并發癥的發生。楊暉等[10]研究發現,NAION患者血脂水平與正常健康者并無統計學意義,高血脂水平不是NAION發病的危險因素。但國外的一項研究結果顯示,一眼發生NAION后,對側眼發病率在5年內較一般人群高15%;糖尿病患者中,另眼發病率則增加20%[11]。這些研究結果說明NAION的發生與心腦血管疾病是否存在相關性尚存在較大爭議,可能存在其他的一些因素。
目前尚無流行病學調查結果顯示NAION發病與季節的相關性。本研究結果顯示,27.6%、24.1%的患者分別在3~4、9~10月發病,占全年發病的一半以上;與其他月份發病率比較,差異有統計學意義。我們推測,此兩個時間段是氣候變化差異較大的春夏及秋冬轉換季節,氣候變化差異較大,引起體內某些因子的代謝水平急劇變化,導致血管收縮、血液動力學的改變以及抗凝機制的異常。文獻報道,腦梗死、心肌梗死等心腦血管疾病的發生與氣溫驟然變化及季節變換存在相關性,而腦梗死、心肌梗死發生的原因主要是高血壓、高血脂[12-14]。王潤生等[15]研究發現,NAION患者血漿內皮素-1濃度顯著高于正常人群。血漿內皮素-1是一種強烈的縮血管物質,我們推測氣候差異變化較大時,血管為適應氣候的變化,應激條件下產生較多的血漿內皮素-1引起血管的收縮可能是這兩個季節發病率較高的原因。當然,更確切的依據,需要更大樣本的進一步研究。
NAION特征性的視野缺損是與生理盲點相連的水平偏盲或垂直偏盲,而非像視路受損后以正中線為界極整齊的偏盲或象限性視野缺損。本研究中,36.5%的患眼下方視野缺損,9.0%的患眼上方視野缺損。楊嘉彬和邱維生[16]報道NAION患眼下方視野缺損為58.34%,而鐘毅敏等[17]的研究結果僅為23.6%。上方、下方視野缺損多與篩板后供應視神經的睫狀后短動脈解剖有關。Olver等[18]認為睫狀后短動脈在篩板后由中間支及側旁支吻合為Zinn-Haller環,環被分為上下兩個部分進入眼內,下方視野缺損較多,表明進入上支的血管較易阻塞,上方視神經纖維易受損。王建民等[19]對一組NAION患眼行FFA檢查,結果發現視盤弱熒光或熒光充盈延遲、缺損區域與視野缺損區域相對應;視盤上方和下方缺血的比例明顯大于鼻側和顳側。說明上方和下方對缺血較為敏感,是上方、下方視野缺損較多的原因。本研究中,76.9%的患眼視盤早期出現弱熒光,82.1%的患眼晚期呈強熒光。結果與文獻報道一致。出現此表現的原因可能與NAION的病程進展以及病理的細微變化有關,提示臨床醫師不能過于依賴單一的輔助檢查結果,作出或排除診斷,需要綜合考慮整個眼部情況。
臨床研究結果顯示,NAION患者杯盤比明顯小于正常人群且多為小視盤,認為當視神經通過視盤和篩板時, 會因空間的狹窄產生擁擠現象, 導致軸漿運輸受阻而發生視盤水腫, 軸索的水腫通過壓迫神經束內小血管和毛細血管, 破壞了動脈的有效灌注,極易誘發NAION [20]。然而,本組患者中小視盤僅5例。其原因可能為,本組小視盤僅為眼底檢查發現明顯小視盤者,而不是將不同大小等級的杯盤比進行對照研究,結果可能會出現誤差。今后我們將對是否合并全身疾病的NAION患者的視盤特征做進一步研究。