美國加州大學洛杉磯分校 David Geffen 醫學院 Enrique Rozengurt 教授、在自然出版社與川大華西醫院生物治療國家重點實驗室聯合主辦的《Signal Transduction and Targeted Therapy》(STTT)上發表研究綜述,回顧了關于Yes相關蛋白(YAP)在胰腺癌中的相關信號通路的最新知識,分析了176例胰腺導管腺癌患者的基因表達譜和預后,認為YAP信號通路可作為治療胰腺癌的靶點,值得進一步的研究。(https://www.nature.com/articles/s41392-017-0005-2,閱讀原文及下載PDF可直接點擊本文最下方“閱讀原文”)Enrique Rozengurt 教授為本文的第一作者與通訊作者。

胰腺癌被稱為“癌中之王”,其主要的病理類型為胰腺導管腺癌(Pancreatic ductal adenocarcinoma, PDAC),是惡性程度極高的消化道腫瘤。盡管胰腺癌在所有的癌癥中發病率并沒有很高,占3%左右,但患者的5年生存率僅為7%,中位生存期為4-6個月。據估計,2017年這種疾病在美國的發病率會增加到53670例。事實上,由于PDAC導致的死亡預計會急劇增加,使得該疾病成為2030年前美國癌癥相關死亡的第二位主要原因。因此,迫切需要能對PDAC進行治療和預防。
目前對PDAC的研究已經很多,研究發現,KRAS是PDAC中最經常突變的基因(?95%),PDAC中所有錯義KRAS突變的大部分發生在G12位,其中G12D突變最普遍。這些突變阻止KRAS-GTP和KRAS GTPase激活蛋白(GAP)之間的相互作用,從而導致KRAS延長激活并由此激活下游信號效應子,其中最好的顯著的相關信息通路是RAF/MEK/ERK/PI3K/AKT/mTOR通路,KrasG12D突變對PDAC的發生和發展都起著關鍵作用。除此之外,腫瘤抑制基因的突變,如TP53,CDKN2A, SMAD4和/或環境刺激(肥胖,2型糖尿病)都是侵襲性PDAC發生和發展的重要因素。而所有的這些信號通路,都可歸屬于YAP信號通路,在這文中Enrique Rozengurt教授及其同事總結了YAP信號傳導的最新研究,并使用開放獲取數據庫Human Protein Atlas分析176例胰腺導管腺癌患者的基因表達譜和預后,并提出了可能的針對YAP信號網絡的治療策略。
YAP和TAZ(具有PDZ結合基序的轉錄共激活因子)是Hippo腫瘤抑制通路的主要下游靶點(圖1),也受到包括KRAS在內的許多其他蛋白的調節(圖2)。Enrique Rozengurt教授的研究表明,包括YAP(圖3)在內的多個YAP信號網絡的許多蛋白都與PDAC的總體存活率相關(圖4)。事實上,YAP/TAZ/TEAD的多個下游蛋白與PDAC患者的不利生存相關。研究也表明,激活YAP活性的多種成分,包括AP1【與YAP協同增效】、生長因子(TGFα,EPEG和HBEGF),GPCRs(P2Y2R,GPR87),特定整聯蛋白(ITGA2)或Hippo通路抑制劑(MUC1),都與PDAC的不利生存相關(圖4)。與之形成鮮明對比的是,YAP抑制途徑(LKB-1,PKA,TSC)的表達則會有利于胰腺癌的預后。這些數據都說明,YAP信號通路可作為PDAC治療和預防的靶點。
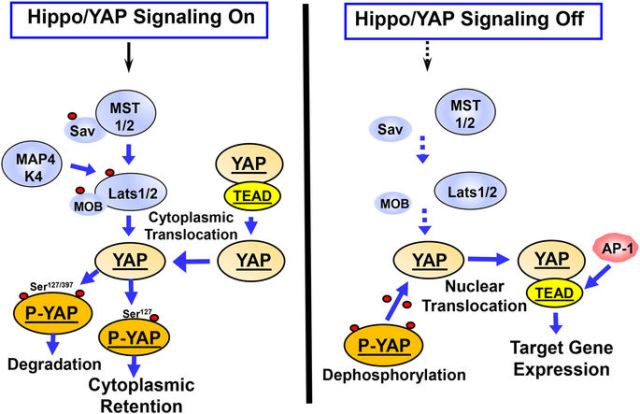
<圖 1 Hippo signaling phosphorylates YAP and regulates its nuclear/cytoplasmic distribution>.
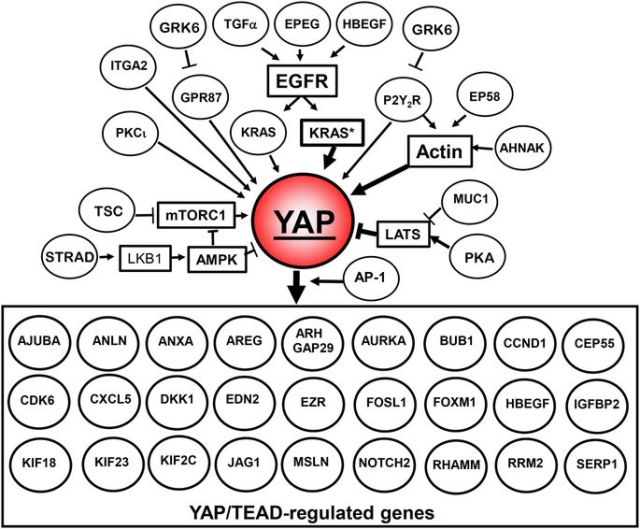
<圖2 YAP is at the epicenter of a signaling network.>
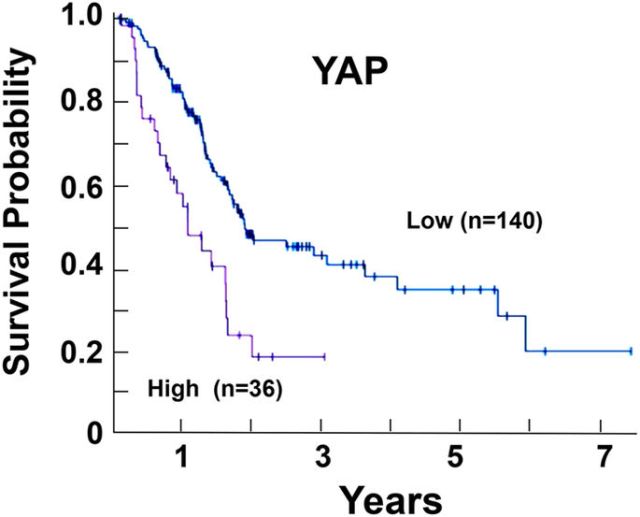
<圖3 Kaplan–Meier plots for YAP expression in PDAC. The image was reproduced from the Human Protein Atlas (version 17).>
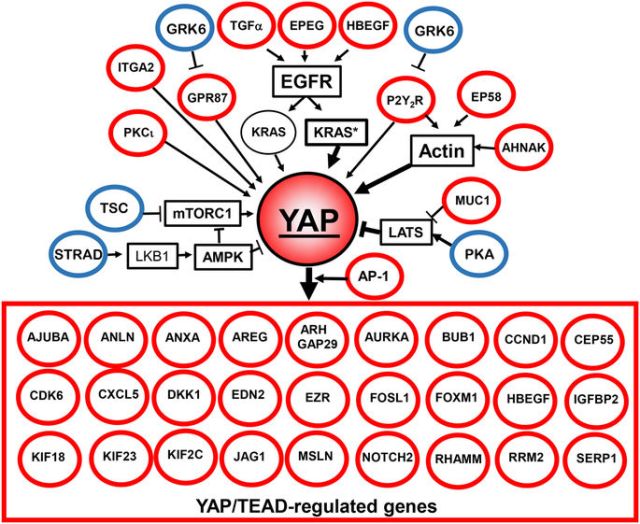
<圖4 YAP signaling is associated with unfavorable prognosis for PDAC.>
例如, EGFR抑制劑作為于YAP通信通路的上游,已有研究表明EGFR抑制劑能對治療PDAC有利,遺憾的是,細胞內有多種替代通路可繞過EGFR激活YAP從而導致耐藥性。他汀類藥物和二甲雙胍通過不同的機制干擾YAP功能,最近的流行病學研究表明它們的使用可以增加PDAC患者的生存率。在YAP的下游,NOTCH通路的抑制劑在臨床前模型中顯示出活性,但因為在晚期PDAC患者中沒有響應而沒有進一步的研究。
由此可見,目前已經有一些經FDA批準并應用于臨床的藥物能影響YAP信號網絡,因此,可以根據YAP信號網絡發現新的治療策略。此外,還可以研發破壞YAP / TEAD和TAZ / TEAD分子復合物的小分子。
參考文獻
(1) Wang, J., Sinnett-Smith, J., Stevens, J. V., Young, S. H. & Rozengurt, E. Biphasic regulation of Yes-associated Protein (YAP) cellular localization, phosphorylation, and activity by G protein-coupled receptor agonists in intestinal epithelial cells: a novel role for protein kinase D (PKD). J. Biol. Chem. 291, 17988–18005 (2016).
(2) Kisfalvi, K., Eibl, G., Sinnett-Smith, J. & Rozengurt, E. Metformin disrupts crosstalk between G protein-coupled receptor and insulin receptor signaling systems and inhibits pancreatic cancer growth. Cancer Res. 69, 6539–6545 (2009).
(3) Rozengurt, E., Sinnett-Smith, J. & Kisfalvi, K. Crosstalk between Insulin/Insulin-like growth factor-1 receptors and G protein-coupled receptor signaling systems: a novel target for the antidiabetic drug metformin in pancreatic cancer. Clin. Cancer Res. 16, 2505–2511 (2010).
(4) Rozengurt, E., Rey, O. & Waldron, R. T. Protein kinase D signaling. J. Biol. Chem. 280, 13205–13208 (2005).
(5) Rozengurt, E. Protein kinase D signaling: multiple biological functions in health and disease. Physiology 26, 23–33 (2011).
(6) Soares, H. P., Ni, Y., Kisfalvi, K., Sinnett-Smith, J. & Rozengurt, E. Different patterns of Akt and ERK feedback activation in response to rapamycin, active-site mTOR inhibitors and metformin in pancreatic cancer cells. PLoS ONE 8, e57289 (2013).
(7) Kisfalvi, K., Moro, A., Sinnett-Smith, J., Eibl, G. & Rozengurt, E. Metformin inhibits the growth of human pancreatic cancer xenografts. Pancreas 42, 781–785 (2013).
(8) Rozengurt, E., Soares, H. P. & Sinnet-Smith, J. Suppression of feedback loops mediated by PI3K/mTOR induces multiple overactivation of compensatory pathways: an unintended consequence leading to drug resistance. Mol. Cancer Ther. 13, 2477–2488 (2014).
Enrique Rozengurt 教授簡介

Enrique Rozengurt教授目前就職于加州大學洛杉磯分校David Geffen醫學院。目前擔任CURE消化疾病研究中心主任。目前已經在Cell, PNAS,Cancer Research等國際著名期刊上發表論文130余篇。Enrique Rozengurt教授致力于研究消化道腫瘤發生發展的信號通路。
Signal Transduction and Targeted Therapy簡介
《Signal Transduction and Targeted Therapy》(STTT)是自然出版集團和四川大學華西醫院生物治療國家重點實驗室合作出版的全英文生物醫學專業期刊(網站:http://www.nature. com/sigtrans,點擊本網站最下方"閱讀原文”)。主編由美國俄亥俄州立大學Carlo M. Croce教授(美國三院院士,Cancer Research前主編),UCSD的張康教授、川大華西醫院魏于全教授/院士擔任。有來自全球等多個國家及地區的多位相關領域的近百位著名學者組成編委會。本雜志每周五發表文章,歡迎各位投稿,包括論著或綜述。對于原創性成果采取“快速通道”模式,幫助作者以最快的速度發表文章,最快一周可接收。該雜志發表論文可免收發表費。該雜志投稿格式不限,正式發表之前再按雜志格式修改。感謝將此信息轉發給您們的同事、朋友以及學生等。
Cite this article
Enrique Rozengurt, James Sinnett-Smith & Guido Eibl,Yes-associated protein (YAP) in pancreatic cancer: at the epicenter of a targetable signaling network associated with patient survival. Signal Transduction and Targeted Therapyvolume 3, Article number: 11 (2018). doi:10.1038/s41392-017-0005-2
點擊“閱讀原文”可查看原文并免費下載PDF