國際知名免疫學家,誘導性調節T細胞的主要發現者鄭頌國教授和國際關節炎研究的先鋒之一David Brand教授聯合課題組在自然出版社與川大華西醫院生物治療國家重點實驗室聯合主辦的《Signal Transduction and Targeted Therapy》(STTT)上發表專家述評,在分析白介素2(IL-2)的生物學特性及其對調節性T細胞(Treg)作用機制的基礎上,總結目前使用低劑量IL-2治療的自身免疫疾病的臨床研究作用及機制,提出在優化IL-2安全劑量和與其他細胞因子復合物的聯合作用方面需要進行更深入的研究。博士研究生葉聰秀為第一作者。

調節性T細胞(Treg)在維持機體免疫平衡中起重要作用,尤其是自身免疫疾病。白介素2(IL-2),一種可溶性細胞因子,主要通過與三種高親和力的受體(CD25,CD122和CD132)結合發揮作用。鄭頌國教授課題組及其他課題組近年來研究發現IL-2在Treg細胞分化、增殖及功能維持方面有重要作用,有可能成為新的治療自身免疫性疾病的手段。其中鄭頌國課題組在國際上首先報道IL-2信號途徑在誘導調節T細胞的分化和穩定性中有獨特價值(參考文獻1),之后國際Treg著名學者Eathan Shevach課題組立即證實了這個發現(參考文獻2)。這些成果對低劑量IL-2通過促進Treg來治療各種自身免疫性疾病奠定了一定的理論基礎。
本文對IL-2的生物學特性及其對調節性T細胞(Treg)作用機制、目前使用低劑量IL-2治療的自身免疫疾病的臨床研究進行了系統述評,使讀者對IL-2的作用有一個新的認識:高劑量作用于效應T細胞用于腫瘤的治療,低劑量作用于Treg用于自身免疫疾病的治療。
文章也展示IL-2與其受體結合方式及其下游的信號通路。IL-2通過與其受體CD25、CD122和CD132結合形成三聚體后,使 JAK1和JAK3其磷酸化,激活下游的三條信號通路:1)STAT5s信號通路,2)Ras–Raf-MAPK信號通路和3)PI3K信號通路(見圖1)。。
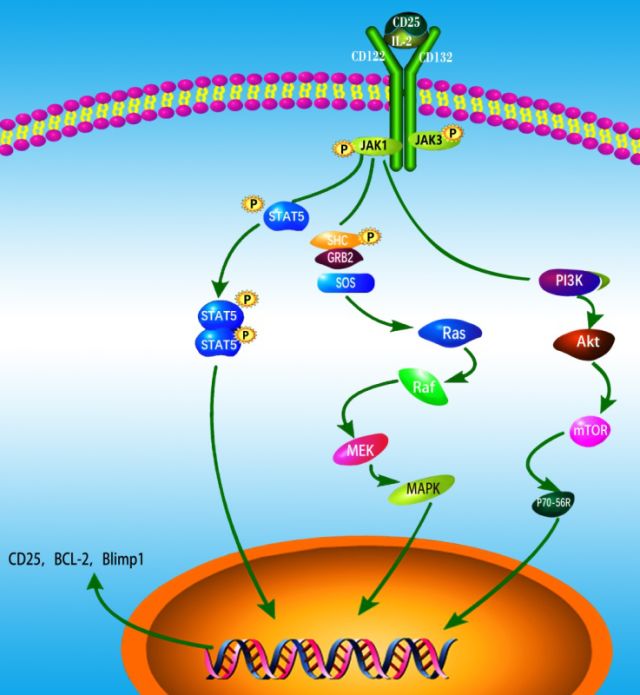
<圖1 IL-2 binding to IL-2 receptors (IL-2Rs) and
its downstream signaling.>
之后,描述了IL-2信號對胸腺及外周Treg的主要作用特征。在胸腺內,幼稚性CD4細胞短暫表達CD25,IL-2通過與CD25結合激活STAT5s信號通路,上調CD4細胞中CD25 和Foxp3的表達,使其分化為成熟的CD4 調節T細胞。成熟的Treg從胸腺遷移至外周,并持續表達CD25,分化為激活的CD4 Treg并發揮其免疫調節作用。IL-2也能刺激CD8 T細胞,使其成為激活的CD8 Treg,但是具體機制目前尚不明確(見圖2)。
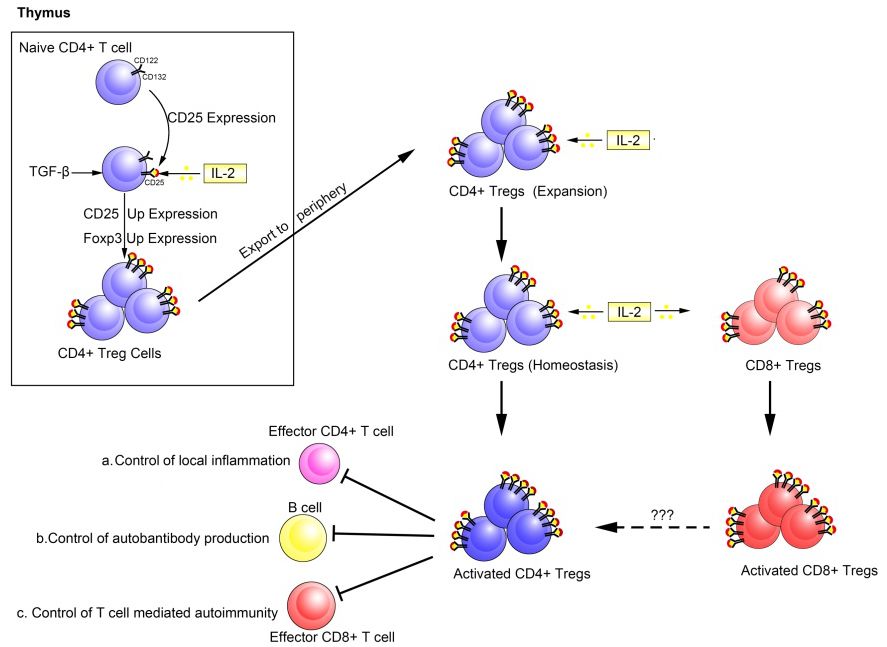
<圖2 Main role of IL-2 signal in thymus and
peripheral Tregs.>
最后,文章總結近年來報道的使用IL-2治療幾種自身免疫疾病的動物模型研究和臨床研究,發現低劑量IL-2確實能通過增加Treg數量、增強其免疫抑制功能的機制,發揮治療免疫性疾病的作用,同時具有更好的安全性。這些免疫性疾病包括造血干細胞移植后(HSCT)的治療、1型糖尿病(T1D)、GVHD的預防和治療、斑禿、系統性紅斑狼瘡(SLE)。同時提出設想,低劑量IL-2對其他自身免疫疾病,如類風濕關節炎(RA)可能具有同樣的治療作用。但是,在優化IL-2安全劑量和與其他細胞因子復合物的聯合作用方面還需要進行更深入的研究。。
參考文獻
(1)Yitian Cai, Seng Yin Kelly Wee, Junjie Chen, Boon Heng Dennis Teo, Yee Leng Carol Ng, Khai Pang Leong and Jinhua Lu. Broad Susceptibility of Nucleolar Proteins and Autoantigens to Complement C1 Protease Degradation. J Immunol. October 25, 2017, ji1700728; DOI: https://doi. org/10.4049/jimmunol.1700728
(2)Daphne Palacios-Macapagal, Jane Connor, Tomas Mustelin, Thirumalai R. Ramalingam, Thomas A. Wynn and Todd S. Davidson. Cutting Edge: Eosinophils Undergo Caspase-1–Mediated Pyroptosis in Response to Necrotic Liver Cells. J Immunol. June 26, 2017, ji1601162; DOI: https: //doi.org/10.4049/jimmunol.1601162
鄭頌國 教授簡介

鄭頌國教授, 中山大學教授,美國賓夕法尼亞州立大學(PSU)終身正教授,自身免疫性疾病研究中心主任。長期從事免疫調節T細胞的誘導,發育和維持機制的研究,是國際上發明TGF-β誘導調節T細胞工作的領導科學家,誘導性調節T細胞的主要奠基人,SCI論文超過100多篇,他人引用超過7000多次。
David Brand 教授簡介

David Brand教授目前任職美國田納西大學,主要從事免疫方面的研究,CIA模型的國際先鋒,發表SCI論文80余篇。
Signal Transduction and Targeted Therapy簡介
《Signal Transduction and Targeted Therapy》(STTT)是自然出版集團和四川大學華西醫院生物治療國家重點實驗室合作出版的全英文生物醫學專業期刊(網站:http://www.nature. com/sigtrans,點擊本網站最下方"閱讀原文”)。主編由美國俄亥俄州立大學Carlo M. Croce教授(美國三院院士,Cancer Research前主編),UCSD的張康教授、川大華西醫院魏于全教授/院士擔任。有來自全球等多個國家及地區的多位相關領域的近百位著名學者組成編委會。本雜志每周五發表文章,歡迎各位投稿,包括論著或綜述。對于原創性成果采取“快速通道”模式,幫助作者以最快的速度發表文章,最快一周可接收。該雜志發表論文可免收發表費。該雜志投稿格式不限,正式發表之前再按雜志格式修改。感謝將此信息轉發給您們的同事、朋友以及學生等。
Cite this article
Congxiu Ye, David Brand2, Song G Zheng. Targeting IL-2: an unexpected effect in treating immunological diseases. Signal Transduct Target Ther 3. Jan 19, 3, 2 (2018). doi:10. 1038/s41392-017-0001-5.
點擊“閱讀原文”可查看原文并免費下載PDF