中國醫學科學院納米生物醫學聯合研究中心許海燕教授和王琛教授在在自然出版社與川大華西醫院生物治療國家重點實驗室聯合主辦的《Signal Transduction and Targeted Therapy》(STTT)上發表論文,化學合成CXCR4拮抗多肽克服乳腺癌細胞耐藥和抑制腫瘤血管形成。該文的通訊作者為許海燕教授和王琛教授,第一 作者為郭華博士。

CXCR4是趨化受體家族的重要成員之一,在數十種人類腫瘤細胞中高表達,其配體CXCL12主要由存在于骨髓、脾臟、肺臟中的基質細胞所分泌。實體腫瘤組織中也存在大量基質細胞,腫瘤細胞通過與基質細胞粘附而抵抗化療藥物的殺傷;同時,基質細胞通過分泌CXCL12從外周循環招募內皮祖細胞進入腫瘤組織,促進血管形成和介導腫瘤細胞的轉移。
中國醫學科學院基礎醫學研究所許海燕實驗室和國家納米科學中心王琛實驗室合作研發了一種化學合成的新型CXCR4拮抗多肽(E5);并已在急性髓系白血病動物模型上證明了E5可有效抑制白血病細胞對CXCL12的響應,顯著提高了白血病細胞對多種化療藥的敏感性,延長了白血病小鼠的生存時間[參考文獻1,2]。本研究的目的是探明E5能否應用于實體腫瘤的治療。
研究結果表明, E5能與表達CXCR4的小鼠乳腺癌細胞4T1和原代人臍靜脈血管內皮細胞HUVEC細胞特異性結合(圖1);在較高濃度下,通過誘導細胞凋亡對4T1細胞產生殺傷作用(圖2)。
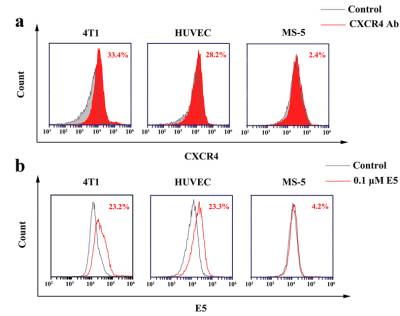
<圖1. E5 had high affinity towards 4T1 cells and HUVECs (b) which had high levels of CXCR4 expression (a).>
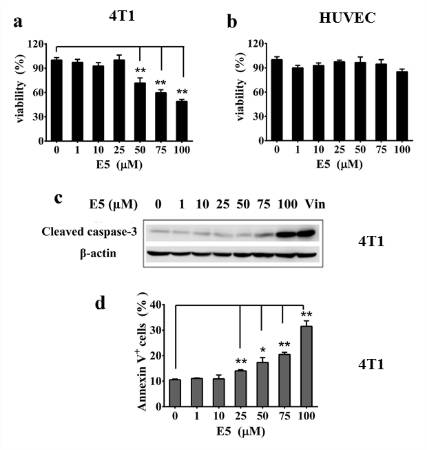
<圖2. E5 is cytotoxic to 4T1 cells in a concentration-dependent manner.>
尤其重要的是,E5能夠在較低濃度下有效抑制4T1和HUVEC細胞對CXCL12和基質細胞介導的遷移與粘附的響應能力(圖3);克服基質細胞對腫瘤細胞的保護作用,顯著提高腫瘤細胞對多種化療藥物的敏感性(圖4)。
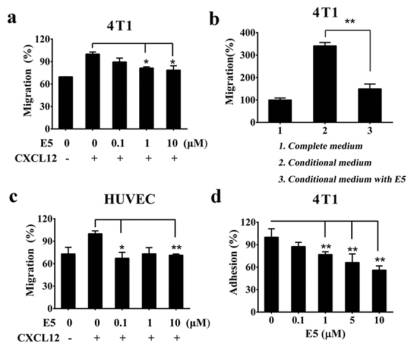
<圖3. E5 inhibited the migration of 4T1 cells or HUVECs
induced by CXCL12 (a, b, c) and the adhesion of
4T1 cells to MS-5 cells (d).>
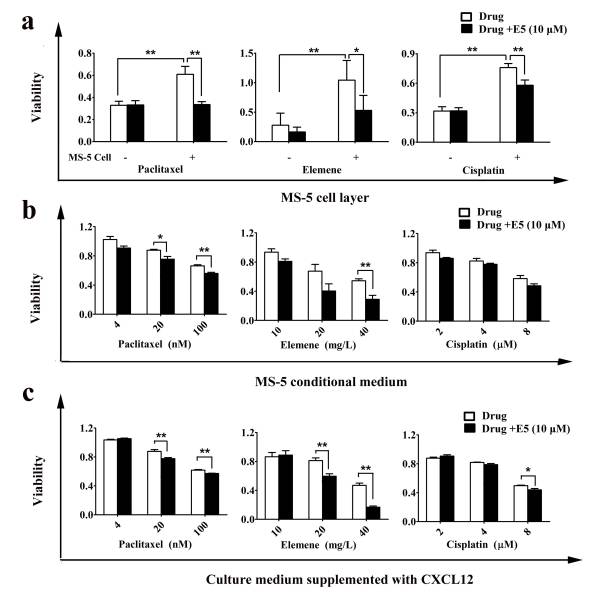
<圖4. E5 enhanced the sensitivity of 4T1 cells to different >
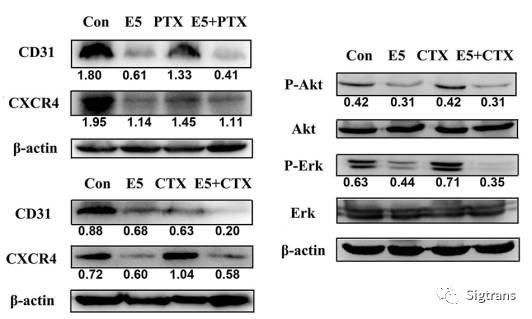
在乳腺癌小鼠模型上,E5與低劑量紫三醇或長春新堿聯合應用時,通過拮抗CXCR4進而下調Akt和Erk的磷酸化,并抑制腫瘤血管的生成,使化療效果得到顯著提升(圖5和圖6)。與此同時,在體內穩定性方面E5具有明顯優勢,其半衰期約為10 h,遠遠長于現有CXCR4拮抗分子(圖7)。
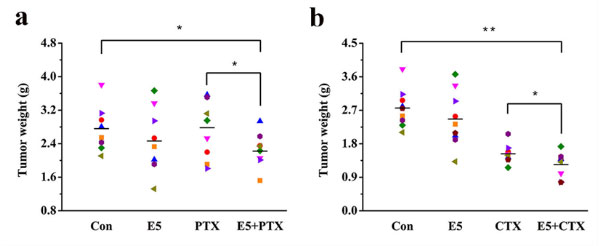
<圖5. E5 in combination with chemotherapeutic drugs PTX or CTX inhibited tumor growth in a breast cancer model.>
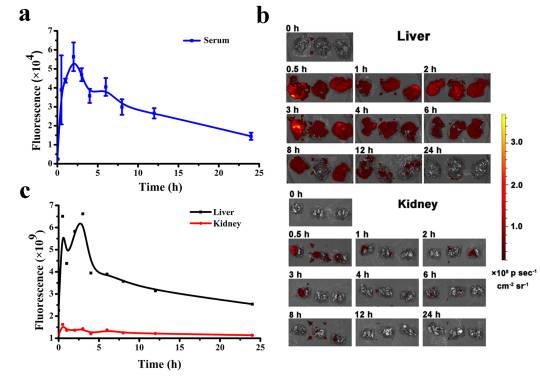
<圖7. E5 had good in vivo stability.>
綜上,E5通過干擾CXCR4/CXCL12生物軸而提高腫瘤細胞對化學藥物的敏感性,顯示出其在實體腫瘤治療方面的轉化價值與臨床應用前景。
參考文獻:
(1)Li X, Guo H, Yang Y, Meng J, Liu J, Wang C et al. A designed peptide targeting CXCR4 displays anti-acute myelocytic leukemia activity in vitro and in vivo. Sci Rep 2014; 4: 6610.
(2)Li X, Guo H, Duan H, Yang Y, Meng J, Liu J et al. Improving chemotherapeutic efficiency in acute myeloid leukemia treatments by chemically synthesized peptide interfering with CXCR4/CXCL12 axis. Sci Rep 2015; 5: 16228.
許海燕教授簡介

許海燕教授,中國醫學科學院納米生物醫學聯合研究中心主任及基礎醫學研究所生物醫學工程系主任。研究方向之一為基于納米技術的抗腫瘤藥物研發,涉及多種白血病耐藥相關蛋白的拮抗多肽篩選及分子機制,以及天然藥物與免疫佐劑的納米新劑型等研究;此外,應用納米材料的特性設計功能支架,調控創傷免疫微環境和引導組織再生。
個人主頁:http://zhaosheng.sbm.pumc.edu.cn/viewname. asp?/1644.html
王琛教授簡介

王琛教授,國家納米科學中心研究員,研究方向為生物體系中分子納米結構及其效應,闡釋了小分子和短肽等對淀粉樣多肽組裝結構與過程的調控規律;發現了淀粉樣多肽與單個染料標記分子的互作模式,確定了單個標記分子在β淀粉樣多肽和朊病毒多肽片段等序列上的作用位點;利用SPM技術揭示了發卡型結構中折疊位點的多重性。
個人主頁:http://sourcedb.cas.cn/sourcedb_nanoctr_cas /zw/ zxrck/200906/t20090602_252691.html
Signal Transduction and Targeted Therapy簡介
《Signal Transduction and Targeted Therapy》(STTT)是自然出版集團和四川大學華西醫院生物治療國家重點實驗室合作出版的全英文生物醫學專業期刊(網站:http://www.nature. com/sigtrans,點擊本網站最下方"閱讀原文”)。主編由美國俄亥俄州立大學Carlo M. Croce教授(美國三院院士,Cancer Research前主編),UCSD的張康教授、川大華西醫院魏于全教授/院士擔任。有來自全球等多個國家及地區的多位相關領域的近百位著名學者組成編委會。本雜志每周五發表文章,歡迎各位投稿,包括論著或綜述。對于原創性成果采取“快速通道”模式,幫助作者以最快的速度發表文章,最快一周可接收。該雜志發表論文可免收發表費。該雜志投稿格式不限,正式發表之前再按雜志格式修改。感謝將此信息轉發給您們的同事、朋友以及學生等。
實驗室網站:http://labs.wpi.edu/dempskilab/
Cite this article
Hua Guo, Yangyang Ge, Xiaojin Li, Yanlian Yang, Jie Meng, Jian Liu, Chen Wang & Haiyan Xu.Targeting the CXCR4/CXCL12 axis with the peptide antagonist E5 to inhibit breast tumor progression. Signal Transduction and Targeted Therapy (2017) 2, e17033; doi:10.1038/sigtrans. 2017.33
點擊“閱讀原文”可查看原文并免費下載PDF