冠狀動脈旁路移植術(coronary artery bypass grafting,CABG)是治療冠狀動脈粥樣硬化性心臟病(冠心病)的常用外科手段,與傳統的體外循環下CABG(on-pump coronary artery bypass grafting,ONCAB)相比,非體外循環下CABG(off-pump coronary artery bypass grafting,OPCABG)能夠降低全身系統性炎癥反應、減少主動脈插管及主動脈壁鉗夾過程中血管壁斑塊脫落等不良事件,從而降低患者的手術風險及術后并發癥發生率等[1],尤其是對高風險冠心病患者受益更多。術后心房顫動(postoperative atrial fibrillation,POAF)是OPCABG的常見并發癥之一,發生率為12%~40%,常見于術后2~4 d,第2 d是高峰期[2],可能引發患者腦卒中、出血、感染、腎衰竭、心臟驟停等,不但會延長患者住院時間,延緩康復進程,增加醫療費用[3],甚至導致術后30 d和6個月死亡率上升2倍[4]。雖然各學會已制訂POAF相關診療共識、意見[5],但在過去十幾年中POAF發病率并無明顯降低[4, 6]。因此,POAF的預防和管理成為亟待解決的問題。近年來有不少學者對POAF的預測因素進行研究,但各研究間納入分析危險因素和結果存在差異,且無全面綜合總結OPCABG患者發生POAF危險因素的系統評價。本研究通過對相關研究結果進行Meta分析,明確OPCABG患者發生POAF的危險因素,以期為臨床制訂預防、管理OPCABG患者發生POAF的策略提供依據。
1 資料與方法
1.1 納入和排除標準
納入標準:(1)研究類型:已公開發表的觀察性研究;(2)研究對象:確診為冠心病且行OPCABG的患者,不限國籍、種族;(3)暴露因素:與OPCABG患者新發POAF相關的患者基本情況、術前疾病情況、術前用藥情況、術中因素和術后因素,有≥2項研究報告的暴露因素即納入Meta分析;(4)結局指標:OPCABG新發POAF[7-9]的危險因素。排除標準:(1)無明確OPCABG后POAF診斷標準;(2)未排除術前合并房顫患者。(3)非中文或英文文獻;(4)無法提取數據或數據重復的文獻;(5)重復發表的文獻。
1.2 文獻檢索策略
于2022年9月,計算機檢索PubMed、EMbase、Web of Science、The Cochrane Library、中國知網、萬方數據知識服務平臺、維普網(VIP)、中國生物醫學信息數據庫(SinoMed)。檢索時間范圍為建庫至2022年9月。采用主題詞、自由詞相結合的方式。中文檢索詞包括:冠狀動脈旁路移植術、冠狀動脈搭橋術、冠脈旁路移植、冠脈搭橋術、非體外循環、不停跳、心房顫動、房顫、心房纖顫、危險因素、風險因素等;英文檢索詞為:coronary artery bypass,off pump/beating heart coronary artery bypass,atrial fibrillation/auricular fibrillation*/fibrillation*,atrial/POAF,risk factors/risk factor/risk predictor等。
1.3 文獻篩選與資料提取
由2位研究者(第1作者和第2作者)獨立篩選文獻、提取相關資料,再交叉核對,如存爭議,雙方討論或請第3位研究者(第3作者)仲裁。文獻篩選過程中,先用NoteExpress篩出重復文獻,閱讀文獻題目及摘要,選出初步符合納入標準的文獻(初篩);再通讀全文,根據納入和排除標準,確定最終納入分析的文獻(復篩);提取資料包括:作者、發表年份、地區、研究類型、樣本量、年齡、新發房顫發生率、暴露因素及結局測量相關數據。
1.4 納入研究的質量評價
病例對照研究及隊列研究使用紐卡斯爾-渥太華量表(Newcastle-Ottawa scale,NOS)評分[10],共8個條目,滿分為9分,≥7分為高質量研究。2名研究者(第1作者、第2作者)獨立進行文獻質量評價,均接受過系統的循證課程培訓。若2位研究者評分出現爭議由第3位研究者(第3作者,省級循證護理師)仲裁。
1.5 統計學分析
采用Stata12.0、RevMan 5.4軟件對數據進行分析。計數資料選擇比值比(odds ratio,OR)為效應指標,計量資料用加權均數差或標準化均屬差為效應指標,采用95%可信區間。若異質性檢驗P≥0.1,I2≤50%,表明研究具有同質性,采用固定效應模型;若I2≥50%,提示研究有異質性,采用隨機效應模型,通過敏感性分析或亞組分析尋找異質性來源,若異質性仍較大則進行描述性分析。采用Egger’s檢驗及漏斗圖對文章進行發表偏依分析。P≤0.05為差異有統計學意義。
1.6 研究注冊
本研究在英國國立衛生研究院(National Institute for Health Research,NIHR)PROSPERO數據庫注冊,注冊編號為:CRD42022364737。
2 結果
2.1 文獻檢索結果
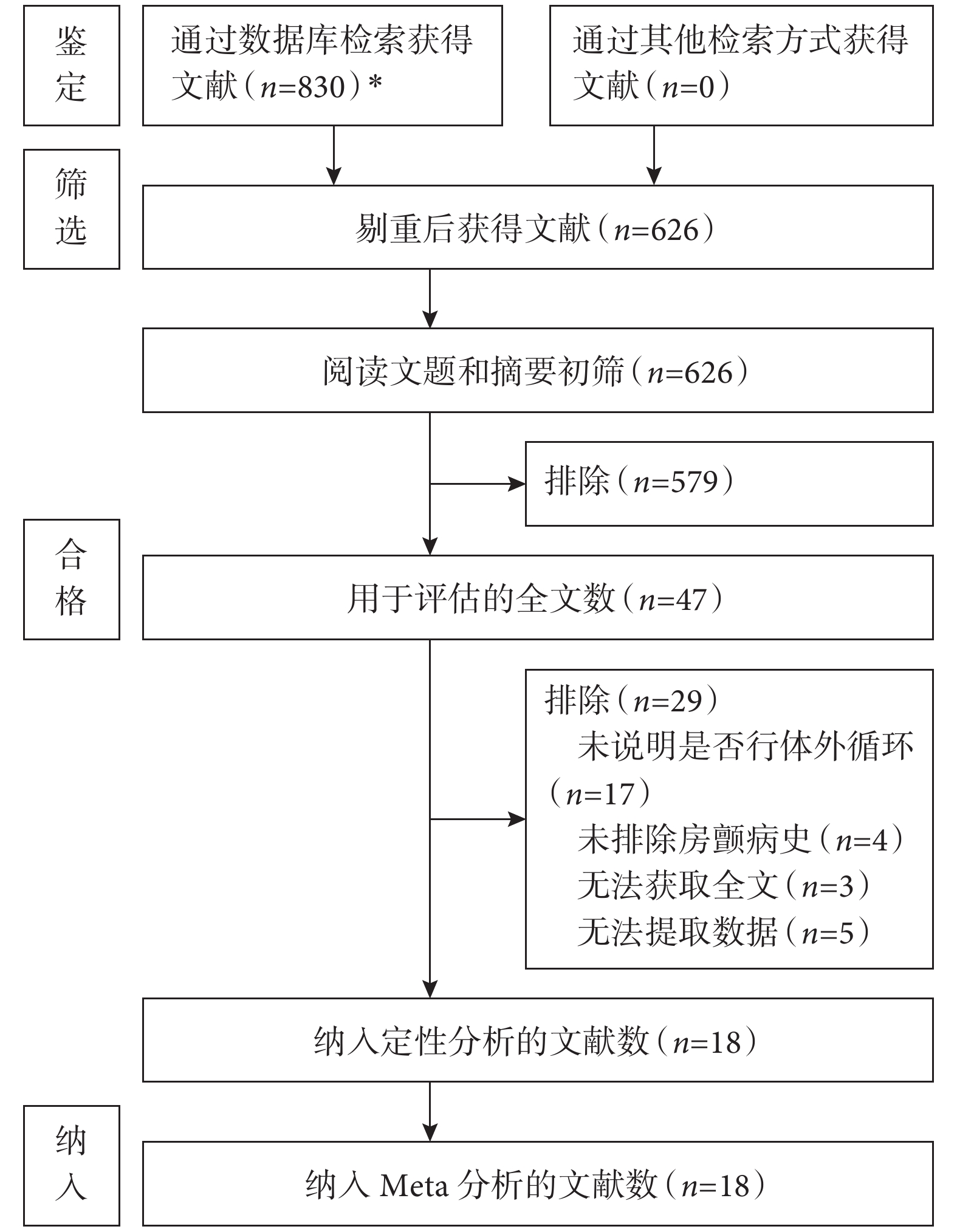
根據文獻檢索策略共檢索出OPCABG術后新發POAF危險因素相關文獻830篇,進行文獻篩選后初步納入47篇文獻進行全文閱讀,最終納入18篇文獻[1-3, 8, 11-25];見圖1。納入研究均為病例對照研究,共6 354例OPCABG患者,POAF患者1 393例,非POAF患者4 961例,納入31項暴露因素。納入研究的NOS評分為6~8分;見表1。
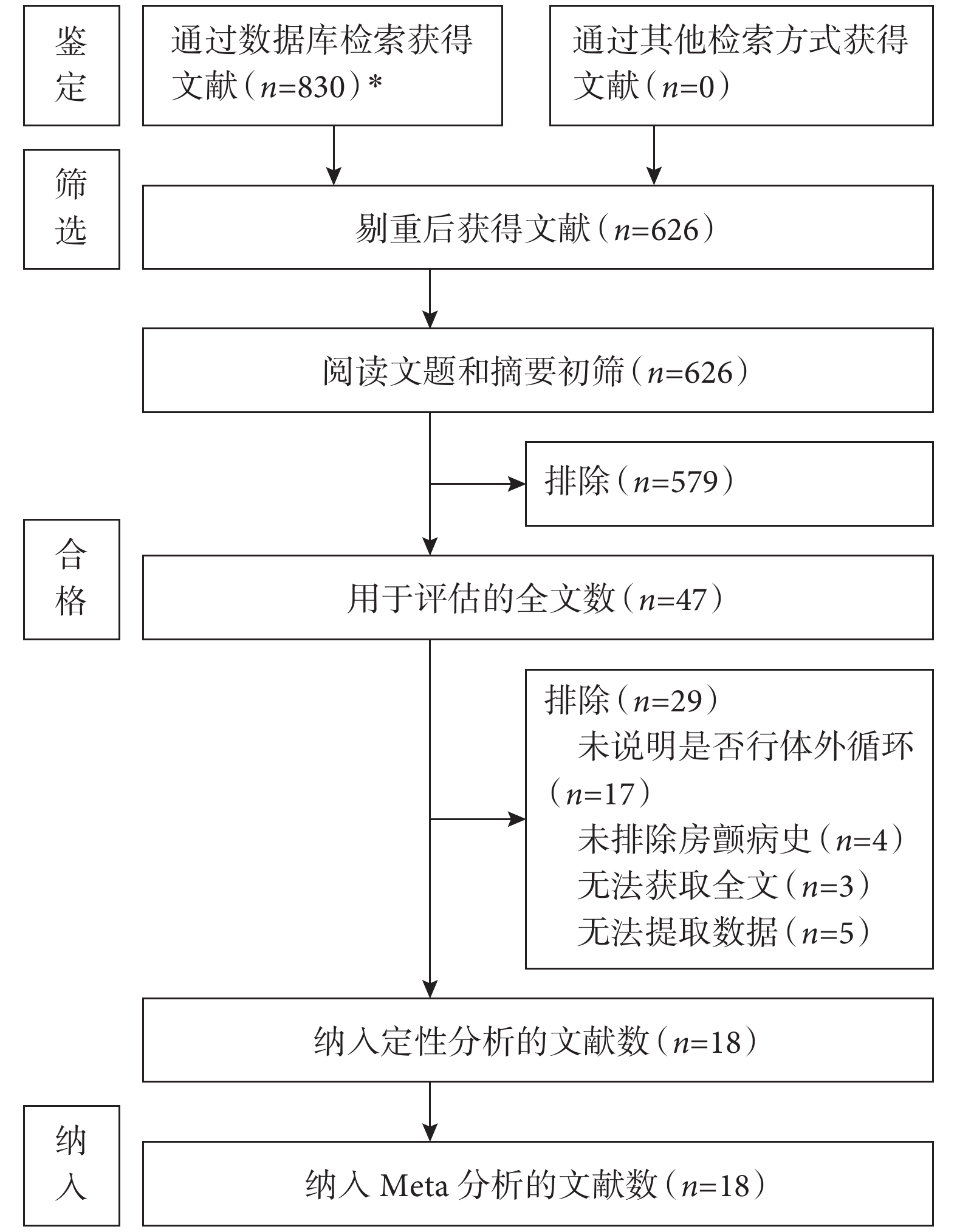 圖1
文獻檢索流程圖
圖1
文獻檢索流程圖
*所檢索數據庫的文獻數具體如下:CNKI(
2.2 Meta分析結果
2.2.1 患者自身因素
納入研究包括的患者自身因素有年齡、性別、體重指數(body mass index,BMI)、吸煙史、飲酒史、EuroSCOREⅡ評分、高血壓病史、糖尿病病史、心肌梗死病史、頻發房性早搏(房早)或房性心動過速(房速)、腎功能不全、高脂血癥、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)、腦血管病史。Meta分析結果顯示年齡、高血壓、EuroSCOREⅡ評分、頻發房早是OPCABG患者新發POAF的危險因素。性別、BMI、吸煙史、飲酒史、糖尿病史、腦血管病史、心肌梗死病史、腎功能不全、高脂血癥、COPD與OPCABG患者新發POAF無關;見表2。
2.2.2 術前因素
納入研究包括的術前因素包括C反應蛋白(C-reactiveprotein,CRP)、肌酐、總膽固醇、甘油三酯、低密度脂蛋白、左房內徑(left atrium diameter,LAD)、左室射血分數(left ventricular ejection fraction,LVEF)、合并右冠狀動脈狹窄、冠狀動脈三支病變、左主干病變、β受體阻滯劑、他汀類藥物、血管緊張素轉化酶抑制劑/血管緊張素受體拮抗劑。Meta分析結果顯示LAD、LVEF、合并右冠脈狹窄、冠狀動脈三支病變、未使用β受體阻滯劑是OPCABG患者新發POAF的術前危險因素。術前CRP、肌酐、總膽固醇、甘油三酯、低密度脂蛋白、左主干病變、使用他汀類藥物、使用血管緊張素轉化酶抑制劑/血管緊張素受體拮抗劑與OPCABG患者新發POAF無關;見表2。
2.2.3 術中因素
納入研究包括的術中因素包括旁路血管支數、手術時間。Meta分析結果顯示手術時間是OPCABG患者新發POAF的術中危險因素;旁路血管支數與OPCABG患者新發POAF無關;見表2。
2.2.4 術后因素
納入研究包括的術后因素包括術后NLR、機械通氣時間。Meta分析結果顯示、機械通氣時間[OR=2.85,95%CI(1.79,3.91),P<0.001]是OPCABG患者新發POAF的術后危險因素。術后NLR[OR=1.52,95%CI(-1.10,4.14),P=0.13]與OPCABG患者新發POAF無關;見表2。
2.2.5 敏感性分析
通過轉換隨機效應模型和固定效應模型進行敏感性分析。計算12項危險因素的合并OR值、95%CI,結果未見明顯改變,表明該部分結果穩定性較好、可信度高;見表3。
2.2.6 發表偏倚
采用Stata15.0進行Egger's檢驗進行發表偏倚分析。結果顯示,年齡(P=0.086)、性別(P=0.075)、吸煙史(P=0.325)、糖尿病(P=0.519)、LAD(P=0.574)、LVEF(P=0.314)、β受體阻滯劑(P=0.782)無明顯發表偏倚。。
3 討論
OPCABG是治療冠心病常用的手術方式,研究表明其能有效避免ONCAB因體外循環引發的全身炎癥反應、心肌缺血再灌注,一定程度上減少誘發心房顫動等不良事件[1]。但有學者[26-27]報道,盡管使用OPCABG,POAF仍有較高的發生率,而本研究同樣顯示發生率為12.5%~32.8%,處于較高水平。由此說明,可能存在除體外循環以外其他導致患者新發POAF的影響因素。盡管OPCABG術后新發POAF并不是發生持續AF的先兆,通常使用抗心律失常藥物或電復律后可恢復為竇性心律,普通患者可耐受,但對于心功能下降及冠心病高發的老年患者,術后早期心律失常會造成患者血流動力學不穩定、降低心排出量,增加患者卒中的風險,因此識別其危險因素至關重要。
3.1 患者自身因素
本Meta分析結果顯示,OPCABG患者新發POAF的患者自身影響因素有:(1)年齡是OPCABG患者新發POAF的重要危險因素。本研究結果顯示,年齡每增加1歲,患者POAF發生率增加近3倍,與既往研究結果相同。Mathew等[28]的研究表明,年齡每增加10歲,AF發生率增加75%,且年齡>70歲是POAF的高危因素,當年齡>72歲時,POAF發生率約為<55歲患者的4.4倍[19]。其潛在機制可能為:人體衰老過程中出現心功能進行性下降、心室重構、心肌細胞減少、剩余心肌細胞過度肥大、心肌纖維化等變化[2, 11],引起心內傳導系統紊亂并導致異常的折返通路[3],進而引發AF。雖然年齡是不可干預因素,醫護人員應加強對高齡OPCABG患者的術前預防,術中管理及術后觀察,形成老年患者規范化重點管理流程。(2)高血壓是OPCABG患者新發POAF的重要危險因素之一。本研究表明合并高血壓的患者發生POAF風險增加2倍,與既往研究[3, 12]結果相同。從病理生理角度分析:高血壓導致左心室順應性下降、舒張功能障礙、左室肥大,進而使左室充盈壓升高,冠脈血流灌注減少,刺激交感神經,激活腎素-血管緊張素-醛固酮系統(RAAS)[3, 11]。另外,兒茶酚胺分泌增多、神經內分泌紊亂、循環血容量失調和炎性反應增強均可導致心肌電活動不穩定,導致AF[13]。因此對于有高血壓的患者應提前進行干預,控制血壓在合適范圍。(3)頻發房顫和房早與OPCABG患者新發POAF存在相關性。頻發房顫和房早患者POAF風險增加3.7倍,可能與心房組織纖維化,激活RAAS系統有關,和高血壓引發POAF機制相似。盡早糾正房顫及房早在預防OPCABG患者新發POAF中至關重要。(4)EuroSCOREⅡ是預測心血管外科圍手術期風險的重要方式,分數高的患者可能在術后發生嚴重的炎癥反應,進而導致POAF的發生[29]。綜上所述,患者自身狀況是POAF不可忽略的重要因素,冠狀動脈旁路移植術后相關指南[30]指出,術前應對患者基本情況、心血管危險因素等做全面評估,盡早發現患者自身危險因素,積極干預,全面觀察,同時給予社會支持,緩解焦慮情緒引起的神經系統異常反應。
3.2 術前因素
Meta分析結果表明,術前危險因素有:(1)術前LAD增大、EF降低是OPCABG患者新發POAF的預測因素,原因可能是:心室重構或心肌纖維化,引起早期復極縮短、晚期復極延長、增加興奮性,引發心律失常,心律失常進而加重心房重構,進而引發POAF[31-33];兩項Meta分析結果顯示[34-35],EF降低與冠狀動脈旁路移植術后急性腎損傷、低氧血癥相關。因此應加強對EF降低患者的管理,降低術后相關并發癥。(2)右冠狀動脈狹窄可能導致竇房結動脈血流中斷、減少,進而導致竇房結缺血,房內傳導延遲,誘發POAF,右冠狀動脈作為OPGCABG患者新發POAF危險因素的研究有限,納入總樣本量較少,需要更多大樣本量的研究予以證實[2]。(3)冠狀動脈三支病變通常意味著患者病情較重,Lokshyn等的1項納入3340例冠脈造影患者的研究表明,在房顫組(30.5%)中,三支病變的發生率明顯高于竇性心律組(20.4%)。(3)OPCABG患者新發POAF受術前是否服用β受體阻滯劑影響。β受體阻滯劑作為第二類抗心律失常藥物,多篇指南[5, 36-38]將β受體阻滯劑作為CABG術前預防性用藥列入一級推薦。有研究[21, 39]認為,術后使用β受體阻滯劑可降低POAF的發生率,而術前使用繼而術后停藥使POAF發病率增加91%。對于擬行OPCABG的患者,無論是否急診手術,在時間允許的情況下,建議常規行心臟超聲檢查,以識別高危患者。圍手術期可使用β受體阻滯劑預防POAF的發生,術前使用者不建議術后立即停藥,應在患者病情穩定后循序漸進撤藥。
3.3 術中因素
對于術中相關參數,本研究發現手術時間長是OPCABG患者新發POAF的危險因素之一。OPCABG手術時間較長患者較短時間患者發生POAF的風險更高。可能是手術引發交感神經興奮,加之手術牽拉、心肌缺血、再灌注損傷等導致竇房結功能下降,竇房、房內傳導延遲,繼而引發AF[40-41]。本研究結果發現旁路移植血管支數和房顫無關,但在敏感性分析中,改變效應模型后結果發生改變,說明統計結果不穩定,可能與納入研究報道較少有關,未來需要更多高質量研究來驗證這一結果。因此,醫護人員應術前合理安排手術流程,聯合麻醉醫師等多學科團隊,共同制定手術計劃,術中保證心肌供血,減少不必要的損傷,縮短手術時間,降低POAF發生風險。
3.4 術后因素
本次研究結果顯示,機械通氣時間與OPCABG患者新發POAF密切相關。Dave等[42]學者發現,機械通氣時間>24 h與POAF的發生呈正相關。機械通氣時間不僅在一定程度上體現了患者病情嚴重程度,而且機械通氣時間延長會導致肺泡損傷,延緩康復進程[43]。有研究[29, 44]報道SinoSCORE評分系統對OPCABG術后機械通氣時間延長有一定的預測價值,可以為術前準備,手術決策及術后干預提供參考依據,因此,建議術前應用SinoSCORE評分系統進行機械通氣時間延長風險評估。另外,指南[30]指出,CABG患者術后易出現肺功能降低,應完善術前預康復,指導患者進行呼吸訓練,有效咳嗽,降低術后機械通氣時間;擬脫機患者,應結合血氣、胸片等綜合評估,階梯調節呼吸參數,配合呼吸機進行肺康復,避免二次插管。既往研究顯示,術后炎性指標的升高與POAF發生率存在一定相關性,有學者[3]認為,術后炎性因子導致細胞內鈣超載,心房細胞有效不應期及動作電位發生改變,引發AF;同時,鈣超載也可引起心肌細胞受損和凋亡,出現心房肌纖維化,影響心肌細胞電傳導,誘導AF發生。中性粒細胞和淋巴細胞水平比值(neutrophil-to-lymphocyte ratio,NLR)反映了兩個重要的免疫途徑[14]。Xu等[45]對2 766例患者數據進行Meta分析顯示,NLR是心臟手術后的獨立危險因素,對POAF的發生有預測價值,但該結果在本研究中并未得到驗證,可能與納入研究較少,且部分研究未說明是術前或術后NLR有關。
本研究的局限性:(1)本研究納入文獻多為病例對照,且為單中心,樣本量較小,可能會對研究結果產生一定影響;(2)本研究未納入灰色文獻,可能對研究結果產生偏倚;(3)本研究部分影響因素納入文獻和樣本量較少,可能對統計結果產生影響;(4)本研究納入的術中、術后危險因素、文獻較少,可能對研究結論產生偏倚。因此,今后仍需要開展多中心、大樣本、更全面的流行病學研究,尤其是對圍手術期可干預因素的探索,以明確OPCABG患者發生POAF的相關危險因素。
綜上所述,高齡、高血壓、EuroSCOREⅡ評分高、頻發房早或房速、有腦血管病史、LAD增大、LVEF降低、合并右冠脈狹窄、冠狀動脈三支病變、未使用β受體阻滯劑、手術時間延長、機械通氣時間延長是OPCABG患者新發POAF的危險因素。因此,臨床可根據臨床因素(高齡、高血壓等)與其他相關生理生化及影像學指標開發更綜合有效的OPCABG患者新發POAF預測工具,以更好的識別高風險患者,其預測準確性可靠性高于單一指標,更科學的指導臨床對于高危患者的識別及早期干預治療,從而減少術后并發癥以及改善患者預后。
利益沖突:無。
作者貢獻:木楠負責研究設計,研究注冊,研究實施,數據整理與分析,論文撰寫;何秋煜、陳名桂、黎鈺晴負責數據整理與分析;邱寅龍、張曉璇負責研究設計,論文審閱與修改。
冠狀動脈旁路移植術(coronary artery bypass grafting,CABG)是治療冠狀動脈粥樣硬化性心臟病(冠心病)的常用外科手段,與傳統的體外循環下CABG(on-pump coronary artery bypass grafting,ONCAB)相比,非體外循環下CABG(off-pump coronary artery bypass grafting,OPCABG)能夠降低全身系統性炎癥反應、減少主動脈插管及主動脈壁鉗夾過程中血管壁斑塊脫落等不良事件,從而降低患者的手術風險及術后并發癥發生率等[1],尤其是對高風險冠心病患者受益更多。術后心房顫動(postoperative atrial fibrillation,POAF)是OPCABG的常見并發癥之一,發生率為12%~40%,常見于術后2~4 d,第2 d是高峰期[2],可能引發患者腦卒中、出血、感染、腎衰竭、心臟驟停等,不但會延長患者住院時間,延緩康復進程,增加醫療費用[3],甚至導致術后30 d和6個月死亡率上升2倍[4]。雖然各學會已制訂POAF相關診療共識、意見[5],但在過去十幾年中POAF發病率并無明顯降低[4, 6]。因此,POAF的預防和管理成為亟待解決的問題。近年來有不少學者對POAF的預測因素進行研究,但各研究間納入分析危險因素和結果存在差異,且無全面綜合總結OPCABG患者發生POAF危險因素的系統評價。本研究通過對相關研究結果進行Meta分析,明確OPCABG患者發生POAF的危險因素,以期為臨床制訂預防、管理OPCABG患者發生POAF的策略提供依據。
1 資料與方法
1.1 納入和排除標準
納入標準:(1)研究類型:已公開發表的觀察性研究;(2)研究對象:確診為冠心病且行OPCABG的患者,不限國籍、種族;(3)暴露因素:與OPCABG患者新發POAF相關的患者基本情況、術前疾病情況、術前用藥情況、術中因素和術后因素,有≥2項研究報告的暴露因素即納入Meta分析;(4)結局指標:OPCABG新發POAF[7-9]的危險因素。排除標準:(1)無明確OPCABG后POAF診斷標準;(2)未排除術前合并房顫患者。(3)非中文或英文文獻;(4)無法提取數據或數據重復的文獻;(5)重復發表的文獻。
1.2 文獻檢索策略
于2022年9月,計算機檢索PubMed、EMbase、Web of Science、The Cochrane Library、中國知網、萬方數據知識服務平臺、維普網(VIP)、中國生物醫學信息數據庫(SinoMed)。檢索時間范圍為建庫至2022年9月。采用主題詞、自由詞相結合的方式。中文檢索詞包括:冠狀動脈旁路移植術、冠狀動脈搭橋術、冠脈旁路移植、冠脈搭橋術、非體外循環、不停跳、心房顫動、房顫、心房纖顫、危險因素、風險因素等;英文檢索詞為:coronary artery bypass,off pump/beating heart coronary artery bypass,atrial fibrillation/auricular fibrillation*/fibrillation*,atrial/POAF,risk factors/risk factor/risk predictor等。
1.3 文獻篩選與資料提取
由2位研究者(第1作者和第2作者)獨立篩選文獻、提取相關資料,再交叉核對,如存爭議,雙方討論或請第3位研究者(第3作者)仲裁。文獻篩選過程中,先用NoteExpress篩出重復文獻,閱讀文獻題目及摘要,選出初步符合納入標準的文獻(初篩);再通讀全文,根據納入和排除標準,確定最終納入分析的文獻(復篩);提取資料包括:作者、發表年份、地區、研究類型、樣本量、年齡、新發房顫發生率、暴露因素及結局測量相關數據。
1.4 納入研究的質量評價
病例對照研究及隊列研究使用紐卡斯爾-渥太華量表(Newcastle-Ottawa scale,NOS)評分[10],共8個條目,滿分為9分,≥7分為高質量研究。2名研究者(第1作者、第2作者)獨立進行文獻質量評價,均接受過系統的循證課程培訓。若2位研究者評分出現爭議由第3位研究者(第3作者,省級循證護理師)仲裁。
1.5 統計學分析
采用Stata12.0、RevMan 5.4軟件對數據進行分析。計數資料選擇比值比(odds ratio,OR)為效應指標,計量資料用加權均數差或標準化均屬差為效應指標,采用95%可信區間。若異質性檢驗P≥0.1,I2≤50%,表明研究具有同質性,采用固定效應模型;若I2≥50%,提示研究有異質性,采用隨機效應模型,通過敏感性分析或亞組分析尋找異質性來源,若異質性仍較大則進行描述性分析。采用Egger’s檢驗及漏斗圖對文章進行發表偏依分析。P≤0.05為差異有統計學意義。
1.6 研究注冊
本研究在英國國立衛生研究院(National Institute for Health Research,NIHR)PROSPERO數據庫注冊,注冊編號為:CRD42022364737。
2 結果
2.1 文獻檢索結果
根據文獻檢索策略共檢索出OPCABG術后新發POAF危險因素相關文獻830篇,進行文獻篩選后初步納入47篇文獻進行全文閱讀,最終納入18篇文獻[1-3, 8, 11-25];見圖1。納入研究均為病例對照研究,共6 354例OPCABG患者,POAF患者1 393例,非POAF患者4 961例,納入31項暴露因素。納入研究的NOS評分為6~8分;見表1。
 圖1
文獻檢索流程圖
圖1
文獻檢索流程圖
*所檢索數據庫的文獻數具體如下:CNKI(
2.2 Meta分析結果
2.2.1 患者自身因素
納入研究包括的患者自身因素有年齡、性別、體重指數(body mass index,BMI)、吸煙史、飲酒史、EuroSCOREⅡ評分、高血壓病史、糖尿病病史、心肌梗死病史、頻發房性早搏(房早)或房性心動過速(房速)、腎功能不全、高脂血癥、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)、腦血管病史。Meta分析結果顯示年齡、高血壓、EuroSCOREⅡ評分、頻發房早是OPCABG患者新發POAF的危險因素。性別、BMI、吸煙史、飲酒史、糖尿病史、腦血管病史、心肌梗死病史、腎功能不全、高脂血癥、COPD與OPCABG患者新發POAF無關;見表2。
2.2.2 術前因素
納入研究包括的術前因素包括C反應蛋白(C-reactiveprotein,CRP)、肌酐、總膽固醇、甘油三酯、低密度脂蛋白、左房內徑(left atrium diameter,LAD)、左室射血分數(left ventricular ejection fraction,LVEF)、合并右冠狀動脈狹窄、冠狀動脈三支病變、左主干病變、β受體阻滯劑、他汀類藥物、血管緊張素轉化酶抑制劑/血管緊張素受體拮抗劑。Meta分析結果顯示LAD、LVEF、合并右冠脈狹窄、冠狀動脈三支病變、未使用β受體阻滯劑是OPCABG患者新發POAF的術前危險因素。術前CRP、肌酐、總膽固醇、甘油三酯、低密度脂蛋白、左主干病變、使用他汀類藥物、使用血管緊張素轉化酶抑制劑/血管緊張素受體拮抗劑與OPCABG患者新發POAF無關;見表2。
2.2.3 術中因素
納入研究包括的術中因素包括旁路血管支數、手術時間。Meta分析結果顯示手術時間是OPCABG患者新發POAF的術中危險因素;旁路血管支數與OPCABG患者新發POAF無關;見表2。
2.2.4 術后因素
納入研究包括的術后因素包括術后NLR、機械通氣時間。Meta分析結果顯示、機械通氣時間[OR=2.85,95%CI(1.79,3.91),P<0.001]是OPCABG患者新發POAF的術后危險因素。術后NLR[OR=1.52,95%CI(-1.10,4.14),P=0.13]與OPCABG患者新發POAF無關;見表2。
2.2.5 敏感性分析
通過轉換隨機效應模型和固定效應模型進行敏感性分析。計算12項危險因素的合并OR值、95%CI,結果未見明顯改變,表明該部分結果穩定性較好、可信度高;見表3。
2.2.6 發表偏倚
采用Stata15.0進行Egger's檢驗進行發表偏倚分析。結果顯示,年齡(P=0.086)、性別(P=0.075)、吸煙史(P=0.325)、糖尿病(P=0.519)、LAD(P=0.574)、LVEF(P=0.314)、β受體阻滯劑(P=0.782)無明顯發表偏倚。。
3 討論
OPCABG是治療冠心病常用的手術方式,研究表明其能有效避免ONCAB因體外循環引發的全身炎癥反應、心肌缺血再灌注,一定程度上減少誘發心房顫動等不良事件[1]。但有學者[26-27]報道,盡管使用OPCABG,POAF仍有較高的發生率,而本研究同樣顯示發生率為12.5%~32.8%,處于較高水平。由此說明,可能存在除體外循環以外其他導致患者新發POAF的影響因素。盡管OPCABG術后新發POAF并不是發生持續AF的先兆,通常使用抗心律失常藥物或電復律后可恢復為竇性心律,普通患者可耐受,但對于心功能下降及冠心病高發的老年患者,術后早期心律失常會造成患者血流動力學不穩定、降低心排出量,增加患者卒中的風險,因此識別其危險因素至關重要。
3.1 患者自身因素
本Meta分析結果顯示,OPCABG患者新發POAF的患者自身影響因素有:(1)年齡是OPCABG患者新發POAF的重要危險因素。本研究結果顯示,年齡每增加1歲,患者POAF發生率增加近3倍,與既往研究結果相同。Mathew等[28]的研究表明,年齡每增加10歲,AF發生率增加75%,且年齡>70歲是POAF的高危因素,當年齡>72歲時,POAF發生率約為<55歲患者的4.4倍[19]。其潛在機制可能為:人體衰老過程中出現心功能進行性下降、心室重構、心肌細胞減少、剩余心肌細胞過度肥大、心肌纖維化等變化[2, 11],引起心內傳導系統紊亂并導致異常的折返通路[3],進而引發AF。雖然年齡是不可干預因素,醫護人員應加強對高齡OPCABG患者的術前預防,術中管理及術后觀察,形成老年患者規范化重點管理流程。(2)高血壓是OPCABG患者新發POAF的重要危險因素之一。本研究表明合并高血壓的患者發生POAF風險增加2倍,與既往研究[3, 12]結果相同。從病理生理角度分析:高血壓導致左心室順應性下降、舒張功能障礙、左室肥大,進而使左室充盈壓升高,冠脈血流灌注減少,刺激交感神經,激活腎素-血管緊張素-醛固酮系統(RAAS)[3, 11]。另外,兒茶酚胺分泌增多、神經內分泌紊亂、循環血容量失調和炎性反應增強均可導致心肌電活動不穩定,導致AF[13]。因此對于有高血壓的患者應提前進行干預,控制血壓在合適范圍。(3)頻發房顫和房早與OPCABG患者新發POAF存在相關性。頻發房顫和房早患者POAF風險增加3.7倍,可能與心房組織纖維化,激活RAAS系統有關,和高血壓引發POAF機制相似。盡早糾正房顫及房早在預防OPCABG患者新發POAF中至關重要。(4)EuroSCOREⅡ是預測心血管外科圍手術期風險的重要方式,分數高的患者可能在術后發生嚴重的炎癥反應,進而導致POAF的發生[29]。綜上所述,患者自身狀況是POAF不可忽略的重要因素,冠狀動脈旁路移植術后相關指南[30]指出,術前應對患者基本情況、心血管危險因素等做全面評估,盡早發現患者自身危險因素,積極干預,全面觀察,同時給予社會支持,緩解焦慮情緒引起的神經系統異常反應。
3.2 術前因素
Meta分析結果表明,術前危險因素有:(1)術前LAD增大、EF降低是OPCABG患者新發POAF的預測因素,原因可能是:心室重構或心肌纖維化,引起早期復極縮短、晚期復極延長、增加興奮性,引發心律失常,心律失常進而加重心房重構,進而引發POAF[31-33];兩項Meta分析結果顯示[34-35],EF降低與冠狀動脈旁路移植術后急性腎損傷、低氧血癥相關。因此應加強對EF降低患者的管理,降低術后相關并發癥。(2)右冠狀動脈狹窄可能導致竇房結動脈血流中斷、減少,進而導致竇房結缺血,房內傳導延遲,誘發POAF,右冠狀動脈作為OPGCABG患者新發POAF危險因素的研究有限,納入總樣本量較少,需要更多大樣本量的研究予以證實[2]。(3)冠狀動脈三支病變通常意味著患者病情較重,Lokshyn等的1項納入3340例冠脈造影患者的研究表明,在房顫組(30.5%)中,三支病變的發生率明顯高于竇性心律組(20.4%)。(3)OPCABG患者新發POAF受術前是否服用β受體阻滯劑影響。β受體阻滯劑作為第二類抗心律失常藥物,多篇指南[5, 36-38]將β受體阻滯劑作為CABG術前預防性用藥列入一級推薦。有研究[21, 39]認為,術后使用β受體阻滯劑可降低POAF的發生率,而術前使用繼而術后停藥使POAF發病率增加91%。對于擬行OPCABG的患者,無論是否急診手術,在時間允許的情況下,建議常規行心臟超聲檢查,以識別高危患者。圍手術期可使用β受體阻滯劑預防POAF的發生,術前使用者不建議術后立即停藥,應在患者病情穩定后循序漸進撤藥。
3.3 術中因素
對于術中相關參數,本研究發現手術時間長是OPCABG患者新發POAF的危險因素之一。OPCABG手術時間較長患者較短時間患者發生POAF的風險更高。可能是手術引發交感神經興奮,加之手術牽拉、心肌缺血、再灌注損傷等導致竇房結功能下降,竇房、房內傳導延遲,繼而引發AF[40-41]。本研究結果發現旁路移植血管支數和房顫無關,但在敏感性分析中,改變效應模型后結果發生改變,說明統計結果不穩定,可能與納入研究報道較少有關,未來需要更多高質量研究來驗證這一結果。因此,醫護人員應術前合理安排手術流程,聯合麻醉醫師等多學科團隊,共同制定手術計劃,術中保證心肌供血,減少不必要的損傷,縮短手術時間,降低POAF發生風險。
3.4 術后因素
本次研究結果顯示,機械通氣時間與OPCABG患者新發POAF密切相關。Dave等[42]學者發現,機械通氣時間>24 h與POAF的發生呈正相關。機械通氣時間不僅在一定程度上體現了患者病情嚴重程度,而且機械通氣時間延長會導致肺泡損傷,延緩康復進程[43]。有研究[29, 44]報道SinoSCORE評分系統對OPCABG術后機械通氣時間延長有一定的預測價值,可以為術前準備,手術決策及術后干預提供參考依據,因此,建議術前應用SinoSCORE評分系統進行機械通氣時間延長風險評估。另外,指南[30]指出,CABG患者術后易出現肺功能降低,應完善術前預康復,指導患者進行呼吸訓練,有效咳嗽,降低術后機械通氣時間;擬脫機患者,應結合血氣、胸片等綜合評估,階梯調節呼吸參數,配合呼吸機進行肺康復,避免二次插管。既往研究顯示,術后炎性指標的升高與POAF發生率存在一定相關性,有學者[3]認為,術后炎性因子導致細胞內鈣超載,心房細胞有效不應期及動作電位發生改變,引發AF;同時,鈣超載也可引起心肌細胞受損和凋亡,出現心房肌纖維化,影響心肌細胞電傳導,誘導AF發生。中性粒細胞和淋巴細胞水平比值(neutrophil-to-lymphocyte ratio,NLR)反映了兩個重要的免疫途徑[14]。Xu等[45]對2 766例患者數據進行Meta分析顯示,NLR是心臟手術后的獨立危險因素,對POAF的發生有預測價值,但該結果在本研究中并未得到驗證,可能與納入研究較少,且部分研究未說明是術前或術后NLR有關。
本研究的局限性:(1)本研究納入文獻多為病例對照,且為單中心,樣本量較小,可能會對研究結果產生一定影響;(2)本研究未納入灰色文獻,可能對研究結果產生偏倚;(3)本研究部分影響因素納入文獻和樣本量較少,可能對統計結果產生影響;(4)本研究納入的術中、術后危險因素、文獻較少,可能對研究結論產生偏倚。因此,今后仍需要開展多中心、大樣本、更全面的流行病學研究,尤其是對圍手術期可干預因素的探索,以明確OPCABG患者發生POAF的相關危險因素。
綜上所述,高齡、高血壓、EuroSCOREⅡ評分高、頻發房早或房速、有腦血管病史、LAD增大、LVEF降低、合并右冠脈狹窄、冠狀動脈三支病變、未使用β受體阻滯劑、手術時間延長、機械通氣時間延長是OPCABG患者新發POAF的危險因素。因此,臨床可根據臨床因素(高齡、高血壓等)與其他相關生理生化及影像學指標開發更綜合有效的OPCABG患者新發POAF預測工具,以更好的識別高風險患者,其預測準確性可靠性高于單一指標,更科學的指導臨床對于高危患者的識別及早期干預治療,從而減少術后并發癥以及改善患者預后。
利益沖突:無。
作者貢獻:木楠負責研究設計,研究注冊,研究實施,數據整理與分析,論文撰寫;何秋煜、陳名桂、黎鈺晴負責數據整理與分析;邱寅龍、張曉璇負責研究設計,論文審閱與修改。