隨著胸部CT的廣泛使用,肺結節的檢出率大幅提高。在行胸部CT檢查的人群中約50%的患者出現肺結節,而大約95%的肺結節是良性病變[1]。檢出肺結節的患者常通過隨訪,動態觀察肺結節生長情況。而判斷良惡性是決定肺結節是否手術至關重要的一環。目前常采用的檢查方法包括胸部CT,正電子發射計算機斷層掃描(positron emission tomography/computed tomography,PET/CT),支氣管鏡或經胸穿刺活檢的非手術活檢等[2]。與侵入性病理活檢相比,影像學方法具有無創、快速、可重復等優點。高質量的影像數據可以為肺結節良惡性的鑒別提供有用信息。18F-FDG PET/CT通過注射放射性核素F-18標記病變區域,再采用螺旋CT掃描全身的方法,可以提供腫瘤本身和全身轉移的全面信息。然而,由于受炎癥等因素影響,PET/CT給出的診斷信息依然有限。一項Meta分析[3]顯示,18F-FDG PET/CT在診斷惡性孤立性肺結節方面的敏感性和特異性均不夠理想。胸部CT作為肺結節檢出與隨訪的最常見手段,通過薄層掃描可得到肺結節清晰的二維形態,可提取出如毛刺征、胸膜牽拉、血管征等特異性影像學特征,再通過三維重建技術可以得到更加直觀的結節圖像及更全面的參數信息。但由于CT三維重建局限于結節本身,給出的信息較為有限,所以,為了提高整體診斷效率,我們假設18F-FDG PET/CT聯合CT三維重建建立影像組學預測模型可以提高肺小結節的診斷效率。基于這一假設,本研究構建了肺結節的CT三維重建和PET/CT預測模型,并聯合兩種模型比較其診斷效能,探討在肺結節診斷中的應用價值。
1 資料與方法
1.1 臨床資料
回顧性收集2020年7月—2021年8月于江蘇省蘇北人民醫院胸外科行手術治療的肺結節患者的臨床病理資料。納入標準:(1)術前2周內行18F-FDG PET/CT掃描;(2)術前2周內行胸部增強CT并可獲得原始圖像;(3)患者有完整的臨床和病理資料。排除標準:(1)術前接受過抗腫瘤治療者;(2)有既往惡性腫瘤史者;(3)病理診斷不明確;(4)CT圖像質量差或信息不全;(5)原發結節直徑>3 cm;(6)結節內明顯鈣化。收集患者年齡、性別、吸煙史等一般臨床資料。
1.2 胸部增強CT掃描和重建
所有的掃描均在320層CT機上進行的(Aquilino ONE,日本)。采用標準的肺尖至上腹部增強成像方案,參數如下:仰臥位,吸氣后屏氣,旋轉時間0.5 s,準直度320 mm×0.5 mm,電子管電壓120 kVp,螺距 0.828。軸向圖像以1 mm或1.25 mm的切片厚度重建。所有圖像都被傳輸到圖片存檔及通信系統,并在脫機工作站Mimics Medical 21.0(Materialise NV,比利時)中進行三維重建。首先,使用“ Dynamic Region Grow”功能來分割結節并創建相應的蒙版“Mask”,然后使用“Edit mask”功能編輯,刪除冗余區域,并繪制未捕獲的結節區域。最后,應用“Calculate part”功能重建肺結節的三維形態。三維重建處理由兩位胸外科主治以上醫生獨立完成,結果取其平均值。
1.3 18F-FDG PET/CT掃描和分析
患者禁食6 h,血糖濃度<10 mmol/L,靜脈滴注18F-FDG 3.14~5.11 MBq/kg。注射后,患者在安靜的房間休息60 min,然后使用Discovery VCT 64 PET/CT系統(GE Healthcare,美國)進行成像。成像時,患者取仰臥位,雙臂向頭部方向伸展,平靜呼吸。通過在軸向PET圖像上繪制包含整個病灶和肺門/縱隔淋巴結的感興趣區域(region of interest,ROI)來測量對應的SUVmax。SUVmax值是由1位主治醫師以上影像學醫師在手術前獨立確定。
1.4 手術和病理評估
所有患者均行肺切除術,術前主刀醫生根據胸部CT三維重建的結節數目、大小和位置選擇合適的手術方式,包括楔形切除術、肺段切除術或肺葉切除術,若楔形切除后快速病理報告為浸潤性癌則需要進一步行肺葉切除術。術后標本進行常規病理檢查,必要時行免疫組織化學檢測進行鑒別診斷。病理結果根據2021年世界衛生組織肺腫瘤分類標準[3]進行分類。
1.5 統計學分析
所有統計分析均采用SPSS 22.0軟件(IBM,USA)。符合正態分布的連續變量用均數±標準差( ±s)描述,偏態分布的連續變量采用中位數(上下四分位數)[M(P25,P75)]描述。分類變量采用頻數和百分比描述。采用t檢驗和χ2檢驗比較兩組患者的基線特征。受試者工作特征(receiver operating characteristic,ROC)曲線篩選具有診斷效能的參數。采用逐步向前法進行logistic歸建模,將相關參數轉化為對應的模型。ROC曲線和CT直方圖的繪制使用GraphPad Prism 8.0.0,列線圖通過R4.1.3實現。P≤0.05為差異有統計學意義。
±s)描述,偏態分布的連續變量采用中位數(上下四分位數)[M(P25,P75)]描述。分類變量采用頻數和百分比描述。采用t檢驗和χ2檢驗比較兩組患者的基線特征。受試者工作特征(receiver operating characteristic,ROC)曲線篩選具有診斷效能的參數。采用逐步向前法進行logistic歸建模,將相關參數轉化為對應的模型。ROC曲線和CT直方圖的繪制使用GraphPad Prism 8.0.0,列線圖通過R4.1.3實現。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已通過蘇北人民醫院醫學倫理委員會審批,審批號:2021ky322。
2 結果
共納入125例患者,其中男57例(44.6%)、女68例(55.4%),年齡31~78(61.16±8.57)歲。肺葉切除術34例(27.2%),肺段/楔形切除術91例(72.8%)。經組織病理學證實,46例患者診斷為良性病變,其中炎性病變占比71.7%,79例患者診斷為惡性病變,其中肺腺癌占比92.4%。患者的臨床病理和影像學資料特征見表1。
 ]
]
我們從PET/CT和胸部增強CT三維重建中提取的兩個PET/CT參數均具有診斷意義,包括SUVmax≥1.5[AUC=0.688,95%CI(0.591,0.785),P<0.001],肺門/縱隔淋巴結代謝攝取升高[AUC=0.671,95%CI(0.575,0.766),P=0.001]。CT三維重建參數中CT直方圖峰[AUC=0.694,95%CI(0.601,0.787),P<0.001]、三維形狀[AUC=0.652,95%CI(0.549,0.756),P=0.005]、含磨玻璃成分[AUC=0.659,95%CI(0.558,0.760),P=0.003]和平均CT值[AUC=0.652,95%CI(0.558,0.760),P=0.001]差異有統計學意義;見表2。
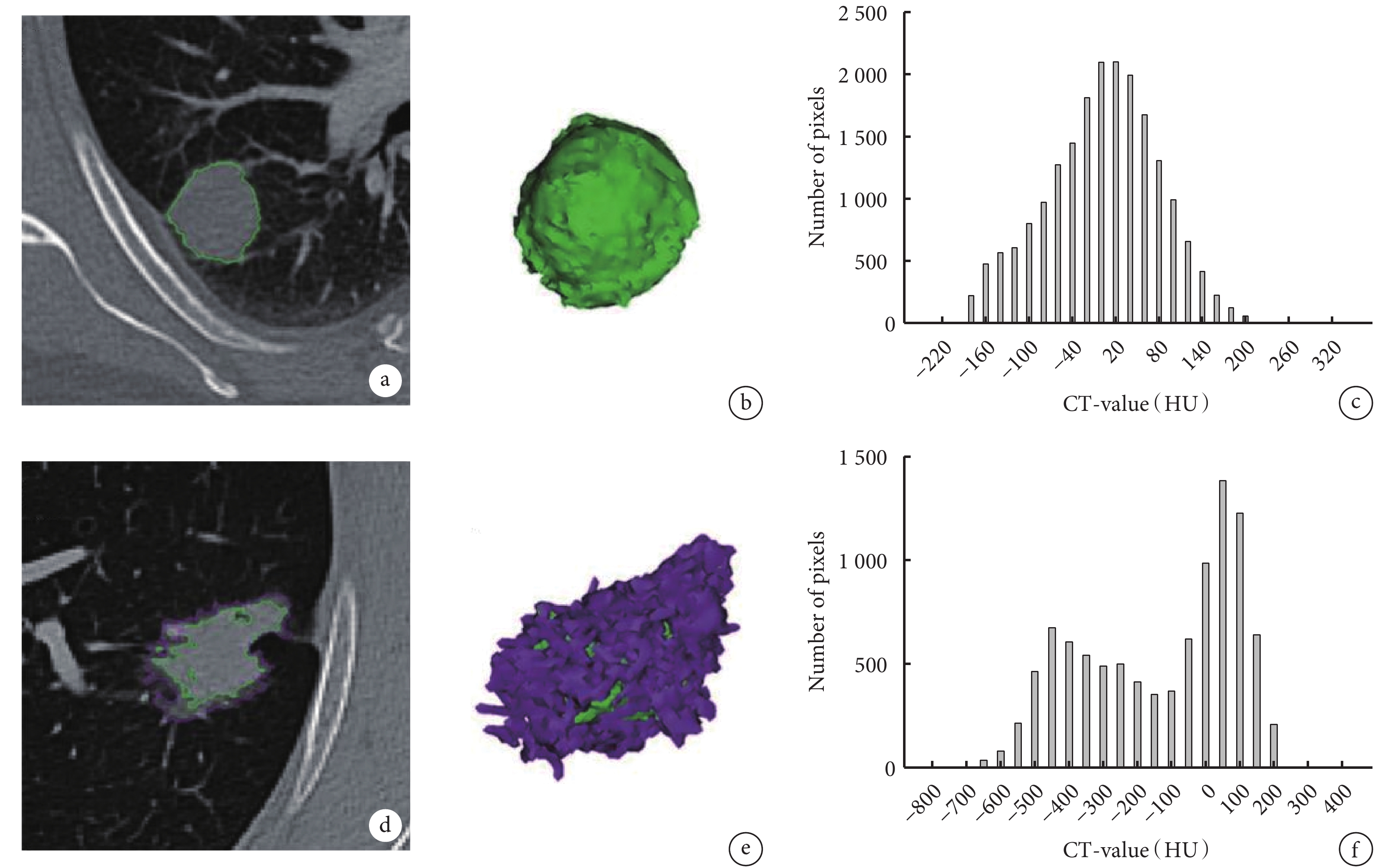
然后,我們通過二元logistic回歸將各類變量轉換為預測模型,其中PET/CT中SUVmax≥1.5和肺門/縱隔淋巴結代謝攝取增加成功納入模型,CT三維重建中CT直方圖峰數和三維形態成功納入模型,CT三維重建提取參數示例見圖1。分別建立PET/CT預測模型(MOD PET)、CT三維重建預測模型(MOD CT-3D)和PET/CT和CT三維重建聯合預測模型(MOD combination),二元logistic回歸模型見表3~4,模型列線圖見圖2。
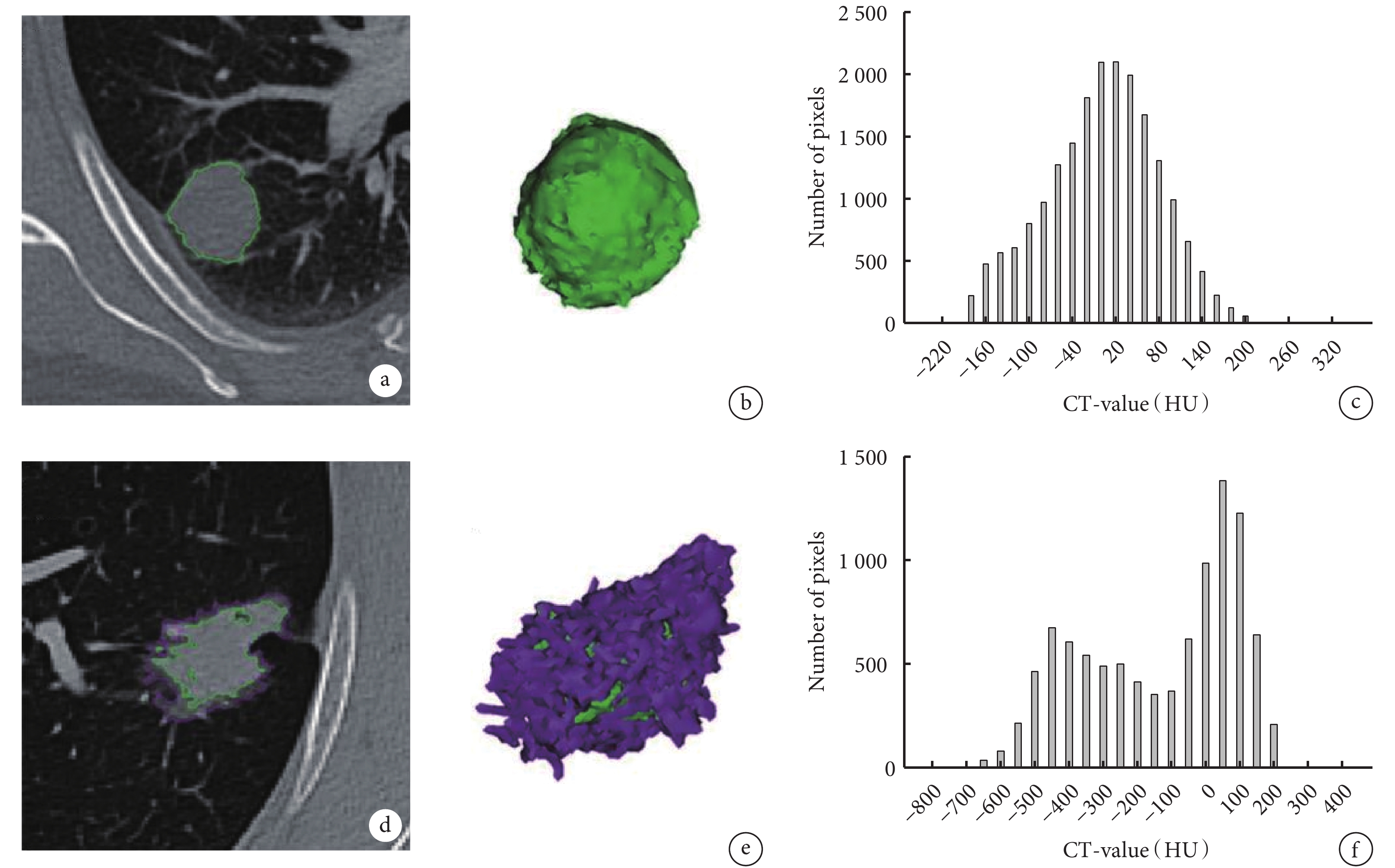 圖1
CT三維重建參數提取實例
圖1
CT三維重建參數提取實例
病例1(a~c)為肉芽腫性炎癥(良性),a:軸位CT顯示實性結節;b:3D圖像形態規則;c:CT值直方圖顯示單峰;病例2(d~f)為肺腺癌(惡性),d:軸位CT顯示亞實性;e:三維圖像形態不規則;f:CT值直方圖呈現兩個峰
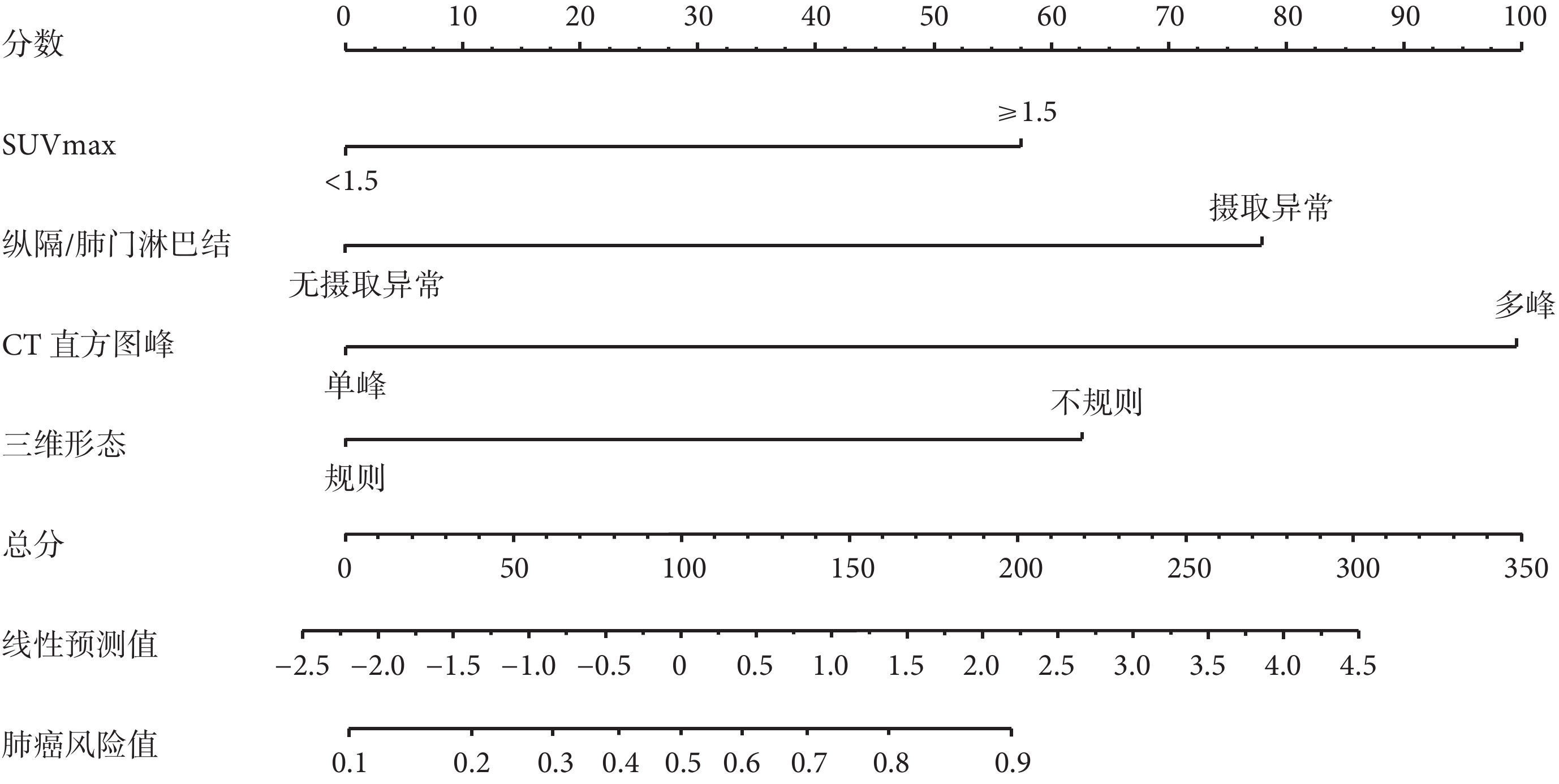
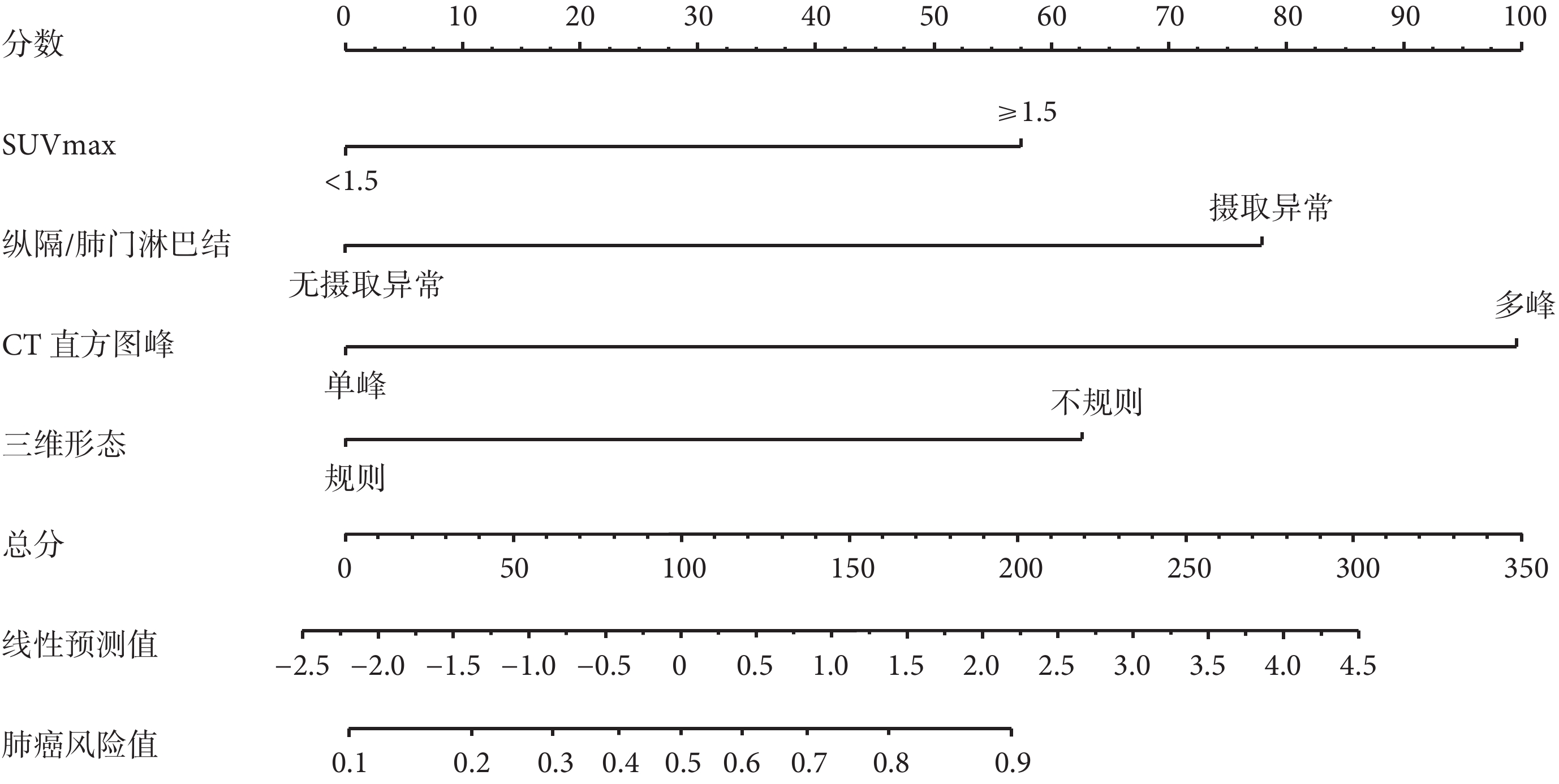 圖2
PET/CT聯合CT三維重建預測模型的列線圖
圖2
PET/CT聯合CT三維重建預測模型的列線圖
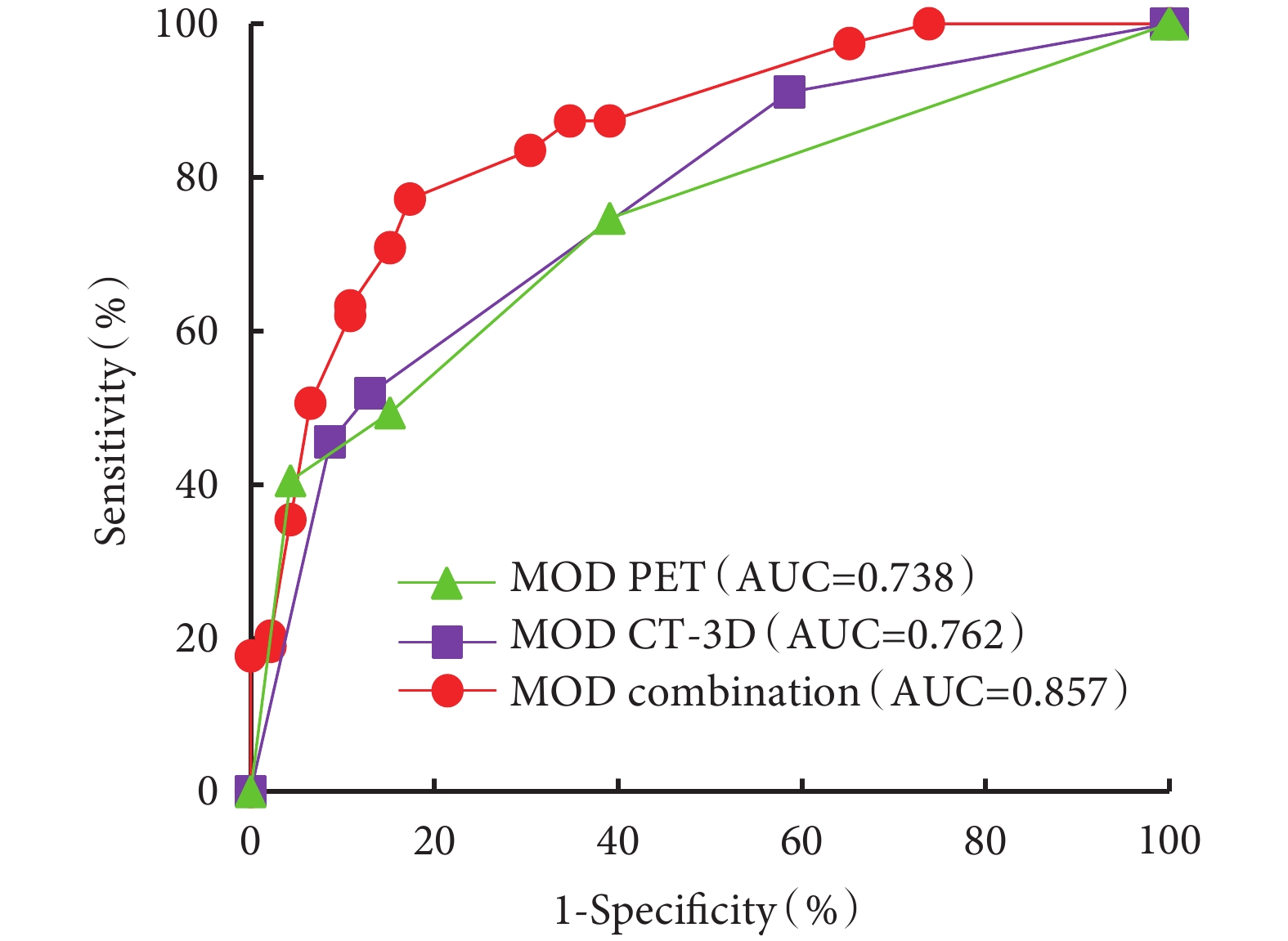 圖3
3種預測模型的受試者工作特征曲線
圖3
3種預測模型的受試者工作特征曲線
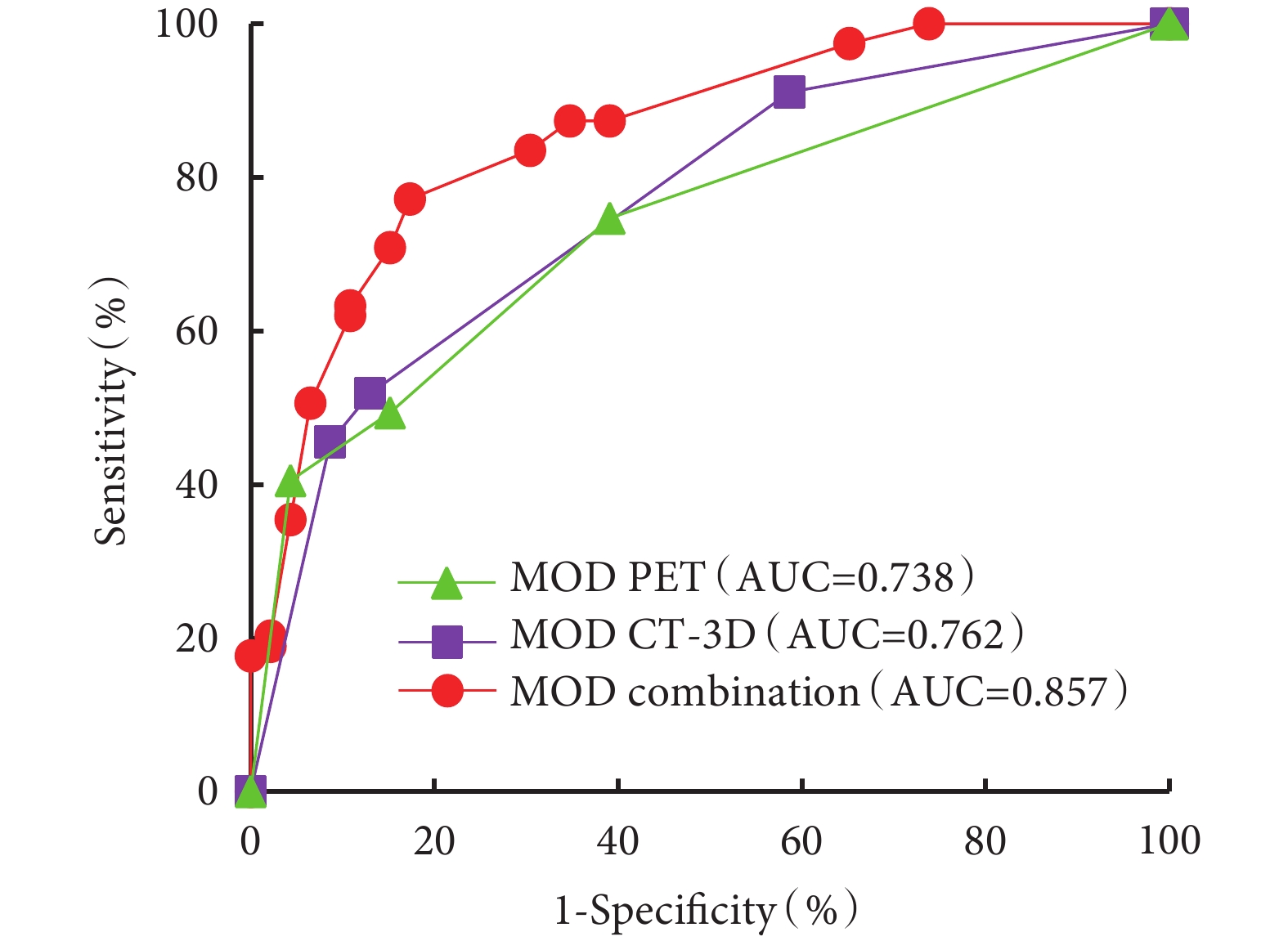
MOD PET:PET/CT預測模型;MOD CT-3D:CT三維重建預測模型;MOD combination:PET/CT和CT三維重建聯合預測模型
最后,使用ROC驗證模型的診斷效能,得到MOD PET的AUC為0.738[95%CI(0.651,0.824)],敏感性為74.7%,特異性為60.9%;MOD CT-3D的AUC為0.762[95%CI(0.677,0.848)],敏感性為51.9%,特異性為87.0%;MOD combination的AUC為0.857[95%CI(0.789,0.925)],敏感性77.2%,特異性82.6%,差異均有統計學意義(P<0.001);見表5和圖3。
3 討論
在本研究中,我們應用18F-FDG PET/CT和增強CT三維重建鑒別肺結節良惡性病變。通過比較PET/CT預測模型、CT三維重建預測模型以及兩者聯合預測模型的AUC,研究發現聯合診斷具有更好的診斷效能。
18F-FDG PET/CT可以揭示器官的代謝特征,腫瘤細胞糖酵解作用增強,可作為肺結節的有效的無創檢查。既往研究[4]表明,PET/CT可以幫助臨床醫師決定對低劑量CT篩查出的肺結節患者進行常規隨訪或病理活檢,并且可預測早期肺腺癌浸潤性,可有效鑒別浸潤性病變和浸潤前病變[5],判斷有無淋巴結轉移[6]。本研究顯示,PET/CT獲得結節SUVmax和肺門/縱隔淋巴結異常的代謝攝取均對肺結節良惡性鑒別有診斷效能(AUC分別為0.688和0.671)。我們分析了SUVmax的不同截斷值,發現在本研究中最優截斷值為1.5。相比之下,以往的研究[7-8]大多采用2.5作為SUVmax的最佳截斷值。這或許與本研究選取的肺結節直徑在3cm之內,其SUVmax的靈敏性相對較高有關,但對于肺小結節的普適性還有待進一步研究。由于PET/CT費用偏高,實際臨床中并不是常規開展肺結節PET/CT檢查,我們選取的患者往往是在常規胸部CT檢查后發現結節表現明顯的血管征、毛刺征、胸膜牽拉征等侵襲影像學表現,或結節倍增時間明顯縮短、密度增加等結節生長加速表現后再進一步行PET/CT檢查。由于肺結節隨訪過程中不常規行PET/CT檢查,限制PET/CT聯合CT三維重建的臨床應用,但對于高危肺結節得到PET/CT檢查再聯合CT三維重建技術可明顯提高影像學對肺結節的鑒別能力,且充分利用了患者的影像學資料,具有較大的臨床價值。
本研究采用CT三維重建技術來進行密度形態可視化。相對二維掃描圖像,三維重建可獲得有更加全面具體的結節信息,可在一定程度上彌補PET/CT低特異性的不足。其中,本研究提取的CT值直方圖的峰值數利用了整個肺結節密度值的整體分布。若整體密度分布均勻,則表現為單峰,范圍小;若分布不均勻,則出現多峰或無峰,且CT值范圍較大。此方法與磨玻璃/實性成分比(G/S)的鑒別方法相比,兩者既有聯系又有區別。兩者都能反映結節密度的差異。G/S法主要考慮結節周圍的磨玻璃成分,與腫瘤浸潤有關。CT直方圖峰涵蓋整個結節的實性和磨玻璃成分比較,與腫瘤惡性程度具有一定相關性。Li等[9]發現高實性成分更有可能伴隨EGFR、TP53、 RBM10和 ARID1B基因突變。Peng等[10]認為CT峰值可能有助于區分浸潤前與浸潤性腺癌。本研究中使用的CT直方圖峰數通過密度分布可視化,更加直觀顯示密度分布差異。CT直方圖峰數對結節良惡性有鑒別意義[AUC=0.694,95%CI(0.601,0.787)]。
隨著大數據時代的發展,加上人工智能在醫學領域的應用,肺結節診斷逐漸從肉眼觀察轉變到人工智能模式,計算機可以通過學習大量的影像組學數據,建立有效的診斷模型,并可在運行中不斷調整優化[11-12],這種利用大數據和人工智能的模式是未來的主要發展趨勢。在低劑量CT篩查中利用對影像組學的深度學習可很好地預測肺結節的良惡性[13]。利用深度學習可提高肺結節的診斷效能[14-15]。本研究為肺結節人工智能的發展提供了良好的思路,整合多種可用的影像學資料進行聯合診斷,提升了診斷效能。能夠更加精準地鑒別出需要及時手術干預的惡性肺結節;而對于惰性肺結節,可以繼續隨訪,從而減少沒必要的手術治療。
本研究存在一些局限性。首先,本研究為單中心回顧性研究,樣本量相對較少,有待進一步在多中心的大樣本中驗證,提高預測模型的準確度。其次,本研究中計算機輔助下的CT三維重建技術在確定選區時有一定的人為選擇因素,可能會對結果帶來人為偏差,需進一步改進重建技術。最后,本研究方法應用范圍有限,對于大部分肺結節,尤其是磨玻璃結節,單獨使用胸部CT進行復查隨訪是首要選擇,本研究更適用于需要進一步行PET/CT檢查的高危肺結節的鑒別診斷。
綜上所述,18F-FDG PET/CT與三維CT重建聯合可提高肺結節良惡性鑒別的診斷效率。該方法能在肺結節隨訪過程中,更加準確地把握肺結節手術時機以及選擇合適的手術方式。同時,本研究也可為肺結節診斷人工智能化提供有用的理論依據。
利益沖突:無。
作者貢獻:陳勇負責論文設計與撰寫,數據整理與分析;吳俊負責數據收集和整理;陸世春、孫超負責數據處理;王霄霖、束余聲負責論文設計、審閱與修改。
隨著胸部CT的廣泛使用,肺結節的檢出率大幅提高。在行胸部CT檢查的人群中約50%的患者出現肺結節,而大約95%的肺結節是良性病變[1]。檢出肺結節的患者常通過隨訪,動態觀察肺結節生長情況。而判斷良惡性是決定肺結節是否手術至關重要的一環。目前常采用的檢查方法包括胸部CT,正電子發射計算機斷層掃描(positron emission tomography/computed tomography,PET/CT),支氣管鏡或經胸穿刺活檢的非手術活檢等[2]。與侵入性病理活檢相比,影像學方法具有無創、快速、可重復等優點。高質量的影像數據可以為肺結節良惡性的鑒別提供有用信息。18F-FDG PET/CT通過注射放射性核素F-18標記病變區域,再采用螺旋CT掃描全身的方法,可以提供腫瘤本身和全身轉移的全面信息。然而,由于受炎癥等因素影響,PET/CT給出的診斷信息依然有限。一項Meta分析[3]顯示,18F-FDG PET/CT在診斷惡性孤立性肺結節方面的敏感性和特異性均不夠理想。胸部CT作為肺結節檢出與隨訪的最常見手段,通過薄層掃描可得到肺結節清晰的二維形態,可提取出如毛刺征、胸膜牽拉、血管征等特異性影像學特征,再通過三維重建技術可以得到更加直觀的結節圖像及更全面的參數信息。但由于CT三維重建局限于結節本身,給出的信息較為有限,所以,為了提高整體診斷效率,我們假設18F-FDG PET/CT聯合CT三維重建建立影像組學預測模型可以提高肺小結節的診斷效率。基于這一假設,本研究構建了肺結節的CT三維重建和PET/CT預測模型,并聯合兩種模型比較其診斷效能,探討在肺結節診斷中的應用價值。
1 資料與方法
1.1 臨床資料
回顧性收集2020年7月—2021年8月于江蘇省蘇北人民醫院胸外科行手術治療的肺結節患者的臨床病理資料。納入標準:(1)術前2周內行18F-FDG PET/CT掃描;(2)術前2周內行胸部增強CT并可獲得原始圖像;(3)患者有完整的臨床和病理資料。排除標準:(1)術前接受過抗腫瘤治療者;(2)有既往惡性腫瘤史者;(3)病理診斷不明確;(4)CT圖像質量差或信息不全;(5)原發結節直徑>3 cm;(6)結節內明顯鈣化。收集患者年齡、性別、吸煙史等一般臨床資料。
1.2 胸部增強CT掃描和重建
所有的掃描均在320層CT機上進行的(Aquilino ONE,日本)。采用標準的肺尖至上腹部增強成像方案,參數如下:仰臥位,吸氣后屏氣,旋轉時間0.5 s,準直度320 mm×0.5 mm,電子管電壓120 kVp,螺距 0.828。軸向圖像以1 mm或1.25 mm的切片厚度重建。所有圖像都被傳輸到圖片存檔及通信系統,并在脫機工作站Mimics Medical 21.0(Materialise NV,比利時)中進行三維重建。首先,使用“ Dynamic Region Grow”功能來分割結節并創建相應的蒙版“Mask”,然后使用“Edit mask”功能編輯,刪除冗余區域,并繪制未捕獲的結節區域。最后,應用“Calculate part”功能重建肺結節的三維形態。三維重建處理由兩位胸外科主治以上醫生獨立完成,結果取其平均值。
1.3 18F-FDG PET/CT掃描和分析
患者禁食6 h,血糖濃度<10 mmol/L,靜脈滴注18F-FDG 3.14~5.11 MBq/kg。注射后,患者在安靜的房間休息60 min,然后使用Discovery VCT 64 PET/CT系統(GE Healthcare,美國)進行成像。成像時,患者取仰臥位,雙臂向頭部方向伸展,平靜呼吸。通過在軸向PET圖像上繪制包含整個病灶和肺門/縱隔淋巴結的感興趣區域(region of interest,ROI)來測量對應的SUVmax。SUVmax值是由1位主治醫師以上影像學醫師在手術前獨立確定。
1.4 手術和病理評估
所有患者均行肺切除術,術前主刀醫生根據胸部CT三維重建的結節數目、大小和位置選擇合適的手術方式,包括楔形切除術、肺段切除術或肺葉切除術,若楔形切除后快速病理報告為浸潤性癌則需要進一步行肺葉切除術。術后標本進行常規病理檢查,必要時行免疫組織化學檢測進行鑒別診斷。病理結果根據2021年世界衛生組織肺腫瘤分類標準[3]進行分類。
1.5 統計學分析
所有統計分析均采用SPSS 22.0軟件(IBM,USA)。符合正態分布的連續變量用均數±標準差( ±s)描述,偏態分布的連續變量采用中位數(上下四分位數)[M(P25,P75)]描述。分類變量采用頻數和百分比描述。采用t檢驗和χ2檢驗比較兩組患者的基線特征。受試者工作特征(receiver operating characteristic,ROC)曲線篩選具有診斷效能的參數。采用逐步向前法進行logistic歸建模,將相關參數轉化為對應的模型。ROC曲線和CT直方圖的繪制使用GraphPad Prism 8.0.0,列線圖通過R4.1.3實現。P≤0.05為差異有統計學意義。
±s)描述,偏態分布的連續變量采用中位數(上下四分位數)[M(P25,P75)]描述。分類變量采用頻數和百分比描述。采用t檢驗和χ2檢驗比較兩組患者的基線特征。受試者工作特征(receiver operating characteristic,ROC)曲線篩選具有診斷效能的參數。采用逐步向前法進行logistic歸建模,將相關參數轉化為對應的模型。ROC曲線和CT直方圖的繪制使用GraphPad Prism 8.0.0,列線圖通過R4.1.3實現。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已通過蘇北人民醫院醫學倫理委員會審批,審批號:2021ky322。
2 結果
共納入125例患者,其中男57例(44.6%)、女68例(55.4%),年齡31~78(61.16±8.57)歲。肺葉切除術34例(27.2%),肺段/楔形切除術91例(72.8%)。經組織病理學證實,46例患者診斷為良性病變,其中炎性病變占比71.7%,79例患者診斷為惡性病變,其中肺腺癌占比92.4%。患者的臨床病理和影像學資料特征見表1。
 ]
]
我們從PET/CT和胸部增強CT三維重建中提取的兩個PET/CT參數均具有診斷意義,包括SUVmax≥1.5[AUC=0.688,95%CI(0.591,0.785),P<0.001],肺門/縱隔淋巴結代謝攝取升高[AUC=0.671,95%CI(0.575,0.766),P=0.001]。CT三維重建參數中CT直方圖峰[AUC=0.694,95%CI(0.601,0.787),P<0.001]、三維形狀[AUC=0.652,95%CI(0.549,0.756),P=0.005]、含磨玻璃成分[AUC=0.659,95%CI(0.558,0.760),P=0.003]和平均CT值[AUC=0.652,95%CI(0.558,0.760),P=0.001]差異有統計學意義;見表2。
然后,我們通過二元logistic回歸將各類變量轉換為預測模型,其中PET/CT中SUVmax≥1.5和肺門/縱隔淋巴結代謝攝取增加成功納入模型,CT三維重建中CT直方圖峰數和三維形態成功納入模型,CT三維重建提取參數示例見圖1。分別建立PET/CT預測模型(MOD PET)、CT三維重建預測模型(MOD CT-3D)和PET/CT和CT三維重建聯合預測模型(MOD combination),二元logistic回歸模型見表3~4,模型列線圖見圖2。
 圖1
CT三維重建參數提取實例
圖1
CT三維重建參數提取實例
病例1(a~c)為肉芽腫性炎癥(良性),a:軸位CT顯示實性結節;b:3D圖像形態規則;c:CT值直方圖顯示單峰;病例2(d~f)為肺腺癌(惡性),d:軸位CT顯示亞實性;e:三維圖像形態不規則;f:CT值直方圖呈現兩個峰
 圖2
PET/CT聯合CT三維重建預測模型的列線圖
圖2
PET/CT聯合CT三維重建預測模型的列線圖
 圖3
3種預測模型的受試者工作特征曲線
圖3
3種預測模型的受試者工作特征曲線
MOD PET:PET/CT預測模型;MOD CT-3D:CT三維重建預測模型;MOD combination:PET/CT和CT三維重建聯合預測模型
最后,使用ROC驗證模型的診斷效能,得到MOD PET的AUC為0.738[95%CI(0.651,0.824)],敏感性為74.7%,特異性為60.9%;MOD CT-3D的AUC為0.762[95%CI(0.677,0.848)],敏感性為51.9%,特異性為87.0%;MOD combination的AUC為0.857[95%CI(0.789,0.925)],敏感性77.2%,特異性82.6%,差異均有統計學意義(P<0.001);見表5和圖3。
3 討論
在本研究中,我們應用18F-FDG PET/CT和增強CT三維重建鑒別肺結節良惡性病變。通過比較PET/CT預測模型、CT三維重建預測模型以及兩者聯合預測模型的AUC,研究發現聯合診斷具有更好的診斷效能。
18F-FDG PET/CT可以揭示器官的代謝特征,腫瘤細胞糖酵解作用增強,可作為肺結節的有效的無創檢查。既往研究[4]表明,PET/CT可以幫助臨床醫師決定對低劑量CT篩查出的肺結節患者進行常規隨訪或病理活檢,并且可預測早期肺腺癌浸潤性,可有效鑒別浸潤性病變和浸潤前病變[5],判斷有無淋巴結轉移[6]。本研究顯示,PET/CT獲得結節SUVmax和肺門/縱隔淋巴結異常的代謝攝取均對肺結節良惡性鑒別有診斷效能(AUC分別為0.688和0.671)。我們分析了SUVmax的不同截斷值,發現在本研究中最優截斷值為1.5。相比之下,以往的研究[7-8]大多采用2.5作為SUVmax的最佳截斷值。這或許與本研究選取的肺結節直徑在3cm之內,其SUVmax的靈敏性相對較高有關,但對于肺小結節的普適性還有待進一步研究。由于PET/CT費用偏高,實際臨床中并不是常規開展肺結節PET/CT檢查,我們選取的患者往往是在常規胸部CT檢查后發現結節表現明顯的血管征、毛刺征、胸膜牽拉征等侵襲影像學表現,或結節倍增時間明顯縮短、密度增加等結節生長加速表現后再進一步行PET/CT檢查。由于肺結節隨訪過程中不常規行PET/CT檢查,限制PET/CT聯合CT三維重建的臨床應用,但對于高危肺結節得到PET/CT檢查再聯合CT三維重建技術可明顯提高影像學對肺結節的鑒別能力,且充分利用了患者的影像學資料,具有較大的臨床價值。
本研究采用CT三維重建技術來進行密度形態可視化。相對二維掃描圖像,三維重建可獲得有更加全面具體的結節信息,可在一定程度上彌補PET/CT低特異性的不足。其中,本研究提取的CT值直方圖的峰值數利用了整個肺結節密度值的整體分布。若整體密度分布均勻,則表現為單峰,范圍小;若分布不均勻,則出現多峰或無峰,且CT值范圍較大。此方法與磨玻璃/實性成分比(G/S)的鑒別方法相比,兩者既有聯系又有區別。兩者都能反映結節密度的差異。G/S法主要考慮結節周圍的磨玻璃成分,與腫瘤浸潤有關。CT直方圖峰涵蓋整個結節的實性和磨玻璃成分比較,與腫瘤惡性程度具有一定相關性。Li等[9]發現高實性成分更有可能伴隨EGFR、TP53、 RBM10和 ARID1B基因突變。Peng等[10]認為CT峰值可能有助于區分浸潤前與浸潤性腺癌。本研究中使用的CT直方圖峰數通過密度分布可視化,更加直觀顯示密度分布差異。CT直方圖峰數對結節良惡性有鑒別意義[AUC=0.694,95%CI(0.601,0.787)]。
隨著大數據時代的發展,加上人工智能在醫學領域的應用,肺結節診斷逐漸從肉眼觀察轉變到人工智能模式,計算機可以通過學習大量的影像組學數據,建立有效的診斷模型,并可在運行中不斷調整優化[11-12],這種利用大數據和人工智能的模式是未來的主要發展趨勢。在低劑量CT篩查中利用對影像組學的深度學習可很好地預測肺結節的良惡性[13]。利用深度學習可提高肺結節的診斷效能[14-15]。本研究為肺結節人工智能的發展提供了良好的思路,整合多種可用的影像學資料進行聯合診斷,提升了診斷效能。能夠更加精準地鑒別出需要及時手術干預的惡性肺結節;而對于惰性肺結節,可以繼續隨訪,從而減少沒必要的手術治療。
本研究存在一些局限性。首先,本研究為單中心回顧性研究,樣本量相對較少,有待進一步在多中心的大樣本中驗證,提高預測模型的準確度。其次,本研究中計算機輔助下的CT三維重建技術在確定選區時有一定的人為選擇因素,可能會對結果帶來人為偏差,需進一步改進重建技術。最后,本研究方法應用范圍有限,對于大部分肺結節,尤其是磨玻璃結節,單獨使用胸部CT進行復查隨訪是首要選擇,本研究更適用于需要進一步行PET/CT檢查的高危肺結節的鑒別診斷。
綜上所述,18F-FDG PET/CT與三維CT重建聯合可提高肺結節良惡性鑒別的診斷效率。該方法能在肺結節隨訪過程中,更加準確地把握肺結節手術時機以及選擇合適的手術方式。同時,本研究也可為肺結節診斷人工智能化提供有用的理論依據。
利益沖突:無。
作者貢獻:陳勇負責論文設計與撰寫,數據整理與分析;吳俊負責數據收集和整理;陸世春、孫超負責數據處理;王霄霖、束余聲負責論文設計、審閱與修改。